Clear Sky Science · de
Unstrukturierter, disulfidgebundener C‑Terminus in helminthischen α‑helicalen antimikrobiellen Peptiden verstärkt und moduliert ihre Aktivität
Warum winzige Parasitenmoleküle wichtig sind
Da die Antibiotikaresistenz zunimmt, suchen Forscher nach neuen Wegen, gefährliche Bakterien zu töten, ohne unsere eigenen Zellen zu schädigen. Eine vielversprechende Quelle sind antimikrobielle Peptide – kurze Proteinfragmente, die viele Organismen als natürliche Antibiotika verwenden. Diese Studie untersucht ein ungewöhnliches Peptid aus einem parasitären Plattwurm und zeigt, wie ein kleiner, lockerer Schwanz an einem Ende, durch eine chemische Bindung zusammengehalten, die Geschwindigkeit und Heftigkeit beeinflussen kann, mit der das Peptid Bakterien abtötet. Das Verständnis dieses eingebauten Regelrads könnte Wissenschaftlern helfen, intelligentere, präzisere Antibiotika‑Alternativen zu entwerfen.
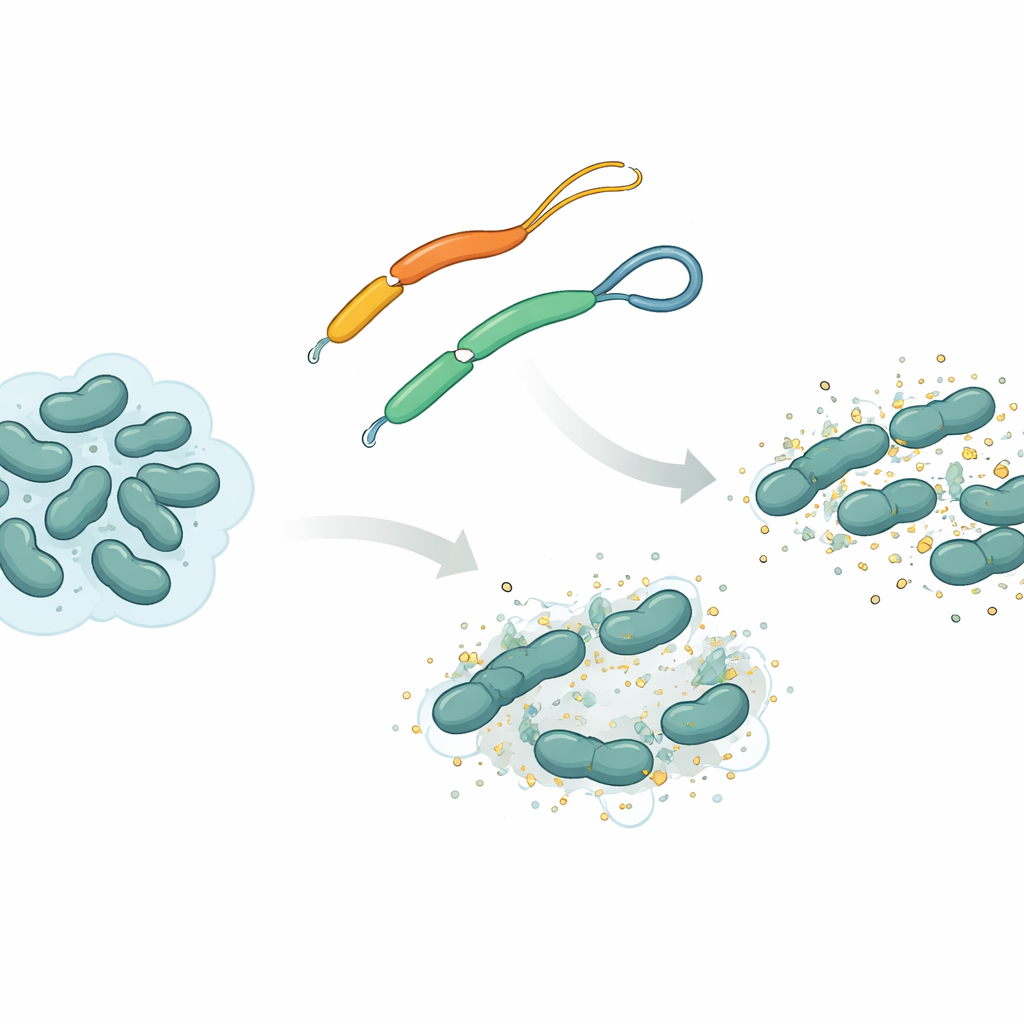
Eine natürliche Waffe aus Plattwürmern
Das Team konzentrierte sich auf ein antimikrobielles Peptid namens mesco‑2, gefunden im Plattwurm Mesocestoides corti. Wie viele solcher Peptide besitzt mesco‑2 einen starren, spiralförmigen „vorderen“ Abschnitt, der mit bakteriellen Membranen interagiert, sowie einen lockereren „Schwanz“ am Ende. In diesem Schwanz sind zwei schwefelhaltige Bausteine durch eine chemische Verbindung, die Disulfidbrücke, zu einer winzigen Schleife verknüpft. Die Forscher verglichen mesco‑2 mit einer nahezu identischen Variante, mesco‑2A, bei der diese Brücke entfernt wurde, sodass der Schwanz völlig offen ist. Diese kleine Änderung verändert die chemische Zusammensetzung insgesamt kaum, beeinflusst jedoch, wie sich das Peptid bewegen kann und wie es beim Angriff auf Bakterien reagiert.
Verborgene Muster in Parasitenabwehr
Bevor sie sich mesco‑2 selbst näher anschauten, durchsuchten die Wissenschaftler große Datenbanken mit vorhergesagten antimikrobiellen Peptiden aus Plattwürmern und vielen anderen Organismen. Sie suchten nach spezifischen Mustern, bei denen zwei schwefelhaltige Einheiten (Cysteine) durch einige andere Bausteine in der Nähe des Molekülendes getrennt sind. Sie fanden, dass ein „CXXXC“-Muster — dieselbe Abstandsanordnung wie in mesco‑2 — in Plattwurm‑Peptiden überraschend häufig vorkommt und oft in flexiblen Endsegmenten statt in wohlgeordneten Regionen sitzt. Computererzeugte 3D‑Modelle mehrerer solcher Peptide zeigten, dass diese cysteinreichen Motive üblicherweise in beweglichen Schwänzen liegen, was nahelegt, dass die Natur diese Schleifen bewusst in verschiebbaren Bereichen platziert, die das Verhalten des Peptids modulieren können.
Wie eine winzige Schleife Bewegung und Zusammenarbeit formt
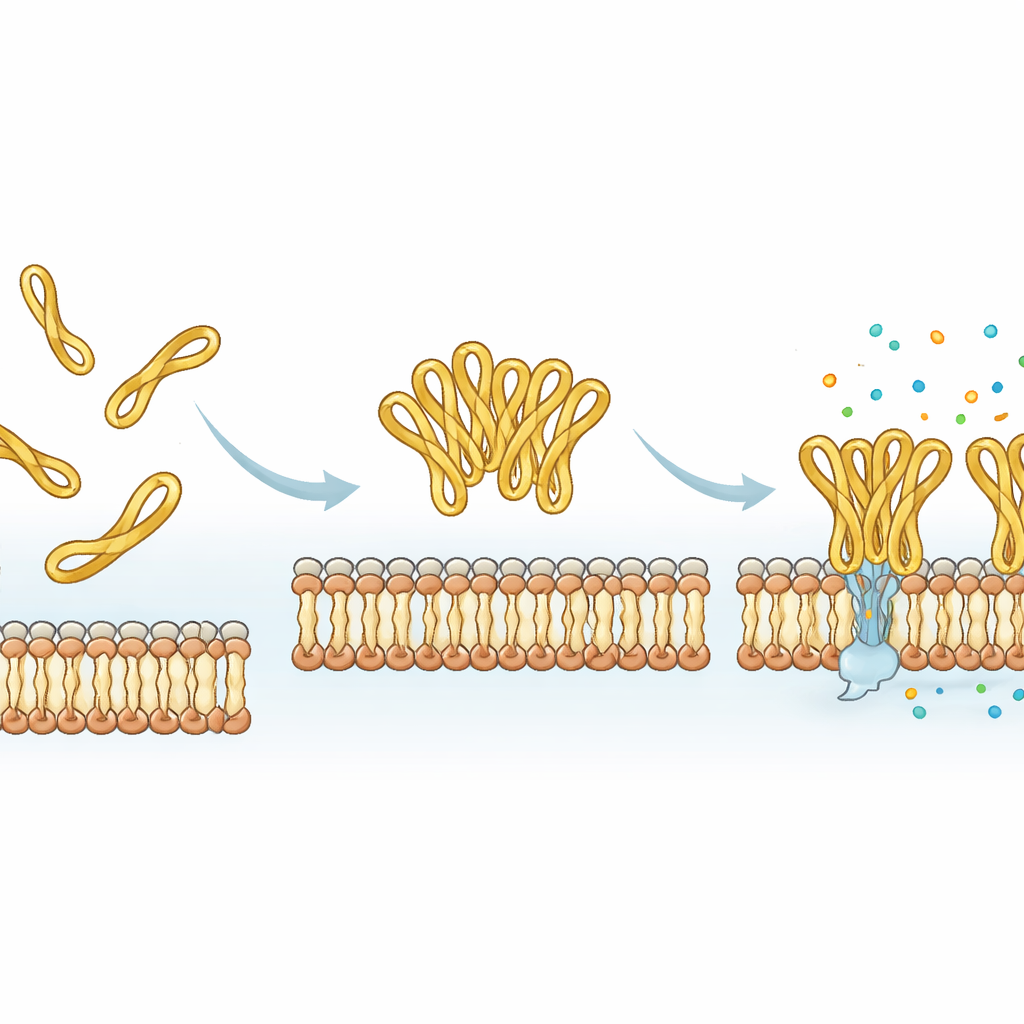
Mithilfe von Molekulardynamik‑Simulationen modellierten die Forscher, wie sich mesco‑2 und mesco‑2A in der Nähe einer vereinfachten bakteriellen Membran bewegen. Beide Versionen binden schnell an die Membranoberfläche, angetrieben von attraktiven Kräften zwischen positiven Ladungen auf dem Peptid und negativen Ladungen der bakteriellen Lipide. Die geschleifte Schwanzregion in mesco‑2 bewirkt jedoch, dass sich der zentrale Spiralkern an einer bestimmten Stelle kippt und eine Orientierung einnimmt, die eine partielle Insertion in die Membran fördert. Sie begünstigt außerdem, dass mehrere mesco‑2‑Moleküle sich zu kleinen Clustern zusammenfinden, insbesondere wenn ihre Schwänze nahe beieinander beginnen, und diese Verbände bleiben beim Andocken an die Membran zusammen. Im Gegensatz dazu ist das offen‑schwänzige mesco‑2A am Ende strukturflexibler, bildet nicht so leicht Cluster und verharrt eher als Einzelexemplar an der Oberfläche statt als koordiniert agierende Gruppe.
Von der Struktur zur bakteriellen Abtötung
Laborversuche bestätigten die Computermodelle. Wenn die Peptide mit einfachen Membranimitaten gemischt wurden, änderten sich beide in öligen oder detergenähnlichen Umgebungen wie erwartet – typisch für membranzielende Moleküle. Jedoch bildete mesco‑2 leichter eine regelmäßige Spiralstruktur und nahm auf negativ geladenen, bakterienähnlichen Membranen eine andere Gestalt an als mesco‑2A. In Tests gegen mehrere Bakterienarten zeigten beide Peptide starke antibakterielle Effekte bei ähnlicher Gesamtpotenz. Wichtige Unterschiede traten jedoch unterhalb der vollständig tödlichen Dosis auf. Mesco‑2 verlangsamte oder stoppte das bakterielle Wachstum viele Stunden lang selbst bei niedrigen Konzentrationen, während Bakterien, die mesco‑2A ausgesetzt waren, schneller wieder erholten. Zeitaufgelöste Messungen von Membranschäden zeigten, dass mesco‑2 Löcher in bakterielle Membranen deutlich schneller schlägt, während mesco‑2A langsamer wirkt, sofern nicht in höheren Dosen eingesetzt. Hochauflösende Bilder zeigten unterschiedliche Muster der Oberflächenschädigung, was wiederum auf verschiedene Mechanismen der Störung der bakteriellen Hülle hindeutet. Entscheidend ist, dass beide Peptide bei bakteriellen Wirkdosen nur geringe Schäden an menschlichen Immunzell‑Modellen verursachten, was auf einen günstigen Sicherheitsbereich schließen lässt.
Ein eingebautes Einstellrad zur Feinabstimmung von Peptidmedikamenten
Unter Einbeziehung aller Befunde zeigt die Studie, dass der kleine, disulfidgebundene Schwanz am Ende von mesco‑2 als molekulares Einstellrad wirkt: Er stabilisiert eine bestimmte geknickte Form, fördert die kooperative Clusterbildung der Peptide und beschleunigt die Membranstörung, alles ohne die Schädigung menschlicher Zellen wesentlich zu erhöhen. Das Entfernen der Schleife erleichtert die Synthese und kann sogar die Anzahl der Moleküle erhöhen, die an ein Modellmembran haften, verlangsamt jedoch den tatsächlichen Tötungsprozess und verändert die Art der Membranschädigung. Für zukünftige, auf solchen Peptiden basierende antibiotikaähnliche Wirkstoffe bedeutet dies, dass scheinbar kleine, flexible Endabschnitte — und nicht nur der Hauptspiralkern — gezielt verändert werden können, um zu steuern, wie schnell, wie stark und wie kooperativ ein Peptid Bakterien angreift.
Zitation: Budimir, A., Stojan, I., Primorac, K. et al. Unstructured, disulfide-bridged C-terminus in helminth α-helical antimicrobial peptides enhances and modulates their activity. Sci Rep 16, 14472 (2026). https://doi.org/10.1038/s41598-026-44795-9
Schlüsselwörter: antimikrobielle Peptide, Plattwurm‑Peptide, Disulfidbrücke, Membranstörung, Antibiotikaresistenz