Clear Sky Science · pt
Extremidade C não estruturada, ligada por dissulfeto, em peptídeos antimicrobianos α‑helicoidais de helmintos aumenta e modula sua atividade
Por que moléculas minúsculas de parasitas importam
À medida que a resistência a antibióticos aumenta, os pesquisadores procuram novas formas de eliminar bactérias perigosas sem ferir nossas próprias células. Uma fonte promissora são os peptídeos antimicrobianos — fragmentos curtos de proteínas que muitos organismos usam como antibióticos naturais. Este estudo examina um peptídeo incomum de um verme parasita e mostra como uma pequena cauda flexível em uma das extremidades, presa por uma ligação química, pode ajustar com precisão a rapidez e a intensidade com que o peptídeo mata bactérias. Entender esse “botão de controle” embutido pode ajudar cientistas a projetar alternativas a antibióticos mais inteligentes e precisas.
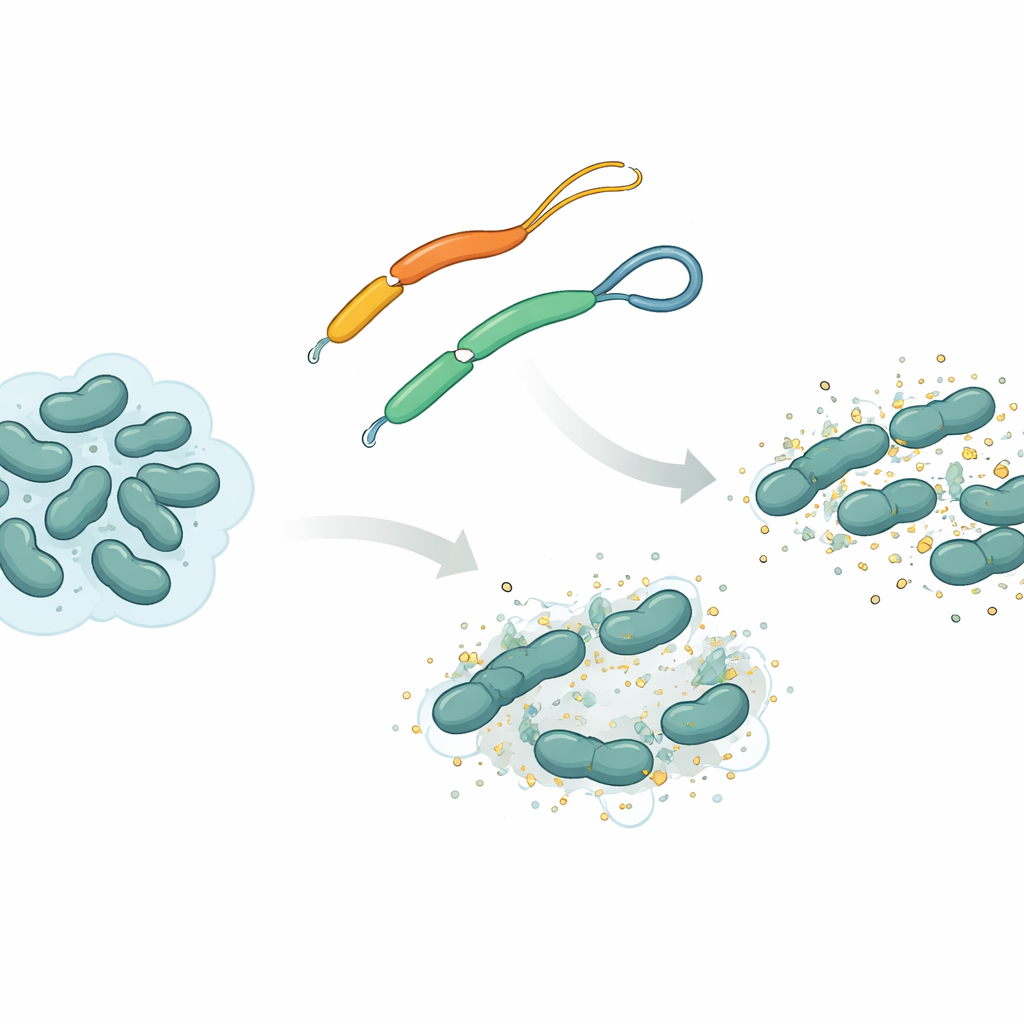
Uma arma natural de platelmintos
A equipe concentrou‑se em um peptídeo antimicrobiano chamado mesco‑2, encontrado no platelminto Mesocestoides corti. Como muitos desses peptídeos, o mesco‑2 tem uma seção “frontal” rígida em forma de espiral que interage com membranas bacterianas, além de uma “cauda” mais solta na parte posterior. Nessa cauda, dois blocos construtores que contêm enxofre estão ligados por um laço químico conhecido como ponte dissulfeto, formando um pequeno anel. Os pesquisadores compararam o mesco‑2 com uma versão quase idêntica, mesco‑2A, na qual essa ponte foi removida para que a cauda ficasse totalmente aberta. Essa pequena mudança não altera muito a composição química geral, mas modifica a mobilidade do peptídeo e seu comportamento ao atacar bactérias.
Padrões ocultos nas defesas de parasitas
Antes de focalizar o mesco‑2 em si, os cientistas vasculharam grandes bancos de dados de peptídeos antimicrobianos previstos de platelmintos e de muitos outros organismos. Procuraram por padrões específicos onde duas unidades contendo enxofre (cisteínas) são separadas por alguns outros blocos construtores perto da extremidade da molécula. Encontraram que o padrão "CXXXC" — o mesmo espaçamento do mesco‑2 — é surpreendentemente comum em peptídeos de platelmintos e frequentemente aparece em segmentos finais flexíveis, em vez de em regiões bem ordenadas. Modelos 3D gerados por computador de vários desses peptídeos mostraram que esses motivos ricos em cisteína costumam estar em caudas soltas, sugerindo que a natureza posiciona deliberadamente esses laços em regiões móveis que podem modular o comportamento do peptídeo.
Como um pequeno laço molda movimento e cooperação
Usando simulações de dinâmica molecular, os pesquisadores modelaram como mesco‑2 e mesco‑2A se movem perto de uma membrana bacteriana simplificada. Ambas as versões se prendem rapidamente à superfície da membrana, impulsionadas por forças atrativas entre cargas positivas no peptídeo e cargas negativas nos lipídios bacterianos. Mas a cauda laçada do mesco‑2 ajuda a região espiral central a dobrar em um ponto específico e a adotar uma orientação que favorece a inserção parcial na membrana. Também incentiva vários peptídeos mesco‑2 a se reunirem em pequenos aglomerados, especialmente quando suas caudas começam próximas, e essas assembleias permanecem unidas enquanto se ligam à membrana. Em contraste, o mesco‑2A de cauda aberta é mais flexível estruturalmente na extremidade, não se agrega tão facilmente e tende a ficar mais na superfície como moléculas individuais, em vez de atuar de forma coordenada.
Da estrutura à morte bacteriana
Experimentos de laboratório confirmaram os modelos computacionais. Quando os peptídeos foram misturados com miméticas simples de membrana, ambos mudaram de forma em ambientes oleosos ou semelhantes a detergente, como esperado para moléculas direcionadas à membrana. Contudo, o mesco‑2 adquiriu estrutura helicoidal regular com mais facilidade e adotou uma conformação diferente da mesco‑2A em membranas carregadas negativamente, semelhantes às bacterianas. Em testes contra várias espécies bacterianas, ambos os peptídeos demonstraram forte efeito antibacteriano com potência geral semelhante. As diferenças importantes surgiram abaixo da dose totalmente letal. O mesco‑2 retardou ou interrompeu o crescimento bacteriano por muitas horas mesmo em níveis baixos, enquanto bactérias expostas ao mesco‑2A de cauda aberta se recuperaram mais cedo. Medições temporais do dano à membrana mostraram que o mesco‑2 perfura as membranas bacterianas muito mais rapidamente, enquanto o mesco‑2A age mais devagar, a menos que seja usado em doses maiores. Imagens de alta resolução revelaram padrões distintos de dano superficial, novamente sugerindo maneiras diferentes pelas quais as duas versões perturbam o envelope bacteriano. Crucialmente, ambos os peptídeos causaram pouco dano a modelos de células imunes humanas em níveis bactericidas, indicando uma margem de segurança favorável.
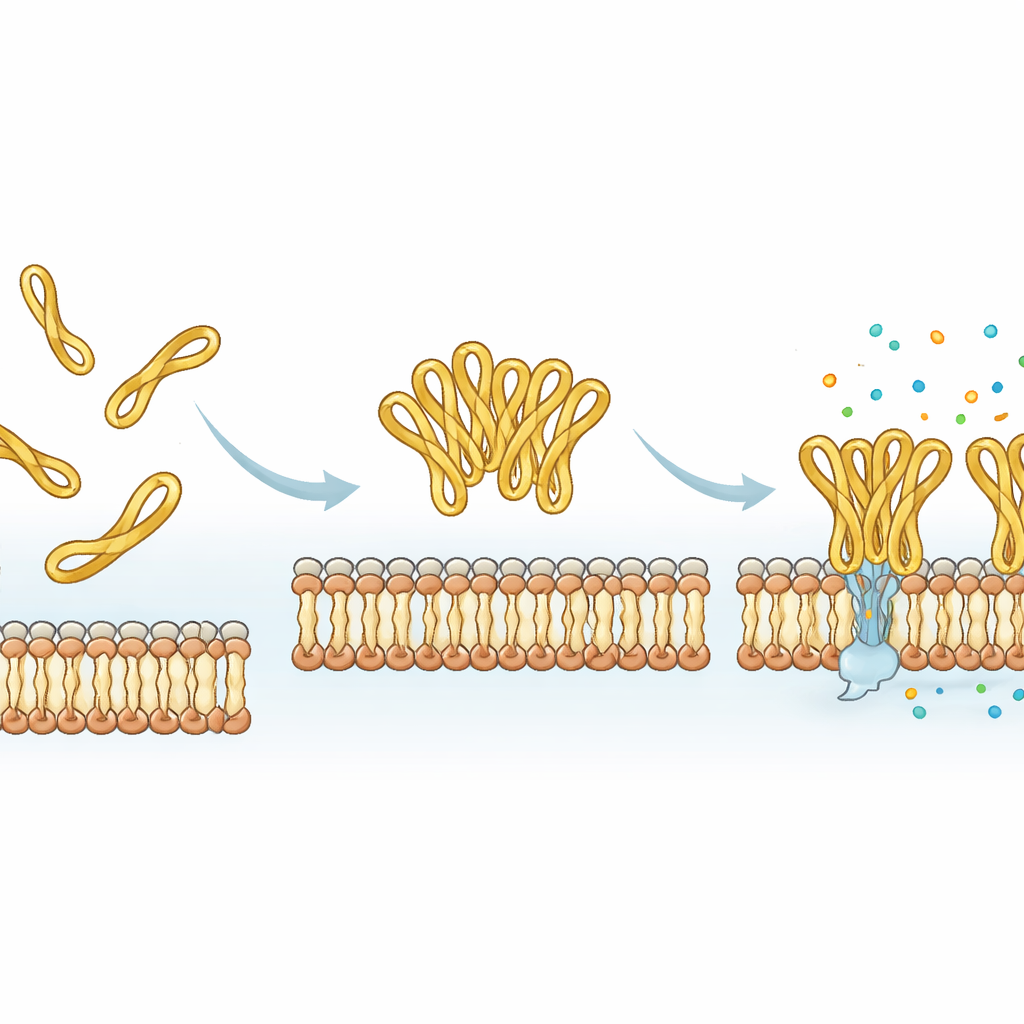
Um botão embutido para ajustar fármacos peptídicos
Reunindo todas as evidências, o estudo mostra que a pequena cauda presa por dissulfeto na extremidade do mesco‑2 atua como um ajuste molecular: estabiliza uma conformação dobrada particular, incentiva os peptídeos a trabalharem de forma cooperativa em aglomerados e acelera a ruptura da membrana, tudo isso sem aumentar muito o dano às células humanas. Remover o laço facilita a síntese e pode até aumentar quantas moléculas aderem a uma membrana modelo, mas retarda o processo de morte efetiva e altera a forma como a membrana é danificada. Para futuros fármacos do tipo antibiótico baseados em tais peptídeos, isso significa que segmentos finais aparentemente menores e flexíveis — e não apenas o núcleo helicoidal principal — podem ser deliberadamente ajustados para controlar a rapidez, a intensidade e a cooperação com que um peptídeo ataca bactérias.
Citação: Budimir, A., Stojan, I., Primorac, K. et al. Unstructured, disulfide-bridged C-terminus in helminth α-helical antimicrobial peptides enhances and modulates their activity. Sci Rep 16, 14472 (2026). https://doi.org/10.1038/s41598-026-44795-9
Palavras-chave: peptídeos antimicrobianos, peptídeos de platelmintos, ponte dissulfeto, ruptura de membrana, resistência a antibióticos