Clear Sky Science · nl
Ongeordende, door disulfidebrug verbonden C-terminus in helmint α-helix antimicrobiële peptiden versterkt en moduleert hun werking
Waarom piepkleine parasietmoleculen ertoe doen
Naarmate antibioticaresistentie toeneemt, zoeken onderzoekers naar nieuwe manieren om gevaarlijke bacteriën te doden zonder onze eigen cellen te beschadigen. Een veelbelovende bron zijn antimicrobiële peptiden — korte eiwitfragmenten die veel organismen als natuurlijke antibiotica gebruiken. Deze studie onderzoekt een ongewone peptide uit een parasitaire platworm en laat zien hoe een kleine, losse staart aan één uiteinde, verbonden door een chemische binding, de snelheid en de intensiteit waarmee de peptide bacteriën doodt kan bijsturen. Begrijpen hoe deze ingebouwde regelaar werkt kan onderzoekers helpen slimmer en nauwkeuriger antibioticumalternatieven te ontwerpen.
Een natuurlijk wapen van platwormen
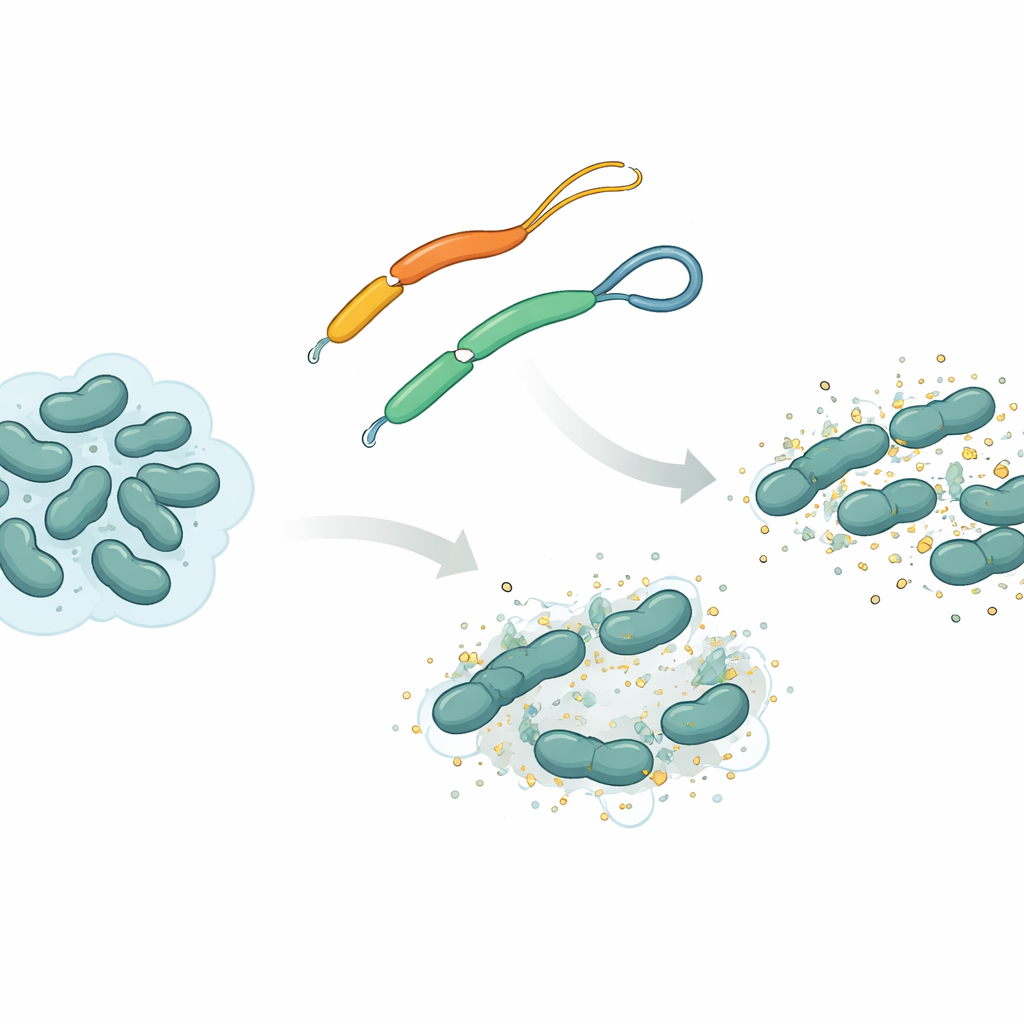
Het team richtte zich op een antimicrobiële peptide genaamd mesco‑2, gevonden in de platworm Mesocestoides corti. Net als veel van dit soort peptiden heeft mesco‑2 een stijver, spiraalvormig “voorste” gedeelte dat met bacteriële membranen interacteert, en een lossere “staart” aan de achterkant. In die staart zijn twee zwavelhoudende bouwstenen met elkaar verbonden door een chemische schakel die bekendstaat als een disulfidebrug, waardoor een klein lusje ontstaat. De onderzoekers vergeleken mesco‑2 met een vrijwel identieke versie, mesco‑2A, waarin die brug is verwijderd zodat de staart volledig openligt. Deze kleine wijziging verandert de algehele samenstelling niet veel, maar beïnvloedt hoe de peptide kan bewegen en hoe ze zich gedraagt tijdens het aanvallen van bacteriën.
Verborgen patronen in parasitaire afweer
Voordat ze mesco‑2 zelf nader bekeken, doorzochten de wetenschappers grote databanken met voorspelde antimicrobiële peptiden van platwormen en vele andere organismen. Ze zochten naar specifieke patronen waarbij twee zwavelhoudende eenheden (cysteïnes) gescheiden zijn door een paar andere bouwstenen dicht bij het uiteinde van het molecuul. Ze vonden dat een "CXXXC"-patroon — dezelfde afstand als in mesco‑2 — verrassend vaak voorkomt in platwormpeptiden en vaak in flexibele eindsegmenten zit in plaats van in goed geordende regio’s. Computergestuurde 3D-modellen van meerdere dergelijke peptiden toonden dat deze cysteïnerijke motieven doorgaans in losse staarten liggen, wat suggereert dat de natuur deze lusjes doelbewust in beweeglijke regio’s plaatst die kunnen moduleren hoe het peptide zich gedraagt.
Hoe een klein lusje beweging en samenwerking vormt
Met moleculaire dynamicasimulaties modelleerden de onderzoekers hoe mesco‑2 en mesco‑2A bewegen nabij een vereenvoudigd bacterieel membraan. Beide versies hechten zich snel aan het membraanoppervlak, gedreven door aantrekkingskrachten tussen positieve ladingen op het peptide en negatieve ladingen op de bacteriële lipiden. Maar de geluste staart in mesco‑2 helpt het centrale spiraalgedeelte bij een specifieke plek te buigen en een oriëntatie aan te nemen die gedeeltelijke insertie in het membraan bevordert. Het bevordert ook dat meerdere mesco‑2-moleculen zich verzamelen tot kleine clusters, vooral wanneer hun staarten dicht bij elkaar beginnen, en deze assemblages blijven samen terwijl ze het membraan binden. Daarentegen is het openstaartige mesco‑2A aan het uiteinde meer structureel flexibel, clustert het minder gemakkelijk en blijft het geneigd meer op het oppervlak te blijven als afzonderlijke moleculen in plaats van als een gecoördineerde groep.
Van structuur naar bacteriedoding
Laboratoriumexperimenten ondersteunden de computermodellen. Wanneer de peptiden werden gemengd met simpele membraannabootsingen, veranderden beide van vorm in vettige of detergentachtige omgevingen, zoals verwacht voor membraantargetende moleculen. Mesco‑2 ontwikkelde echter makkelijker regelmatige spiraalstructuur en nam op negatief geladen, bacterieachtige membranen een andere conformatie aan dan mesco‑2A. In tests tegen meerdere bacteriesoorten toonden beide peptiden sterke antibacteriële effecten bij vergelijkbare algehele werkzaamheid. De belangrijke verschillen verschenen onder de volledig dodelijke concentratie. Mesco‑2 vertraagde of stopte de bacteriële groei urenlang zelfs bij lage concentraties, terwijl bacteriën die aan het openstaartige mesco‑2A werden blootgesteld eerder herstelden. Tijdsgedifferentieerde metingen van membraanschade toonden dat mesco‑2 veel sneller gaten in bacteriële membranen slaat, terwijl mesco‑2A langzamer werkt tenzij in hogere doses toegepast. Hoge-resolutie beeldvorming liet distincte patronen van oppervlaktebeschadiging zien, wat opnieuw wijst op verschillende manieren waarop de twee versies de bacteriële omsluiting verstoren. Cruciaal was dat beide peptiden bij bactericide niveaus weinig schade aan modellen van menselijke immuuncellen veroorzaakten, wat wijst op een gunstige veiligheidsmarge.
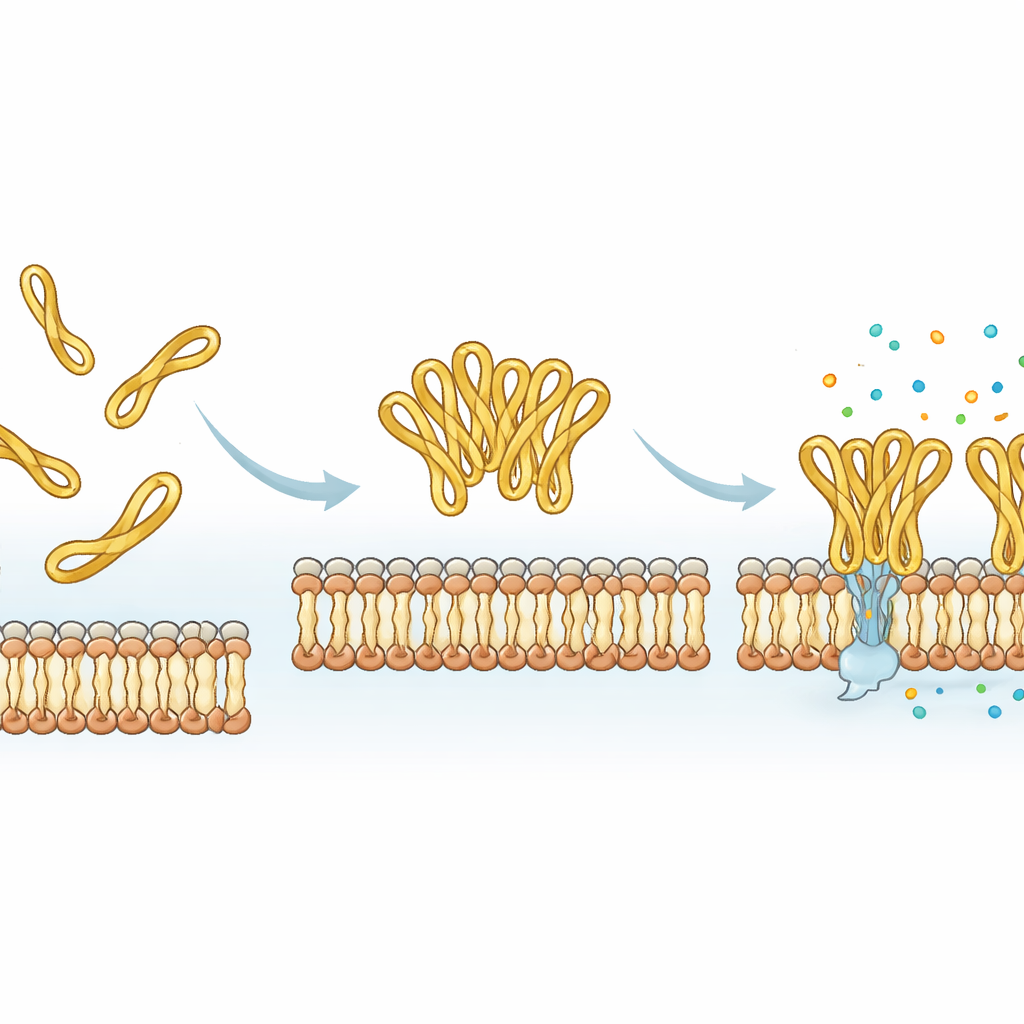
Een ingebouwde knop om peptidegeneesmiddelen af te stellen
Samengebracht laten de bevindingen zien dat de kleine, door een disulfide verbonden staart aan het einde van mesco‑2 fungeert als een moleculaire draaiknop: hij stabiliseert een specifieke gebogen vorm, stimuleert dat peptiden cooperatief als clusters werken, en versnelt membraanstoring, allemaal zonder de schade aan menselijke cellen sterk te vergroten. Het verwijderen van het lusje maakt de synthese eenvoudiger en kan zelfs verhogen hoeveel moleculen aan een modelmembraan hechten, maar vertraagt het daadwerkelijke doodmaakproces en verandert hoe het membraan beschadigd wordt. Voor toekomstige antibiotica-achtige geneesmiddelen gebaseerd op zulke peptiden betekent dit dat ogenschijnlijk kleine, flexibele eindsegmenten — in plaats van alleen de hoofdspiraalcore — doelbewust kunnen worden aangepast om te regelen hoe snel, hoe sterk en hoe cooperatief een peptide bacteriën aanvalt.
Bronvermelding: Budimir, A., Stojan, I., Primorac, K. et al. Unstructured, disulfide-bridged C-terminus in helminth α-helical antimicrobial peptides enhances and modulates their activity. Sci Rep 16, 14472 (2026). https://doi.org/10.1038/s41598-026-44795-9
Trefwoorden: antimicrobiële peptiden, plathelm peptide, disulfidebrug, membraanstoring, antibioticaresistentie