Clear Sky Science · pl
Niestrukturalny, mostkowany disiarczkowo C-koniec w helmintowych peptydach antybakteryjnych o strukturze α-helisy wzmacnia i moduluje ich aktywność
Dlaczego drobne cząsteczki pasożytów mają znaczenie
W miarę wzrostu oporności na antybiotyki naukowcy poszukują nowych sposobów zabijania groźnych bakterii bez szkody dla naszych własnych komórek. Obiecującym źródłem są peptydy antybakteryjne — krótkie fragmenty białek, których wiele organizmów używa jako naturalnych antybiotyków. W tym badaniu przeanalizowano nietypowy peptyd z pasożytniczego płazińca i pokazano, jak mały, miękki ogonek na jednym końcu, związany za pomocą chemicznego wiązania, może precyzować szybkość i siłę działania peptydu wobec bakterii. Zrozumienie tego wbudowanego „pokrętła” może pomóc naukowcom w zaprojektowaniu mądrzejszych, bardziej precyzyjnych alternatyw dla antybiotyków.
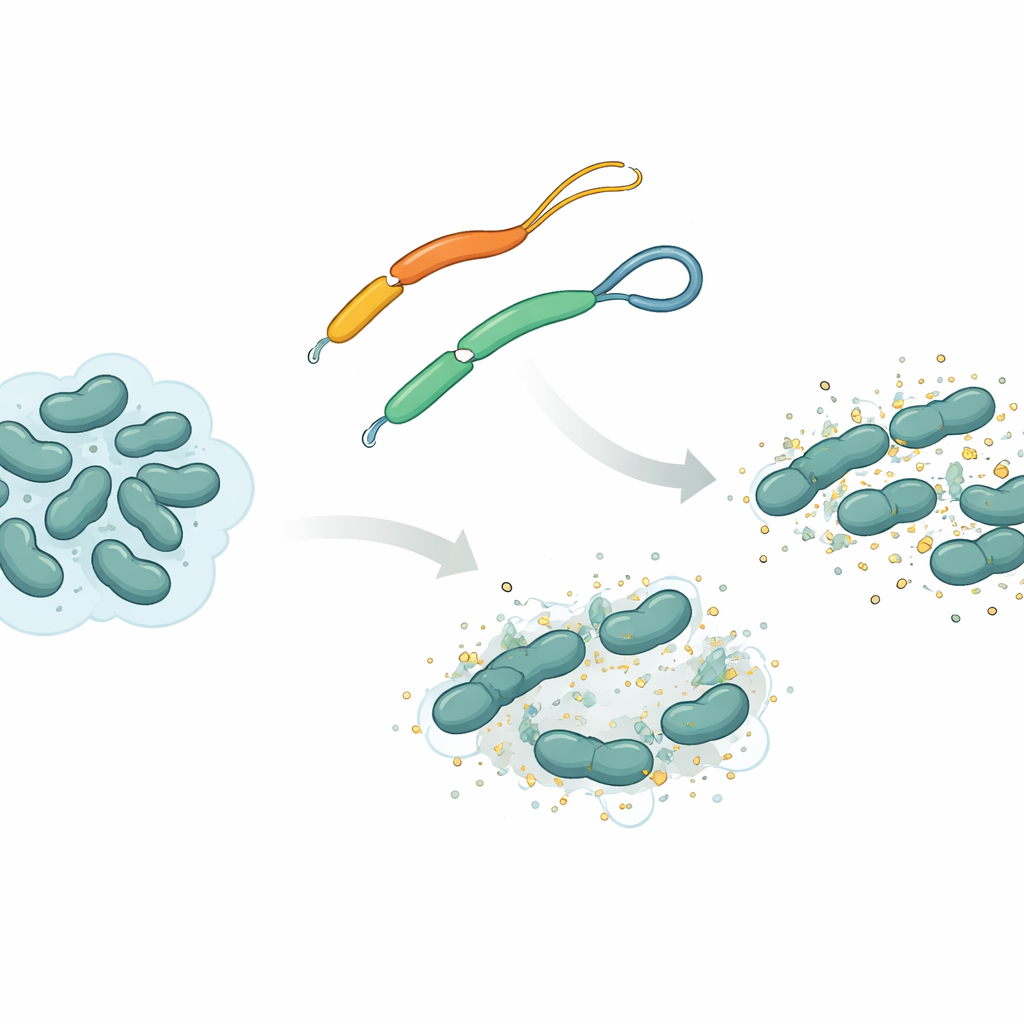
Naturalna broń od płazińców
Zespół skupił się na peptydzie antybakteryjnym nazwanym mesco‑2, odkrytym w płazińcu Mesocestoides corti. Jak wiele takich peptydów, mesco‑2 ma sztywniejszą, spiralną „przednią” część, która oddziałuje z błonami bakterii, oraz luźniejszy „ogon” na końcu. W tym ogonie dwa zawierające siarkę składniki są połączone chemicznym wiązaniem zwanym mostkiem disiarczkowym, tworząc małą pętlę. Badacze porównali mesco‑2 z niemal identyczną wersją, mesco‑2A, w której ten mostek jest usunięty i ogon jest całkowicie otwarty. Ta niewielka zmiana nie zmienia znacznie ogólnego składu chemicznego, ale wpływa na ruchliwość peptydu i jego zachowanie podczas ataku na bakterie.
Ukryte wzorce w obronie pasożytów
Zanim przyjrzeli się samemu mesco‑2, naukowcy przeszukali duże bazy przewidywanych peptydów antybakteryjnych z płazińców i wielu innych organizmów. Szukali specyficznych wzorców, w których dwa reszty zawierające siarkę (cysteiny) są rozdzielone kilkoma innymi resztami blisko końca cząsteczki. Odkryli, że wzorzec „CXXXC” — ta sama odległość co w mesco‑2 — jest zaskakująco powszechny w peptydach płazińców i często występuje w elastycznych segmentach końcowych, a nie w dobrze uporządkowanych regionach. Generowane komputerowo modele 3D kilku takich peptydów pokazały, że motywy bogate w cysteiny zwykle zlokalizowane są w giętkich ogonkach, co sugeruje, że natura celowo umieszcza te pętle w ruchomych regionach, które mogą modulować zachowanie peptydu.
Jak mała pętla kształtuje ruch i współpracę
Wykorzystując symulacje dynamiki molekularnej, badacze modelowali ruch mesco‑2 i mesco‑2A w pobliżu uproszczonej błony bakteryjnej. Obie wersje szybko przyczepiają się do powierzchni błony, napędzane siłami przyciągania między dodatnio naładowanymi miejscami peptydu a ujemnymi ładunkami lipidów bakteryjnych. Jednak związkowany mostkiem ogon w mesco‑2 pomaga centralnemu spiralnemu odcinkowi zgiąć się w konkretnym miejscu i przyjąć orientację sprzyjającą częściowemu wnikaniu w błonę. Dodatkowo sprzyja zbieraniu się kilku cząsteczek mesco‑2 w małe skupiska, zwłaszcza gdy ich ogony zaczynają blisko siebie, a te zespoły pozostają razem podczas wiązania z błoną. W przeciwieństwie do tego otwarty ogon mesco‑2A jest bardziej elastyczny na końcu, rzadziej tworzy skupiska i ma tendencję do pozostawania bardziej na powierzchni jako pojedyncze cząsteczki zamiast działać jako skoordynowana grupa.
Od struktury do zabijania bakterii
Doświadczenia laboratoryjne potwierdziły wyniki modeli komputerowych. Gdy peptydy zmieszano z prostymi imitacjami błon, obie zmieniały kształt w środowiskach oleistych lub detergentopodobnych, co jest oczekiwane dla cząsteczek celujących w błony. Jednak mesco‑2 łatwiej nabierało regularnej struktury spiralnej i przyjmowało inny kształt niż mesco‑2A na ujemnie naładowanych, bakterio‑podobnych błonach. W testach przeciw kilku gatunkom bakterii oba peptydy wykazały silne działanie antybakteryjne o podobnej ogólnej sile. Istotne różnice pojawiały się poniżej dawki całkowicie zabijającej. Mesco‑2 hamowało lub zatrzymywało wzrost bakterii przez wiele godzin nawet przy niskich stężeniach, podczas gdy bakterie wystawione na działanie otwarto‑ogonowego mesco‑2A wracały do wzrostu szybciej. Pomiary czasowo‑rozdzielcze uszkodzenia błony wykazały, że mesco‑2 przebija otwory w błonach bakterii znacznie szybciej, podczas gdy mesco‑2A działa wolniej, chyba że stosowany jest w wyższych dawkach. Obrazowanie o wysokiej rozdzielczości ujawniło różne wzorce uszkodzeń powierzchni, ponownie sugerując odmienne sposoby naruszania osłon bakteryjnych przez obie wersje. Co istotne, oba peptydy wykazały niskie uszkodzenia modeli komórek odpornościowych człowieka przy poziomach bakteriobójczych, co sugeruje korzystny margines bezpieczeństwa.
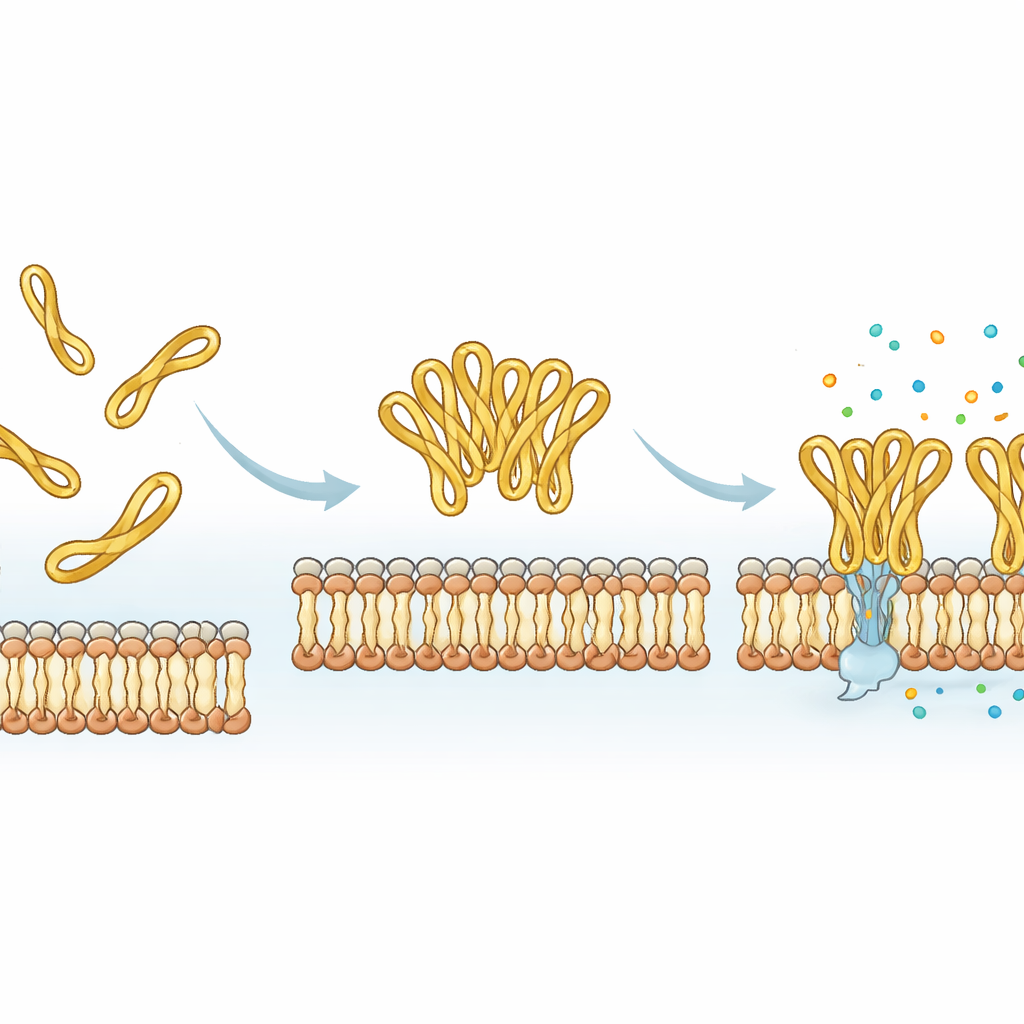
Wbudowane pokrętło do strojenia leków peptydowych
Sumując dowody, badanie pokazuje, że mały, dysiarczkowo związany ogon na końcu mesco‑2 działa jak molekularne pokrętło: stabilizuje określony zgięty kształt, sprzyja współpracy peptydów w formie skupisk i przyspiesza uszkadzanie błony, wszystko to bez znaczącego zwiększenia szkodliwości dla komórek ludzkich. Usunięcie pętli ułatwia syntezę i może nawet zwiększyć liczbę cząsteczek przylegających do modelowej błony, ale spowalnia rzeczywisty proces zabijania i zmienia sposób uszkodzenia błony. Dla przyszłych leków typu antybiotyk opartego na takich peptydach oznacza to, że pozornie drobne, elastyczne segmenty końcowe — a nie tylko główne spiralne jądro — można celowo modyfikować, aby kontrolować szybkość, siłę i wspólne działanie peptydu wobec bakterii.
Cytowanie: Budimir, A., Stojan, I., Primorac, K. et al. Unstructured, disulfide-bridged C-terminus in helminth α-helical antimicrobial peptides enhances and modulates their activity. Sci Rep 16, 14472 (2026). https://doi.org/10.1038/s41598-026-44795-9
Słowa kluczowe: peptydy antybakteryjne, peptydy płazińców, mostek disiarczkowy, uszkodzenie błony, oporność na antybiotyki