Clear Sky Science · fr
Une extrémité C non structurée, bridée par un pont disulfure, chez des peptides antimicrobiens α-héliques d’helminthes améliore et module leur activité
Pourquoi de minuscules molécules parasitaires comptent
Alors que la résistance aux antibiotiques augmente, les chercheurs recherchent de nouvelles façons d’éliminer les bactéries dangereuses sans nuire à nos propres cellules. Une source prometteuse est constituée par les peptides antimicrobiens — de courts fragments protéiques que de nombreux organismes utilisent comme antibiotiques naturels. Cette étude se penche sur un peptide inhabituel issu d’un ver parasite et montre comment une petite queue souple à une extrémité, réunie par une liaison chimique, peut régler la vitesse et l’intensité avec lesquelles le peptide tue les bactéries. Comprendre ce bouton de réglage intégré pourrait aider les scientifiques à concevoir des alternatives antibiotiques plus intelligentes et plus précises.
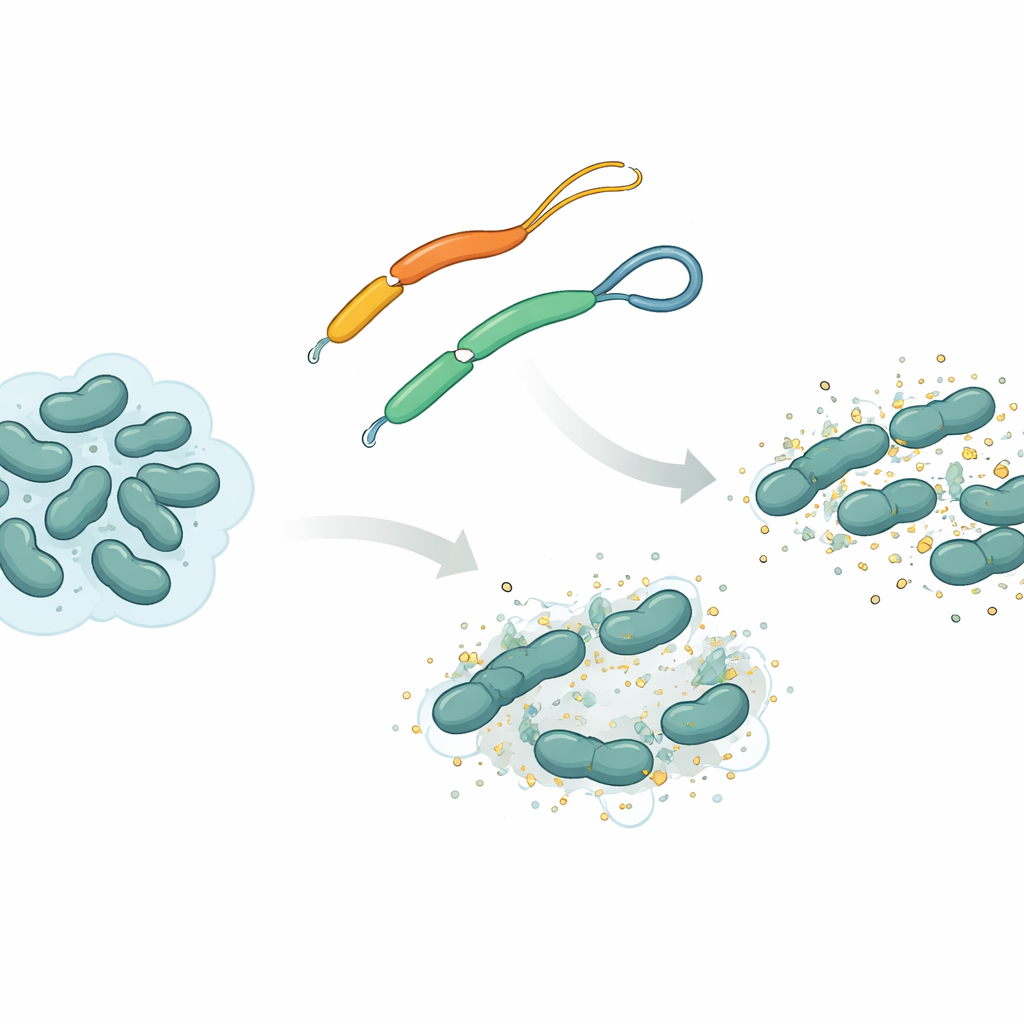
Une arme naturelle venue des plathelminthes
L’équipe s’est concentrée sur un peptide antimicrobien appelé mesco-2, trouvé chez le plathelminthe Mesocestoides corti. Comme beaucoup de ces peptides, mesco-2 possède une section « avant » rigide en forme d’hélice qui interagit avec les membranes bactériennes, ainsi qu’une « queue » plus lâche à l’arrière. Dans cette queue, deux éléments contenant du soufre sont reliés par une liaison chimique connue sous le nom de pont disulfure, formant une petite boucle. Les chercheurs ont comparé mesco-2 à une version presque identique, mesco-2A, dans laquelle ce pont est supprimé, de sorte que la queue est complètement ouverte. Ce petit changement n’altère pas beaucoup la composition chimique globale, mais modifie la mobilité du peptide et son comportement lors de l’attaque des bactéries.
Motifs cachés dans les défenses des parasites
Avant de se concentrer sur mesco-2 lui-même, les scientifiques ont exploré de larges bases de données de peptides antimicrobiens prédits chez les plathelminthes et chez de nombreux autres organismes. Ils ont recherché des motifs spécifiques où deux unités contenant du soufre (cystéines) sont séparées par quelques autres résidus près de l’extrémité de la molécule. Ils ont constaté qu’un motif « CXXXC » — le même espacement que dans mesco-2 — est étonnamment courant chez les peptides de plathelminthes et se situe souvent dans des segments terminaux flexibles plutôt que dans des régions bien ordonnées. Des modèles 3D générés par ordinateur de plusieurs de ces peptides ont montré que ces motifs riches en cystéines se trouvent généralement dans des queues souples, ce qui suggère que la nature place délibérément ces boucles dans des régions mobiles susceptibles de moduler le comportement du peptide.
Comment une minuscule boucle façonne le mouvement et la coopération
À l’aide de simulations de dynamique moléculaire, les chercheurs ont modélisé la façon dont mesco-2 et mesco-2A se déplacent près d’une membrane bactérienne simplifiée. Les deux versions adhèrent rapidement à la surface membranaire, entraînées par des forces d’attraction entre les charges positives du peptide et les lipides négatifs bactériens. Mais la queue bouclée de mesco-2 aide la région hélicoïdale centrale à se plier à un point précis et à adopter une orientation qui favorise une insertion partielle dans la membrane. Elle favorise aussi l’agrégation de plusieurs molécules de mesco-2 en petits amas, en particulier lorsque leurs queues commencent proches les unes des autres, et ces assemblages restent cohésifs pendant la liaison à la membrane. En revanche, la mesco-2A à queue ouverte est plus flexible à son extrémité, s’agrège moins facilement et a tendance à rester davantage en surface comme molécules individuelles plutôt qu’en groupes coordonnés.
De la structure à l’élimination bactérienne
Les expériences en laboratoire ont confirmé les modèles informatiques. Lorsque les peptides ont été mélangés à des mimétiques membranaires simples, les deux ont changé de conformation en environnements huileux ou détergents, comme attendu pour des molécules ciblant les membranes. Cependant, mesco-2 a adopté plus facilement une structure hélicoïdale régulière et a pris une conformation différente de mesco-2A sur des membranes chargées négativement, semblables à celles des bactéries. Dans des tests contre plusieurs espèces bactériennes, les deux peptides ont montré de forts effets antibactériens à une puissance globale comparable. Les différences importantes sont apparues en dessous de la dose létale complète. Mesco-2 a ralenti ou stoppé la croissance bactérienne pendant de nombreuses heures, même à faibles niveaux, tandis que les bactéries exposées à la mesco-2A à queue ouverte se sont rétablies plus tôt. Des mesures temporelles des dommages membranaires ont montré que mesco-2 perce des trous dans les membranes bactériennes beaucoup plus rapidement, alors que mesco-2A agit plus lentement sauf à des doses plus élevées. L’imagerie à haute résolution a révélé des schémas distincts de dommages en surface, suggérant à nouveau des modes différents d’altération de l’enveloppe bactérienne. Fait crucial, les deux peptides ont montré peu d’effets délétères sur des modèles de cellules immunitaires humaines à des niveaux bactéricides, suggérant une marge de sécurité favorable.
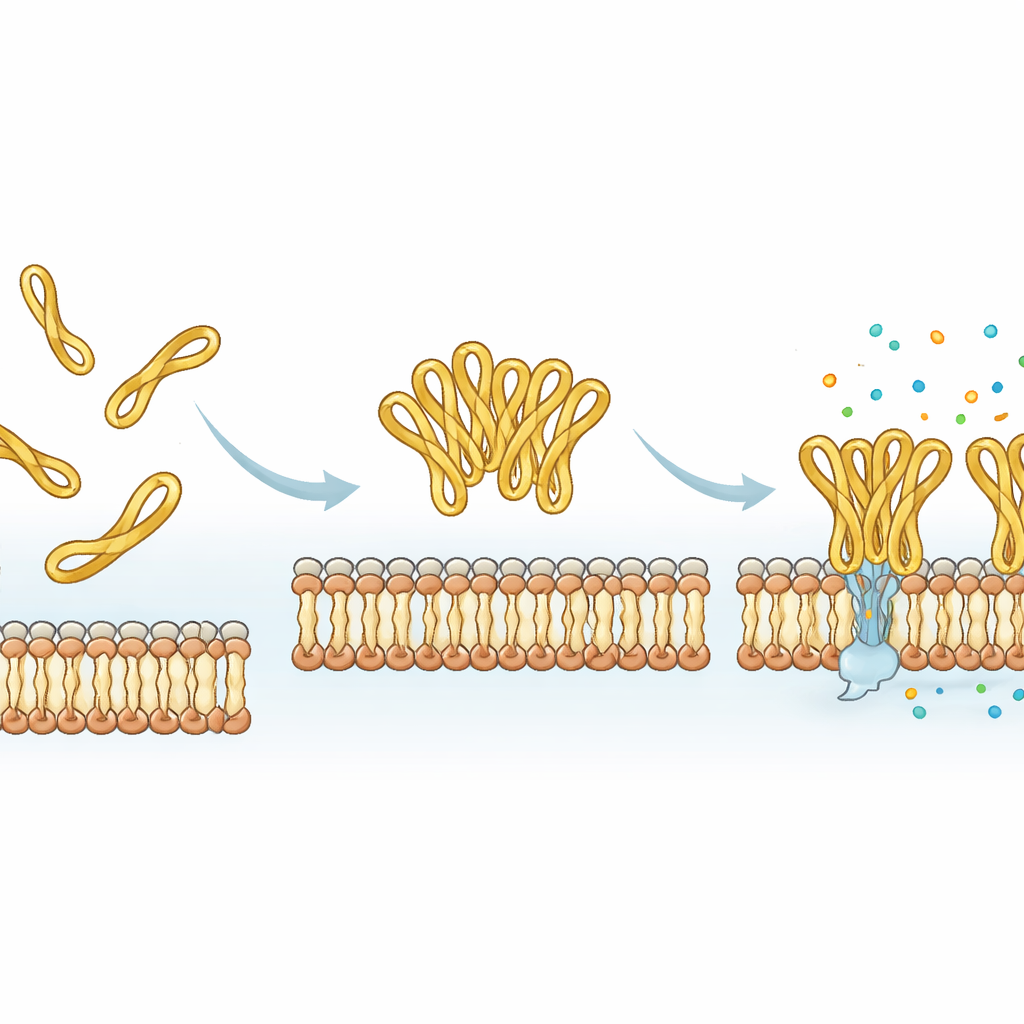
Un cadran intégré pour régler les médicaments peptidiques
En rassemblant toutes les preuves, l’étude montre que la petite queue bridée par un disulfure à l’extrémité de mesco-2 agit comme un cadran moléculaire : elle stabilise une conformation pliée particulière, encourage la coopération des peptides sous forme de clusters et accélère la perturbation membranaire, le tout sans augmenter fortement la toxicité pour les cellules humaines. Retirer la boucle facilite la synthèse et peut même accroître le nombre de molécules adhérant à une membrane modèle, mais ralentit le processus de mise à mort effectif et modifie la façon dont la membrane est endommagée. Pour de futurs médicaments de type antibiotique basés sur de tels peptides, cela signifie que des segments terminaux apparemment mineurs et flexibles — plutôt que seulement le noyau hélicoïdal principal — peuvent être délibérément ajustés pour contrôler la vitesse, l’intensité et la coopération avec lesquelles un peptide attaque les bactéries.
Citation: Budimir, A., Stojan, I., Primorac, K. et al. Unstructured, disulfide-bridged C-terminus in helminth α-helical antimicrobial peptides enhances and modulates their activity. Sci Rep 16, 14472 (2026). https://doi.org/10.1038/s41598-026-44795-9
Mots-clés: peptides antimicrobiens, peptides de plathelminthes, pont disulfure, perturbation membranaire, résistance aux antibiotiques