Clear Sky Science · zh
Numb通过PLK1依赖通路减轻放射线诱导的肠上皮细胞衰老
为什么放疗会损伤肠道
放射治疗对许多癌症是救命的,但对肠道可能非常有害。肠道内衬更新速度很快,因此对放射线特别敏感。当这层内衬受损时,原本将细菌和毒素限制在肠腔内、阻止进入血液的屏障会开始渗漏。本研究探讨了一种较少为人所知的蛋白Numb如何帮助保护肠道屏障免受放射损伤,以及另一种蛋白伙伴PLK1在这种保护中扮演的角色。理解这种相互关系可能为更温和的癌症治疗指明方向,减少长期消化道副作用。
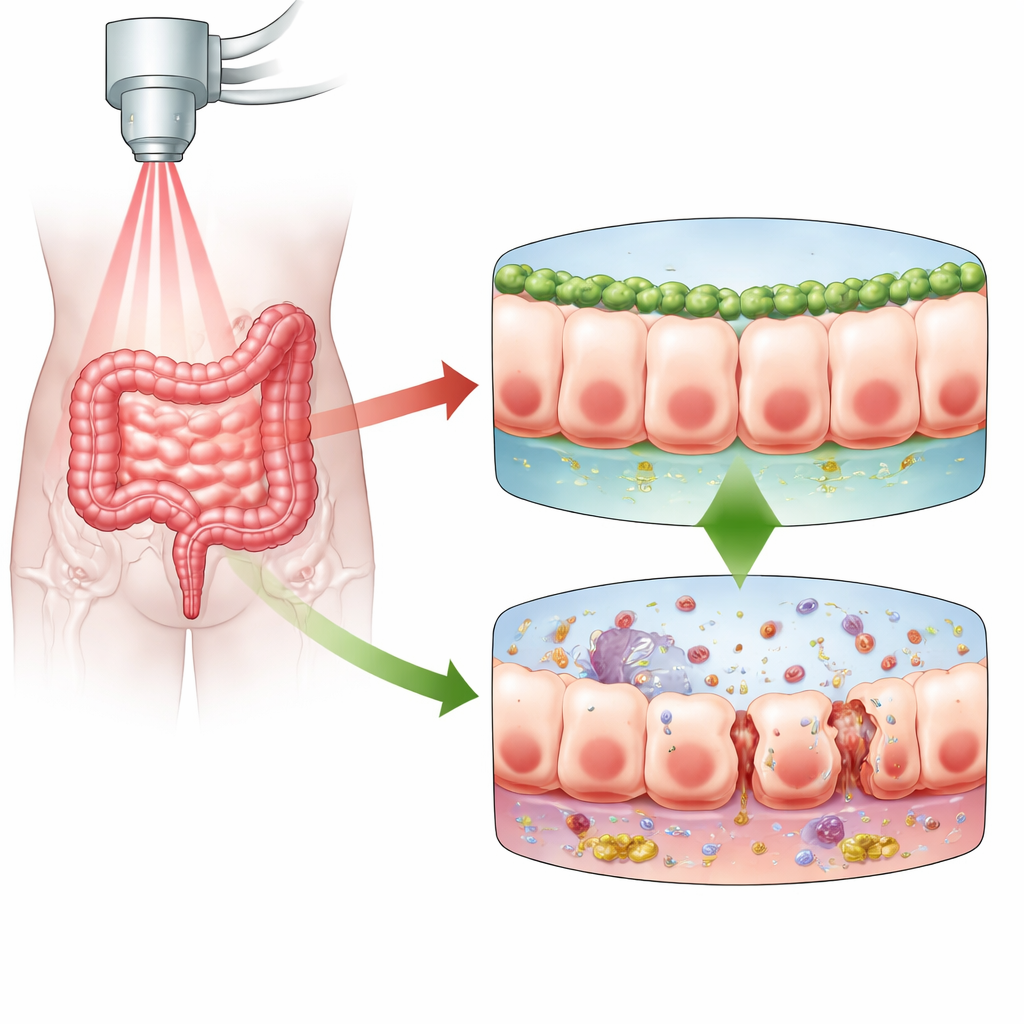
受攻击的肠道保护壁垒
肠黏膜屏障由一层紧密排列的细胞构成,将肠内内容物与机体其他部分分隔开。放射线照射这层屏障会损伤细胞内的DNA。细胞会以不同方式应对:死亡、暂停以修复自身,或进入一种称为衰老的状态——它们停止分裂但仍然存活,且常表现出高度炎症性。作者聚焦于放射性肠炎,这是骨盆放疗后常见的疼痛性且有时致残的并发症。他们怀疑已知参与维持细胞极性、黏附和修复的Numb蛋白,可能影响肠上皮细胞对放射线的反应,以及屏障是保持紧密还是变得渗漏。
关键蛋白沉默时损伤加重
为测试Numb的作用,研究者在小鼠肠道上皮中降低了Numb水平,然后对腹部进行放射照射。缺乏Numb的小鼠结果更糟:死亡率更高、体重下降更明显,血液中肠道通透性指标更高。显微镜观察显示,本应整齐连续的细胞间连接被破坏,覆盖和保护表面的黏液层变薄且不连续。同时,肠组织中的炎症分子显著上升,容纳干细胞并驱动肠道更新的微小隐窝数量减少且损伤更严重。这些变化共同描绘出一个无法有效自我修复或将有害物质限制在肠内的屏障。
细胞过早衰老
进一步分析时,研究组考察了上皮细胞内部的变化。他们发现,在Numb下降的情况下,放射诱发的DNA损伤信号更持久,细胞衰老标志明显上升。更多细胞呈现出典型的衰老形态并对标准的衰老酶染色呈阳性,但整体凋亡——即细胞直接死亡——并未增加。在培养的人结肠细胞系中,去除Numb并未使细胞在放射后更多死亡,但确实促使许多细胞在细胞周期中,尤其是分裂前阶段,进入长期停滞。这些停滞的细胞积累损伤和衰老标志,并开始分泌更高水平的炎性因子,即所谓衰老相关分泌表型,这可进一步削弱组织并促进慢性炎症。
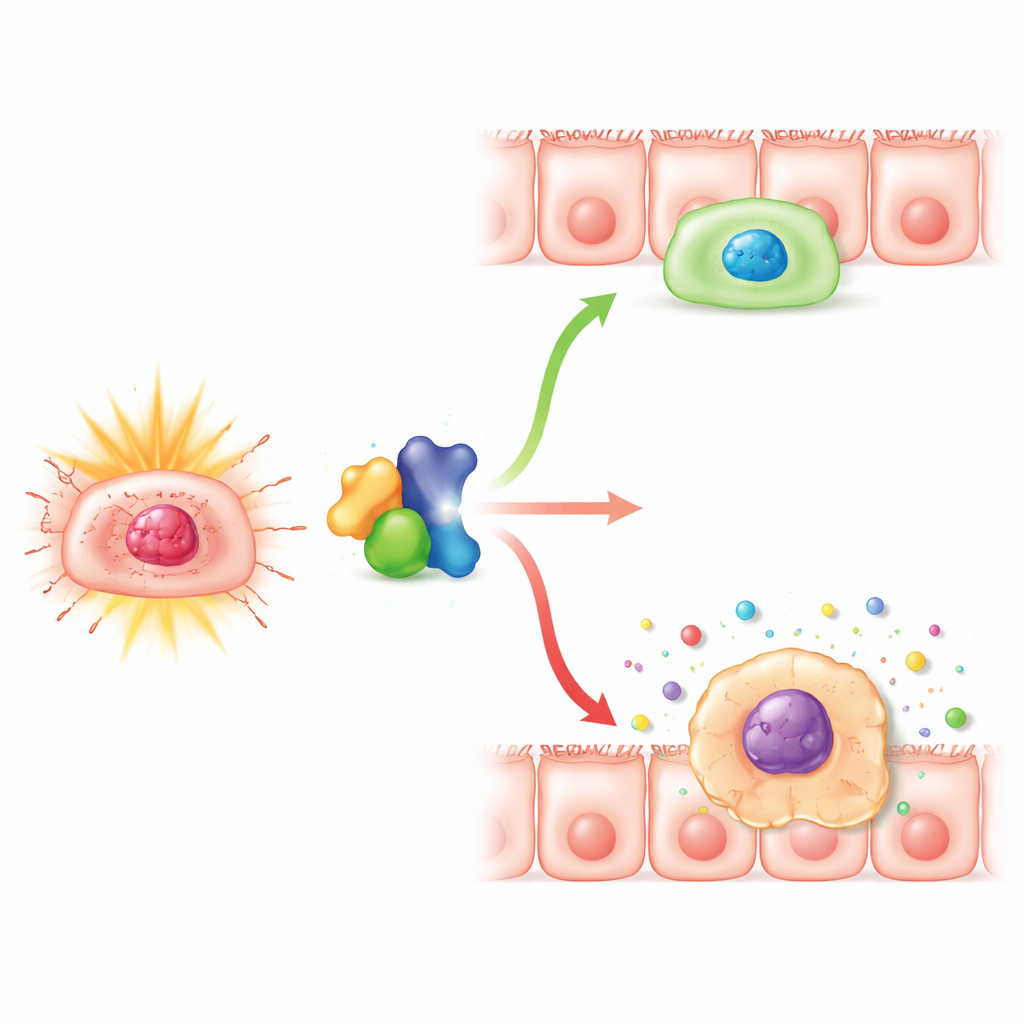
倾斜平衡的分子伙伴
研究者随后转向PLK1,这是一种帮助细胞完成分裂最后步骤并在应激后从检查点暂停中恢复的蛋白。早期工作提示Numb与PLK1存在相互作用。该研究证实二者在肠上皮细胞中有物理结合,并且降低Numb也会使PLK1水平下降。单独抑制PLK1会使放射处理的细胞更易进入衰老,而提高PLK1水平则能部分挽救因Numb缺失导致的衰老和生长停滞。过表达PLK1降低了衰老标志,恢复了细胞生长,减少了停滞在分裂前的细胞比例,并抑制了炎性分子的释放。这些发现表明,Numb有助于维持PLK1的活性,使细胞能够修复损伤并重新进入细胞周期,而不是滑向永久的、促炎的停滞状态。
对患者意味着什么
该研究提出,Numb通过PLK1作为肠道在放射暴露期间的守护者,通过限制肠上皮细胞的过早衰老来维护肠道屏障。与其单纯防止细胞死亡,这一路径似乎更倾向于引导受损细胞走向修复和有控制的恢复,减少会破坏屏障的衰老促炎细胞堆积。尽管许多细节仍需在活体动物和人类患者中进一步验证,这项工作将Numb–PLK1轴指向了作为保护放疗期间肠道的有前景的治疗靶点——有望使医生在保留有效癌症剂量的同时,减少患者的慢性肠道问题。
引用: Yang, Y., Hu, X., Pan, Y. et al. Numb mitigates intestinal epithelial cell senescence induced by radiation through a PLK1-dependent pathway. Sci Rep 16, 10876 (2026). https://doi.org/10.1038/s41598-026-44793-x
关键词: 放射性肠炎, 肠道屏障, 细胞衰老, Numb蛋白, PLK1