Clear Sky Science · it
Il Numb attenua la senescenza delle cellule epiteliali intestinali indotta dalle radiazioni attraverso una via dipendente da PLK1
Perché le radiazioni possono danneggiare l’intestino
La radioterapia è un trattamento salvavita per molti tumori, ma può essere particolarmente aggressiva per l’intestino. L’epitelio intestinale si rinnova rapidamente, caratteristica che lo rende molto sensibile alle radiazioni. Quando questo rivestimento viene danneggiato, la barriera che normalmente impedisce a batteri e tossine di passare nell’organismo inizia a diventare permeabile. Questo studio indaga come una proteina poco conosciuta, chiamata Numb, contribuisca a proteggere la barriera intestinale dal danno da radiazioni, e quale ruolo svolga il suo partner PLK1 in questa protezione. Comprendere questa relazione potrebbe indirizzare verso trattamenti oncologici più delicati, con meno effetti digestivi cronici.
La parete protettiva dell’intestino sotto attacco
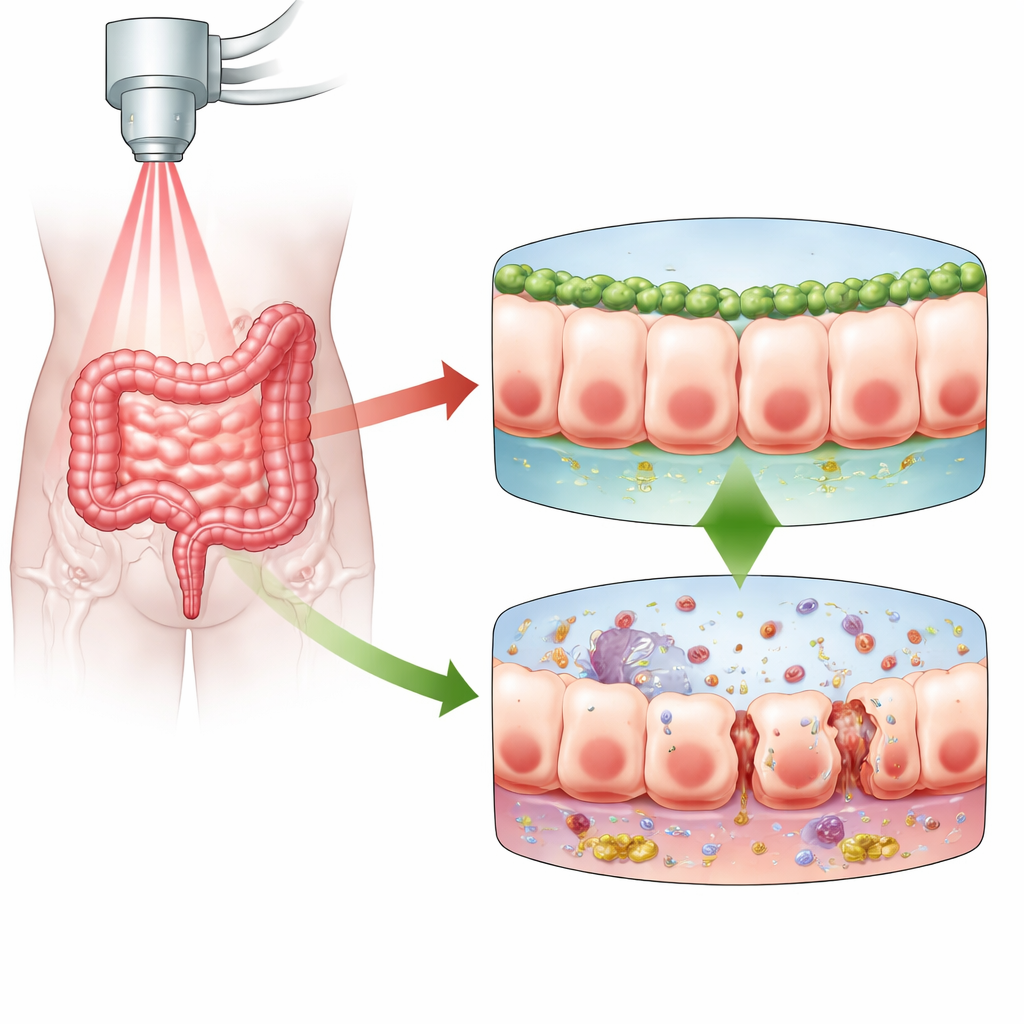
La barriera mucosale intestinale è un foglio singolo e strettamente coeso di cellule che separa il contenuto intestinale dal resto dell’organismo. Quando le radiazioni colpiscono questa barriera, danneggiano il DNA delle cellule. In risposta, le cellule possono morire, arrestarsi per ripararsi o entrare in uno stato chiamato senescenza, in cui smettono di dividersi ma restano vive e spesso diventano altamente infiammatorie. Gli autori si sono concentrati sull’enterite da radiazioni, una complicanza dolorosa e talvolta invalidante della radioterapia pelvica. Hanno ipotizzato che Numb, una proteina già nota per mantenere la polarità cellulare, l’adesione e la riparazione dell’epitelio, potesse influenzare la risposta delle cellule intestinali alle radiazioni e determinare se la barriera resti ermetica o diventi permeabile.
Una proteina chiave peggiora il danno se viene silenziata
Per verificare il ruolo di Numb, i ricercatori hanno usato topi riducendo i livelli di Numb nell’epitelio intestinale prima di esporli a radiazioni addominali. I topi privi di Numb in queste cellule hanno avuto esiti molto peggiori: un tasso di mortalità maggiore, perdita di peso più marcata e indici di permeabilità intestinale nel sangue più elevati. La microscopia ha mostrato che le giunzioni normalmente ordinate e continue tra cellule vicine risultavano interrotte e lo strato di muco protettivo si è assottigliato e presentava lesioni. Contemporaneamente sono aumentate nettamente le molecole infiammatorie nel tessuto intestinale e le piccole cripte che ospitano le cellule staminali e guidano il rinnovamento intestinale risultavano meno numerose e più danneggiate. Nel loro insieme, questi cambiamenti descrivono una barriera incapace di ripararsi efficacemente o di confinare i contenuti nocivi all’interno dell’intestino.
Quando le cellule invecchiano troppo presto
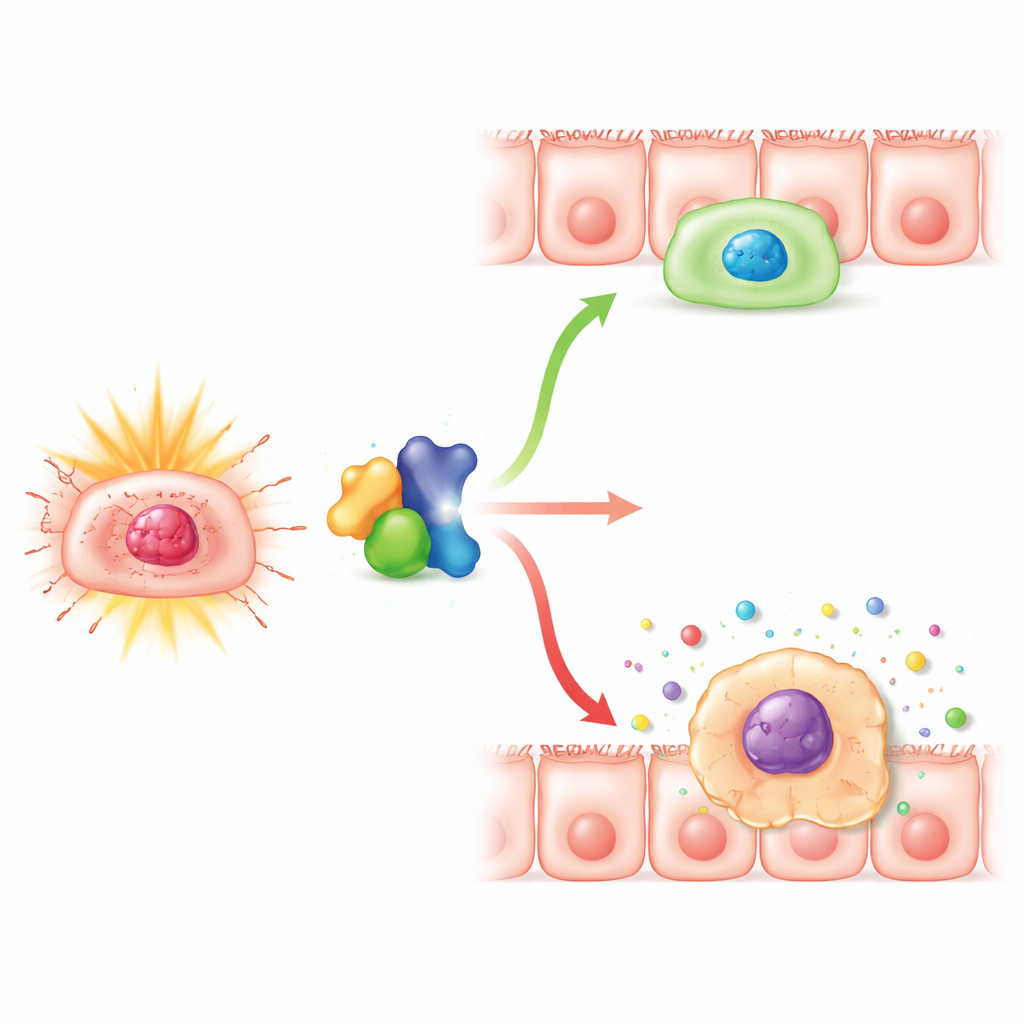
Approfondendo, il gruppo ha esaminato cosa accadeva all’interno delle cellule epiteliali. Hanno riscontrato che, con Numb ridotto, le radiazioni provocavano segnali di danno al DNA più persistenti e un forte aumento dei marcatori della senescenza cellulare. Più cellule assumevano l’aspetto tipico della senescenza e risultavano positive a colorazioni enzimatiche standard per la senescenza, mentre l’apoptosi generale — la morte cellulare netta — non aumentava. In linee cellulari coliche umane in coltura, la rimozione di Numb non aumentava la morte cellulare dopo radiazione, ma induceva molte cellule a un arresto prolungato del ciclo cellulare, specialmente nella fase immediatamente precedente la divisione. Queste cellule bloccate accumulavano danni e marcatori di senescenza e cominciavano a secernere livelli più elevati di fattori infiammatori, la cosiddetta fenotipo secretorio associato alla senescenza, che può indebolire ulteriormente il tessuto e alimentare un’infiammazione cronica.
Un partner molecolare che fa pendere la bilancia
I ricercatori si sono poi concentrati su PLK1, una proteina che aiuta le cellule a completare gli ultimi passaggi della divisione e a riprendersi dalle pause del checkpoint dopo uno stress. Studi precedenti avevano suggerito che Numb e PLK1 interagiscono. Qui il gruppo ha confermato che le due proteine si associano fisicamente nelle cellule intestinali e che la riduzione di Numb abbassa anche i livelli di PLK1. Inibire PLK1 da solo rendeva le cellule trattate con radiazioni più soggette alla senescenza, mentre aumentare PLK1 poteva in parte recuperare lo stato di arresto e senescenza causato dalla perdita di Numb. La sovraespressione di PLK1 diminuiva i marcatori di senescenza, ripristinava la crescita cellulare, riduceva la frazione di cellule bloccate prima della divisione e attenuava il rilascio di molecole infiammatorie. Questi risultati suggeriscono che Numb contribuisca a mantenere l’attività di PLK1 a un livello che permette alle cellule di riparare i danni e rientrare nel ciclo cellulare anziché scivolare in un arresto permanente e infiammatorio.
Cosa significa per i pazienti
Lo studio propone che Numb, agendo tramite PLK1, funzioni come guardiano della barriera intestinale durante l’esposizione alle radiazioni, limitando l’invecchiamento cellulare prematuro dell’epitelio. Piuttosto che prevenire semplicemente la morte cellulare, questa via sembra indirizzare le cellule danneggiate verso la riparazione e un recupero controllato, riducendo l’accumulo di cellule senescenti e pro-infiammatorie che possono compromettere la barriera nel tempo. Pur restando molti dettagli da chiarire, specialmente negli animali vivi e nei pazienti umani, il lavoro indica l’asse Numb–PLK1 come un promettente bersaglio per terapie mirate a proteggere l’intestino durante la radioterapia — potenzialmente consentendo di erogare dosi efficaci contro il tumore risparmiando i pazienti da problemi intestinali cronici.
Citazione: Yang, Y., Hu, X., Pan, Y. et al. Numb mitigates intestinal epithelial cell senescence induced by radiation through a PLK1-dependent pathway. Sci Rep 16, 10876 (2026). https://doi.org/10.1038/s41598-026-44793-x
Parole chiave: enterite da radiazioni, barriera intestinale, senescenza cellulare, proteina Numb, PLK1