Clear Sky Science · sv
Numb mildrar strålningsinducerad senescens i tarmens epitelceller via en PLK1‑beroende väg
Varför strålning kan skada tarmen
Strålbehandling räddar liv vid många cancerformer, men den kan vara hård mot tarmen. Tarmens slemhinna förnyas snabbt vilket gör den särskilt känslig för strålning. När slemhinnan skadas börjar barriären som normalt håller bakterier och toxiner kvar i tarmen läcka mot blodomloppet. Denna studie undersöker hur ett relativt okänt protein kallat Numb bidrar till att skydda tarmbarriären mot strålskador, och hur en annan proteinpartner, PLK1, ingår i det skyddet. Att förstå detta samspel kan peka mot skonsammare cancerbehandlingar med färre långsiktiga matsmältningsbesvär. 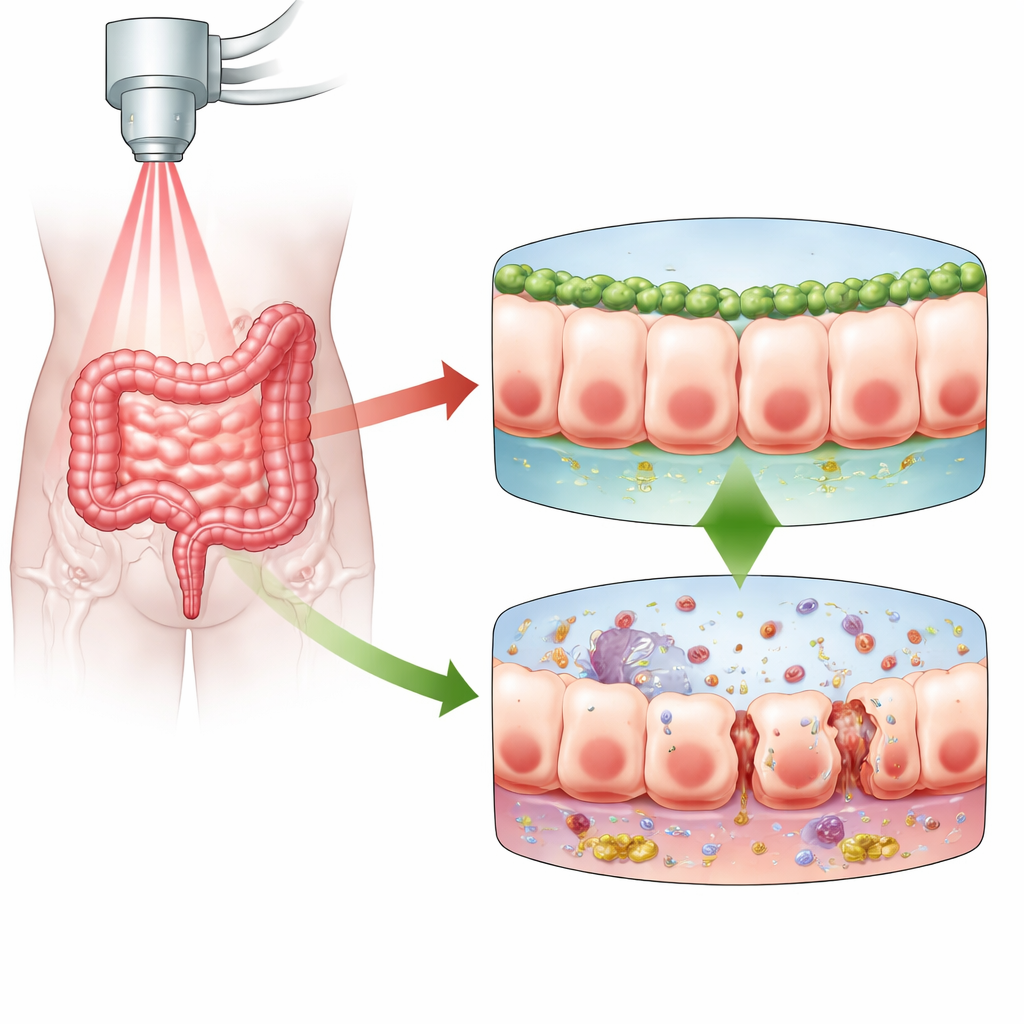
Tarmens skyddsvägg under attack
Tarmens mukösa barriär är ett enda, tätt packat cellager som skiljer tarmens innehåll från resten av kroppen. När strålning träffar denna barriär skadas cellernas DNA. Som svar dör celler, stannar upp för att reparera sig eller går in i ett tillstånd kallat senescens, där de slutar dela sig men förblir levande och ofta blir starkt inflammatoriska. Författarna fokuserade på strålningsenterit, en smärtsam och ibland handikappande komplikation efter bäckenstrålning. De misstänkte att Numb, ett protein som redan är känt för att hjälpa till att upprätthålla cellpolarisering, vidhäftning och reparation i tarmhinnan, kan påverka hur tarmceller svarar på strålning och om barriären förblir tät eller blir läckande.
Ett nyckelprotein förvärrar skadan när det tystas
För att testa Numbs roll sänkte forskarna Numb‑nivåerna i tarmens epitel hos möss innan de utsattes för bukstrålning. Möss utan Numb i dessa celler klarade sig betydligt sämre: fler av dem dog, de tappade mer i vikt och uppmätta markörer för tarmläckage i blodet var högre. Mikroskopi visade att de normalt prydliga, kontinuerliga fogarna mellan intilliggande celler var störda och att det slemskikt som täcker och skyddar ytan blivit tunt och fläckigt. Samtidigt ökade inflammatoriska molekyler i tarmvävnaden kraftigt, och de små kryptorna som rymmer stamceller och driver tarmförnyelsen var färre och mer skadade. Tillsammans gav dessa förändringar en bild av en barriär som inte längre kunde reparera sig effektivt eller hålla skadligt innehåll inkapslat i tarmen.
När celler åldras för tidigt
Genom att gå djupare i vad som skedde inne i epitelcellerna fann teamet att vid minskad Numb ökade strålningen ihållande DNA‑skadesignaler och en kraftig uppgång i markörer för cellulär senescens. Fler celler fick det klassiska senescenta utseendet och testade positivt för ett standardfärgtest för senescens, samtidigt som total apoptos — ren celldöd — inte ökade. I odlade mänskliga koloncellinjer gjorde borttagning av Numb inte att fler celler dog efter strålning, men det satte många av dem i ett utdraget stopp i cellcykeln, särskilt i fasen precis före delning. Dessa stoppade celler ackumulerade skador och senescensmarkörer och började utsöndra högre nivåer av inflammatoriska faktorer, den så kallade senescensassocierade sekretoriska fenotypen, vilket kan försvaga vävnad ytterligare och driva kronisk inflammation. 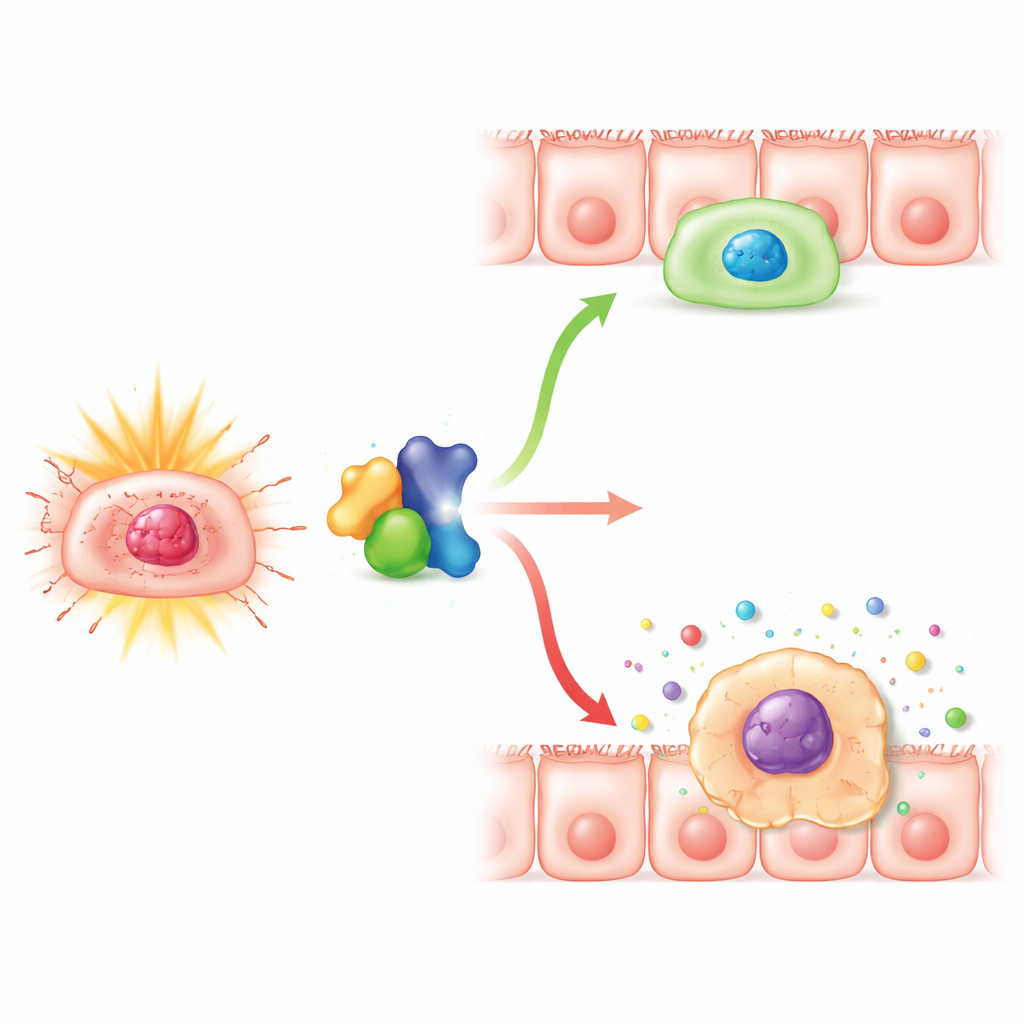
En molekylär partner som tippar balansen
Forskarna riktade därefter in sig på PLK1, ett protein som hjälper celler genom de sista stegen av delning och att återhämta sig från kontrollpunktsuppehåll efter stress. Tidigare arbete hade antytt att Numb och PLK1 interagerar. Här bekräftade teamet att de två proteinerna fysiskt associerar i tarmceller och att minskad Numb också sänkte PLK1‑nivåerna. Att hämma PLK1 ensam gjorde att strålningsbehandlade celler blev mer benägna att gå in i senescens, medan att öka PLK1 delvis kunde rädda den senescenta, tillväxthämmande tillståndet orsakat av Numb‑förlust. Överuttryck av PLK1 minskade senescensmarkörer, återställde celltillväxt, reducerade andelen celler fastnade före delning och dämpade frisättningen av inflammatoriska molekyler. Dessa fynd tyder på att Numb hjälper till att hålla PLK1‑aktiviteten på en nivå som tillåter cellerna att reparera skador och återgå till cellcykeln istället för att glida in i ett permanent, inflammatoriskt stillestånd.
Vad detta betyder för patienter
Studien föreslår att Numb, via PLK1, fungerar som en väktare av tarmbarriären under strålning genom att begränsa för tidigt cellulärt åldrande i tarmhinnan. Istället för att enbart förhindra celldöd verkar denna väg styra skadade celler mot reparation och kontrollerad återhämtning, vilket minskar uppbyggnaden av senescenta, inflammationsdrivande celler som över tid kan undergräva barriären. Även om många detaljer återstår att klarlägga, särskilt i levande djur och mänskliga patienter, pekar arbetet på Numb–PLK1‑axeln som ett lovande mål för behandlingar avsedda att skydda tarmen under radioterapi — vilket potentiellt gör det möjligt för läkare att ge effektiva cancerdoser samtidigt som patienterna skonas från kroniska tarmproblem.
Citering: Yang, Y., Hu, X., Pan, Y. et al. Numb mitigates intestinal epithelial cell senescence induced by radiation through a PLK1-dependent pathway. Sci Rep 16, 10876 (2026). https://doi.org/10.1038/s41598-026-44793-x
Nyckelord: strålningsenterit, tarmbarriär, cellulär senescens, Numb‑protein, PLK1