Clear Sky Science · pl
Numb łagodzi starzenie się komórek nabłonka jelitowego wywołane promieniowaniem poprzez szlak zależny od PLK1
Dlaczego promieniowanie może szkodzić jelitom
Terapia radiacyjna ratuje życie w wielu przypadkach nowotworów, ale może być brutalna dla jelit. Wyściółka naszych jelit odnawia się szybko, co czyni ją szczególnie wrażliwą na promieniowanie. Gdy ta warstwa zostaje uszkodzona, bariera, która normalnie zatrzymuje bakterie i toksyny wewnątrz jelita i chroni krwiobieg, zaczyna przepuszczać. W tej pracy badano, jak mało znane białko o nazwie Numb pomaga chronić barierę jelitową przed uszkodzeniem wywołanym promieniowaniem oraz jak inny partner białkowy, PLK1, wpisuje się w tę ochronę. Zrozumienie tej relacji może wskazać drogę do łagodniejszych terapii przeciwnowotworowych z mniejszymi długoterminowymi skutkami ubocznymi dla układu pokarmowego. 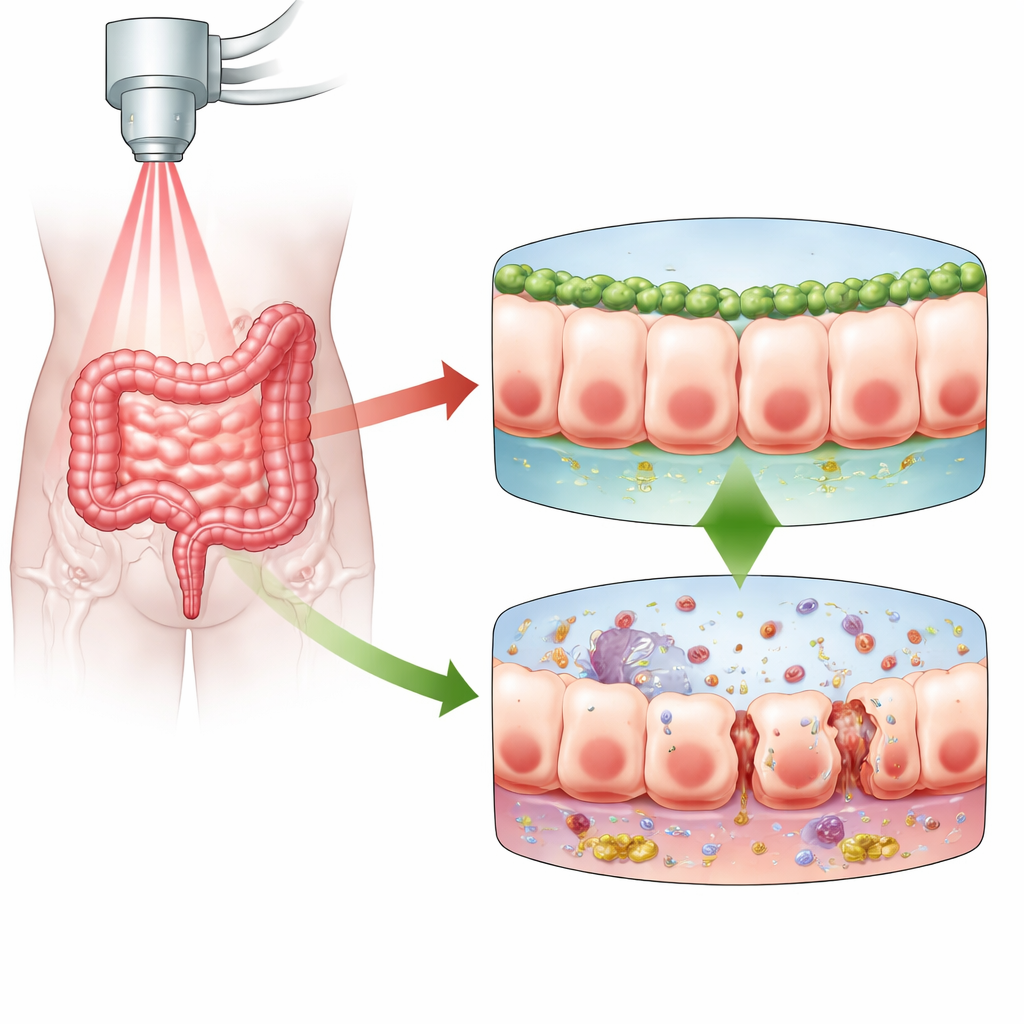
Atak na ochronną ścianę jelita
Śluzówkowa bariera jelitowa to pojedyncza, ściśle upakowana warstwa komórek, która oddziela zawartość jelita od reszty ciała. Gdy promieniowanie trafia w tę barierę, uszkadza DNA w tych komórkach. W odpowiedzi komórki albo umierają, zatrzymują się, by naprawić uszkodzenia, albo wchodzą w stan zwany starzeniem komórkowym (senescencją), w którym przestają się dzielić, pozostają przy życiu i często stają się wysoce zapalne. Autorzy skupili się na radiacyjnym zapaleniu jelit, bolesnym i czasem wyniszczającym powikłaniu radioterapii miednicy. Podejrzewali, że Numb — białko znane już z utrzymania polarności komórkowej, adhezji i naprawy w wyściółce jelitowej — może wpływać na to, jak komórki jelitowe reagują na promieniowanie i czy bariera pozostaje szczelna, czy zaczyna przeciekać.
Główne białko pogarsza uszkodzenia, gdy jest wyciszone
Aby sprawdzić rolę Numb, badacze wykorzystali myszy i zmniejszyli poziom Numb w wyściółce jelita przed napromieniowaniem jamy brzusznej. Myszy pozbawione Numb w tych komórkach radziły sobie znacznie gorzej: więcej z nich umarło, straciły więcej na wadze, a wskaźniki nieszczelności jelitowej we krwi były wyższe. Mikroskopia wykazała, że normalnie uporządkowane, ciągłe połączenia między sąsiednimi komórkami zostały zaburzone, a warstwa śluzu pokrywająca i chroniąca powierzchnię stała się cienka i nieciągła. Jednocześnie w tkance jelitowej gwałtownie wzrosły czynniki zapalne, a drobne krypty zawierające komórki macierzyste i zapewniające odnawianie jelita były nieliczne i bardziej uszkodzone. Te zmiany razem naszkicowały obraz bariery, która nie była w stanie skutecznie się naprawiać ani utrzymać szkodliwych treści wewnątrz jelita.
Kiedy komórki starzeją się zbyt wcześnie
Zagłębiając się dalej, zespół przeanalizował, co dzieje się wewnątrz samych komórek nabłonkowych. Stwierdzili, że przy zmniejszonym poziomie Numb promieniowanie wywołuje bardziej uporczywe sygnały uszkodzenia DNA i silny wzrost markerów senescencji komórkowej. Więcej komórek przyjmowało klasyczny wygląd starzejących się komórek i dawało pozytywny wynik standardowego barwienia enzymatycznego dla senescencji, podczas gdy ogólne wskaźniki apoptozy — całkowitej śmierci komórek — nie wzrosły. W hodowlach ludzkich linii komórek okrężnicy usunięcie Numb nie powodowało większej śmierci komórek po napromieniowaniu, ale skłaniało wiele z nich do przedłużonego zatrzymania w cyklu komórkowym, zwłaszcza w fazie tuż przed podziałem. Te zatrzymane komórki gromadziły uszkodzenia i markery senescencji oraz zaczęły wydzielać wyższe poziomy czynników zapalnych, tzw. zespołu wydzielniczego związanego z senescencją (SASP), które mogą dodatkowo osłabiać tkankę i napędzać przewlekłe zapalenie. 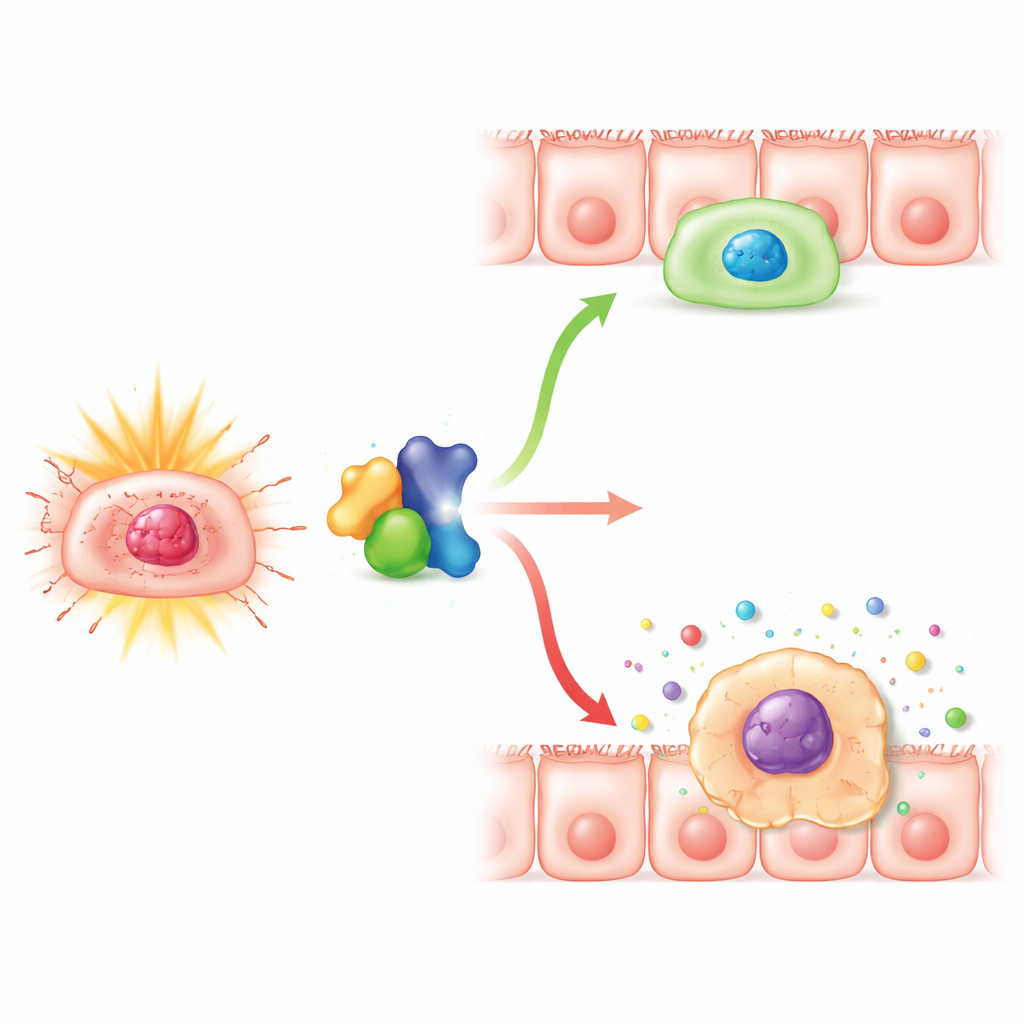
Molekularny partner, który przechyla szalę
Następnie badacze zwrócili uwagę na PLK1, białko pomagające komórkom przejść przez końcowe etapy podziału i odzyskać aktywność po zatrzymaniach kontrolnych wywołanych stresem. Wcześniejsze prace sugerowały interakcję między Numb a PLK1. Tutaj zespół potwierdził, że oba białka fizycznie współdziałają w komórkach jelitowych i że obniżenie Numb prowadzi też do spadku poziomów PLK1. Hamowanie PLK1 samo w sobie sprawiało, że komórki poddane promieniowaniu były bardziej podatne na senescencję, podczas gdy zwiększenie poziomu PLK1 częściowo odwracało senescentny, zahamowany wzrost spowodowany utratą Numb. Nadekspresja PLK1 zmniejszała markery senescencji, przywracała wzrost komórek, redukowała odsetek komórek zablokowanych przed podziałem i tłumiła uwalnianie cząsteczek zapalnych. Wyniki te sugerują, że Numb pomaga utrzymywać aktywność PLK1 na poziomie umożliwiającym komórkom naprawę uszkodzeń i powrót do cyklu podziałowego, zamiast dopuszczać do trwałego, zapalnego zatrzymania.
Co to znaczy dla pacjentów
Badanie proponuje, że Numb działający poprzez PLK1 pełni funkcję strażnika bariery jelitowej podczas ekspozycji na promieniowanie, ograniczając przedwczesne starzenie się komórek wyściółki jelitowej. Zamiast po prostu zapobiegać śmierci komórek, ten szlak zdaje się kierować uszkodzone komórki ku naprawie i kontrolowanemu powrotowi, zmniejszając akumulację senescentnych komórek napędzających zapalenie, które z czasem mogą podważać barierę. Choć wiele szczegółów wymaga dalszych badań, zwłaszcza in vivo i u pacjentów, praca wskazuje oś Numb–PLK1 jako obiecujący cel terapii mających chronić jelita podczas radioterapii — co potencjalnie pozwoli lekarzom stosować skuteczne dawki przeciwnowotworowe przy jednoczesnym zmniejszeniu ryzyka przewlekłych problemów jelitowych dla pacjentów.
Cytowanie: Yang, Y., Hu, X., Pan, Y. et al. Numb mitigates intestinal epithelial cell senescence induced by radiation through a PLK1-dependent pathway. Sci Rep 16, 10876 (2026). https://doi.org/10.1038/s41598-026-44793-x
Słowa kluczowe: radiacyjne zapalenie jelit, bariera jelitowa, starzenie komórkowe, białko Numb, PLK1