Clear Sky Science · es
Numb mitiga la senescencia de las células epiteliales intestinales inducida por radiación mediante una vía dependiente de PLK1
Por qué la radiación puede dañar el intestino
La radioterapia salva vidas en muchos cánceres, pero puede ser muy agresiva para el intestino. El revestimiento de nuestros intestinos se renueva con rapidez, lo que lo hace especialmente sensible a la radiación. Cuando este revestimiento se daña, la barrera que normalmente mantiene las bacterias y las toxinas dentro del intestino y lejos del torrente sanguíneo comienza a filtrarse. Este estudio explora cómo una proteína poco conocida llamada Numb ayuda a proteger la barrera intestinal del daño por radiación y cómo otra proteína asociada, PLK1, encaja en esa protección. Entender esta relación podría señalar vías para tratamientos contra el cáncer menos agresivos y con menos efectos digestivos crónicos.
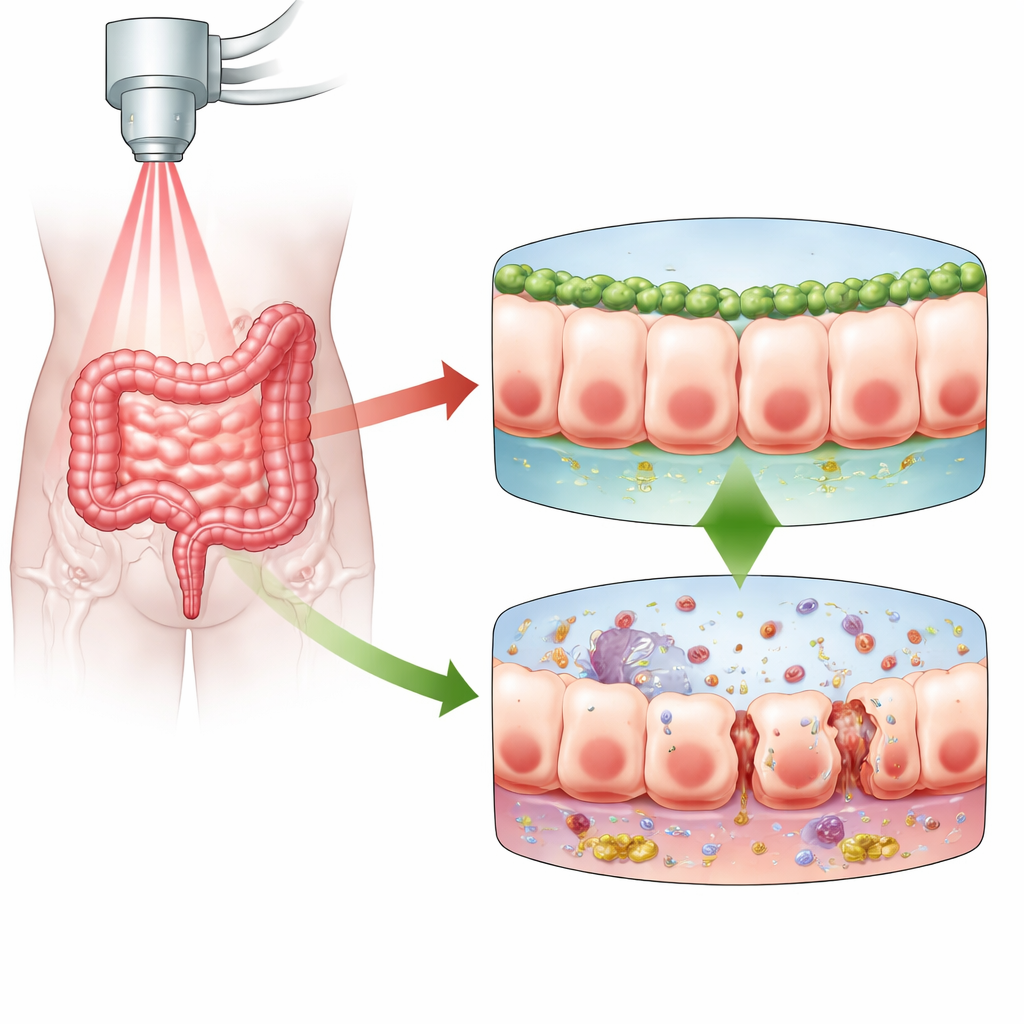
El muro protector del intestino bajo ataque
La barrera mucosa intestinal es una capa única y compacta de células que separa el contenido del intestino del resto del cuerpo. Cuando la radiación alcanza esta barrera, daña el ADN dentro de esas células. En respuesta, las células pueden morir, detenerse para repararse o entrar en un estado denominado senescencia, en el que dejan de dividirse pero permanecen vivas y a menudo se vuelven altamente inflamatorias. Los autores se centraron en la enteritis por radiación, una complicación dolorosa y a veces incapacitante de la radioterapia pélvica. Sospechaban que Numb, una proteína ya conocida por ayudar a mantener la polaridad celular, la adhesión y la reparación en el revestimiento intestinal, podría influir en cómo responden las células intestinales a la radiación y si la barrera se mantiene hermética o se vuelve permeable.
Una proteína clave empeora el daño cuando se silencia
Para probar el papel de Numb, los investigadores usaron ratones y redujeron los niveles de Numb en su revestimiento intestinal antes de exponerlos a radiación abdominal. Los ratones sin Numb en estas células tuvieron resultados mucho peores: más de ellos murieron, perdieron más peso y las mediciones de permeabilidad intestinal en sangre fueron más altas. La microscopía mostró que las uniones normalmente ordenadas y continuas entre células vecinas estaban alteradas, y la capa de moco que recubre y protege la superficie se volvió delgada y parcheada. Al mismo tiempo, las moléculas inflamatorias en el tejido intestinal aumentaron drásticamente, y las pequeñas criptas que albergan las células madre y sustentan la renovación intestinal eran menos numerosas y más dañadas. En conjunto, estos cambios dibujaron el retrato de una barrera que ya no podía repararse con eficacia ni mantener los contenidos nocivos confinados al intestino.
Cuando las células envejecen demasiado pronto
Indagando más, el equipo examinó lo que ocurría dentro de las propias células epiteliales. Encontraron que, con Numb reducido, la radiación provocó señales de daño en el ADN más persistentes y un fuerte aumento de marcadores de senescencia celular. Más células adoptaron la apariencia clásica de senescentes y dieron positivo en una tinción enzimática estándar de senescencia, sin que el nivel global de apoptosis —muerte celular franca— aumentara. En líneas celulares humanas de colon cultivadas, la eliminación de Numb no hizo que las células murieran más tras la radiación, pero sí empujó a muchas de ellas a una parada prolongada del ciclo celular, especialmente en la fase inmediatamente anterior a la división. Estas células estancadas acumularon daño y marcadores de senescencia y empezaron a secretar niveles más altos de factores inflamatorios, el llamado fenotipo secretor asociado a la senescencia, que puede debilitar aún más el tejido y alimentar la inflamación crónica.
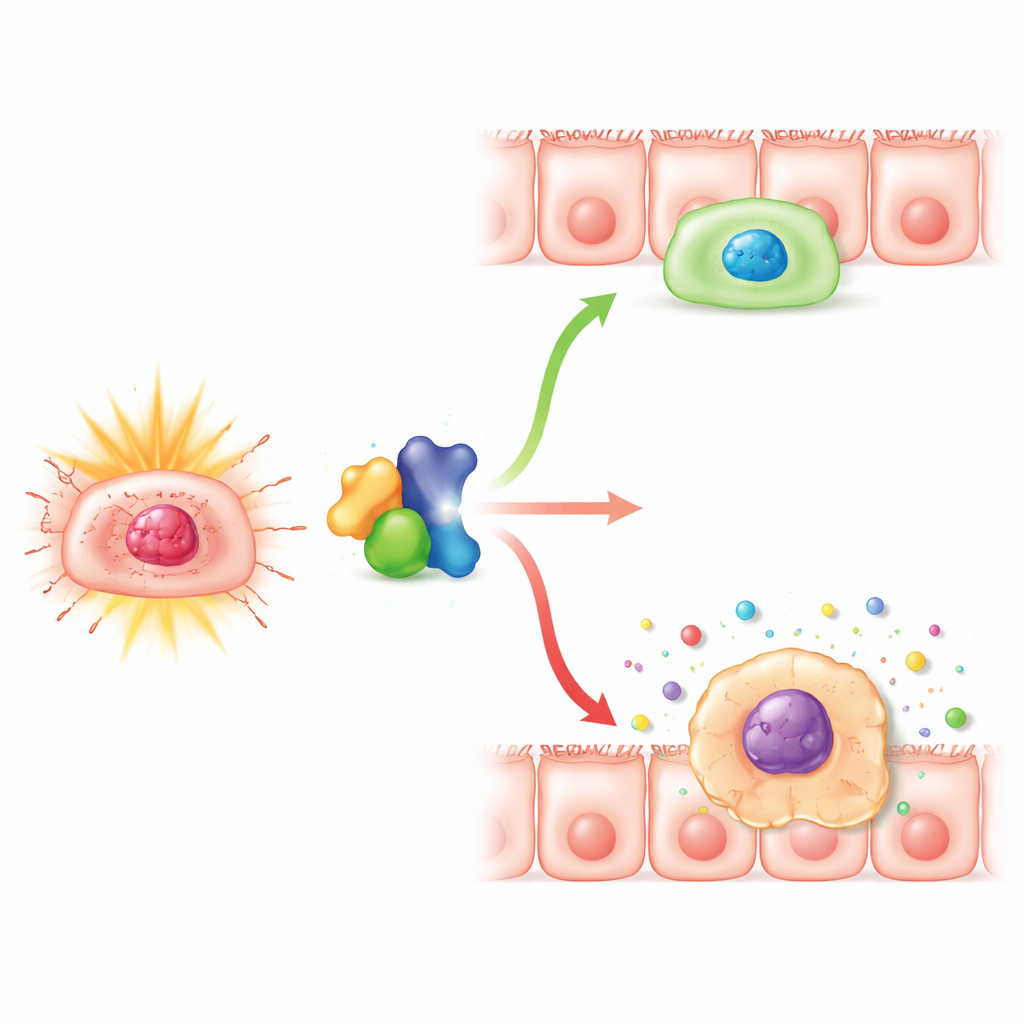
Un compañero molecular que inclina la balanza
Los investigadores se dirigieron entonces a PLK1, una proteína que ayuda a las células a completar los pasos finales de la división y a recuperarse de las pausas del control tras el estrés. Trabajos previos sugerían que Numb y PLK1 interactúan. Aquí, el equipo confirmó que las dos proteínas se asocian físicamente en las células intestinales y que la disminución de Numb también reduce los niveles de PLK1. Bloquear PLK1 por sí solo hizo que las células tratadas con radiación fueran más propensas a la senescencia, mientras que aumentar PLK1 pudo rescatar en parte el estado senescente y detenido en el crecimiento causado por la pérdida de Numb. La sobreexpresión de PLK1 disminuyó los marcadores de senescencia, restauró el crecimiento celular, redujo la fracción de células atrapadas antes de la división y atenuó la liberación de moléculas inflamatorias. Estos hallazgos sugieren que Numb ayuda a mantener la actividad de PLK1 en un nivel que permite a las células reparar el daño y reingresar al ciclo celular en lugar de deslizarse hacia un estado permanente e inflamatorio.
Qué significa esto para los pacientes
El estudio propone que Numb, actuando a través de PLK1, funciona como un guardián de la barrera intestinal durante la exposición a la radiación al limitar el envejecimiento celular prematuro en el revestimiento intestinal. En lugar de limitarse a prevenir la muerte celular, esta vía parece orientar a las células dañadas hacia la reparación y la recuperación controlada, reduciendo la acumulación de células senescentes que promueven la inflamación y que pueden socavar la barrera con el tiempo. Aunque quedan por resolver muchos detalles, sobre todo en animales vivos y pacientes humanos, el trabajo señala al eje Numb–PLK1 como un objetivo prometedor para tratamientos destinados a proteger el intestino durante la radioterapia —potencialmente permitiendo a los médicos administrar dosis efectivas contra el cáncer mientras preservan a los pacientes de problemas intestinales crónicos.
Cita: Yang, Y., Hu, X., Pan, Y. et al. Numb mitigates intestinal epithelial cell senescence induced by radiation through a PLK1-dependent pathway. Sci Rep 16, 10876 (2026). https://doi.org/10.1038/s41598-026-44793-x
Palabras clave: enteritis por radiación, barrera intestinal, senescencia celular, proteína Numb, PLK1