Clear Sky Science · nl
Numb vermindert senescentie van intestinale epitheelcellen door straling via een PLK1-afhankelijke route
Waarom straling de darmen kan beschadigen
Radiotherapie redt levens bij veel vormen van kanker, maar kan hard zijn voor de darmen. Het darmslijmvlies vernieuwt zich snel en is daardoor bijzonder gevoelig voor straling. Wanneer dit slijmvlies beschadigd raakt, begint de barrière die normaal bacteriën en toxines in de darm houdt en uit de bloedbaan houdt, te lekken. Deze studie onderzoekt hoe een weinig bekend eiwit, Numb, helpt de darmbarrière tegen stralingsschade te beschermen, en welke rol een eiwitpartner, PLK1, daarbij speelt. Inzicht in deze relatie kan de weg wijzen naar minder belastende kankerbehandelingen met minder langdurige spijsverteringsklachten.
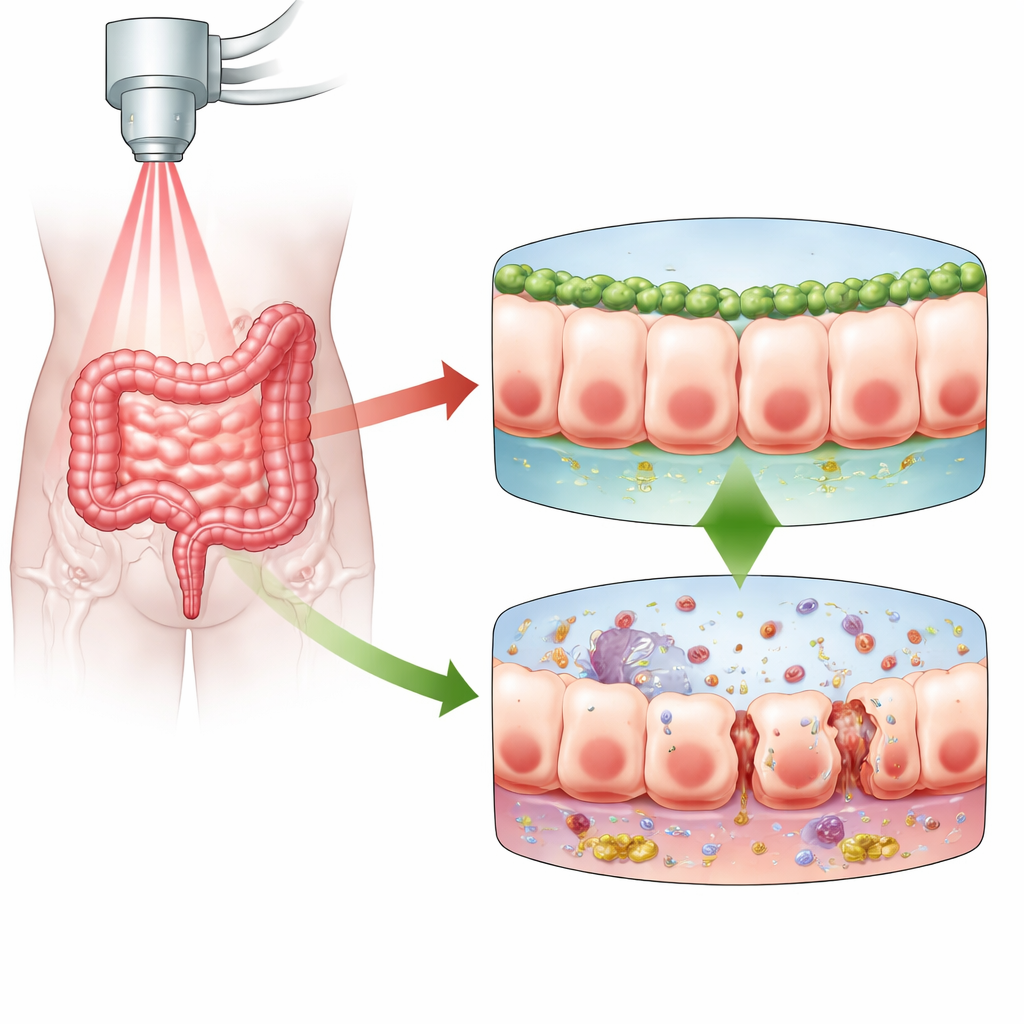
De beschermende wand van de darm onder aanval
De intestinale mucosale barrière is een enkelvoudig, strak aangesloten celblad dat de inhoud van de darm scheidt van de rest van het lichaam. Wanneer straling op deze barrière inwerkt, beschadigt het het DNA in deze cellen. Als reactie sterven cellen, pauzeren ze om zichzelf te repareren, of raken ze in een staat genaamd senescentie, waarbij ze stoppen met delen maar levend blijven en vaak sterk ontstekingsbevorderend worden. De auteurs concentreerden zich op radiation enteritis, een pijnlijke en soms invaliderende complicatie van bekkenradiotherapie. Ze vermoedden dat Numb, een eiwit dat al bekendstaat als belangrijk voor het behoud van celdeling, hechting en herstel in het darmslijmvlies, zou kunnen beïnvloeden hoe intestinale cellen op straling reageren en of de barrière dicht blijft of gaat lekken.
Een sleutel-eiwit verergert schade wanneer het wordt uitgeschakeld
Om de rol van Numb te testen, verlaagden de onderzoekers Numb-niveaus in de darmbekleding van muizen voordat ze abdominale straling kregen. Muizen zonder Numb in deze cellen deden het veel slechter: er stierven er meer, ze verloren meer gewicht en bloedmarkers voor darmlekken waren hoger. Microscopen toonden dat de normaal nette, aaneengesloten verbindingen tussen aangrenzende cellen verstoord waren en dat de slijmlaag die het oppervlak bedekt en beschermt dunner en ongelijk werd. Tegelijkertijd stegen ontstekingsmoleculen in het darmsweefsel sterk, en werden de kleine crypten die stamcellen herbergen en intestinale vernieuwing aandrijven minder talrijk en ernstiger beschadigd. Samen schetsten deze veranderingen een beeld van een barrière die niet langer efficiënt kon herstellen of schadelijke inhoud binnen de darm kon houden.
Wanneer cellen te vroeg oud worden
Dieper gravend bekeken de onderzoekers wat er binnenin de epitheelcellen gebeurde. Ze vonden dat bij verminderde Numb-straling hardnekkigere DNA-schade-signalen veroorzaakte en een scherpe toename van markers voor cellulaire senescentie. Meer cellen kregen het klassieke senescente uiterlijk en testten positief voor een standaard senescentie-enzymkleuring, terwijl algemene apoptose—rechtstreekse celdood—niet toenam. In gekweekte menselijke coloncelijnen zorgde het weghalen van Numb er niet voor dat cellen meer stierven na straling, maar duwde het veel van hen in een langdurige stilstand van de celcyclus, vooral in de fase net voor deling. Deze vastgezette cellen stapelden schade en senescentiemarkers op en begonnen hogere niveaus van ontstekingsfactoren uit te scheiden, het zogenoemde senescence-associated secretory phenotype, wat weefsel verder kan verzwakken en chronische ontsteking kan aanjagen.
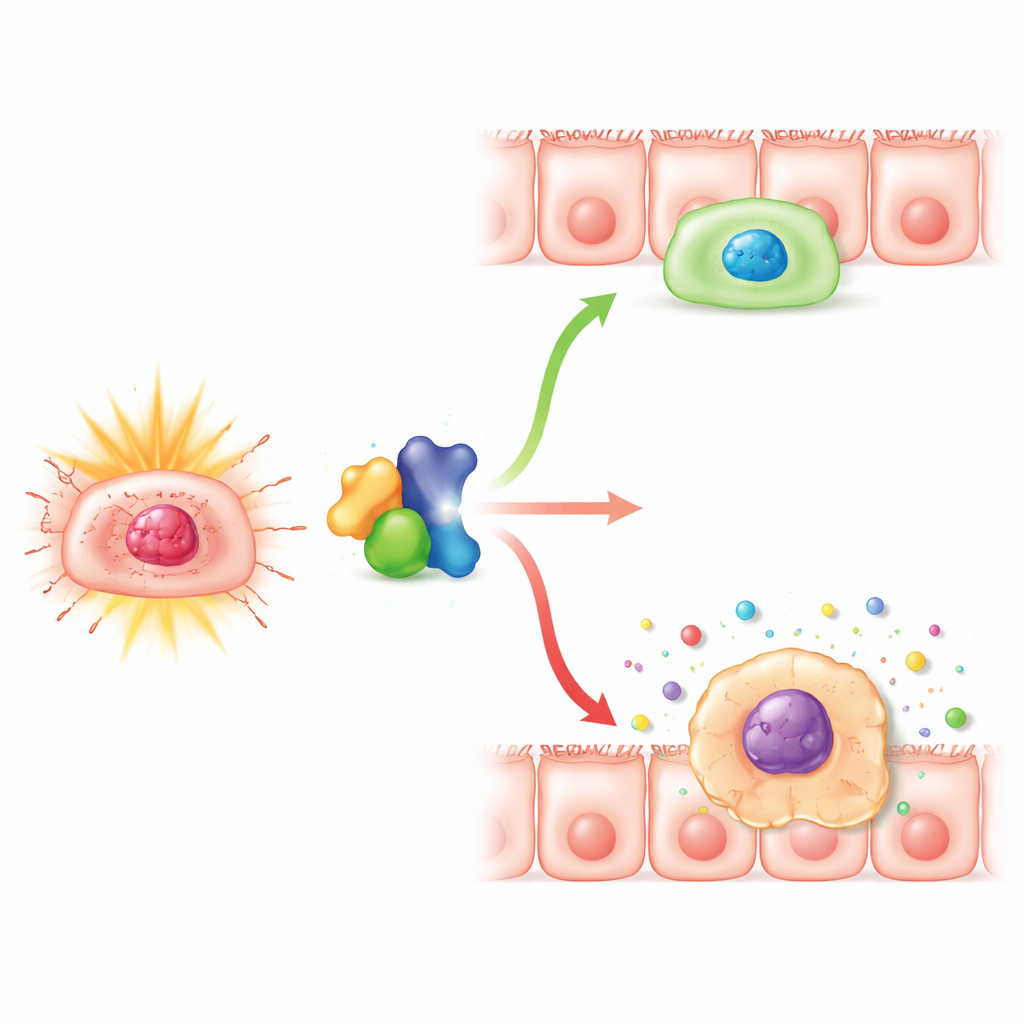
Een moleculaire partner die het evenwicht doet doorslaan
De onderzoekers richtten zich vervolgens op PLK1, een eiwit dat cellen helpt de laatste stappen van deling te doorlopen en te herstellen van stopmomenten na stress. Eerder werk had gesuggereerd dat Numb en PLK1 op elkaar inwerken. Hier bevestigde het team dat de twee eiwitten fysiek geassocieerd zijn in intestinale cellen en dat het verlagen van Numb ook PLK1-niveaus verminderde. Alleen het blokkeren van PLK1 maakte stralingsbehandelde cellen gevoeliger voor senescentie, terwijl het verhogen van PLK1 deels kon herstellen wat de senescente, groei-geremde toestand door Numb-verlies veroorzaakte. Overexpressie van PLK1 verlaagde senescentiemarkers, herstelde celgroei, verminderde het aandeel cellen dat vastzat vóór deling en dempte de afgifte van ontstekingsmoleculen. Deze bevindingen wijzen erop dat Numb helpt PLK1-activiteit op een niveau te houden dat cellen in staat stelt schade te repareren en terug de celcyclus in te gaan in plaats van in een permanente, ontstekingsbevorderende stilstand te belanden.
Wat dit betekent voor patiënten
De studie stelt voor dat Numb, via PLK1, fungeert als hoeder van de darmbarrière tijdens stralingsblootstelling door vroegtijdige veroudering van cellen in het darmslijmvlies te beperken. In plaats van alleen celdood te voorkomen, lijkt deze route beschadigde cellen te sturen naar herstel en gecontroleerd herstel, waardoor de ophoping van senescente, ontsteking-aandrijvende cellen wordt verminderd die de barrière in de loop van de tijd kunnen ondermijnen. Hoewel veel details nog moeten worden uitgewerkt, vooral in levende dieren en menselijke patiënten, wijst het werk op de Numb–PLK1-as als een veelbelovend doel voor behandelingen die de darm tijdens radiotherapie willen beschermen—zodat artsen effectieve kankerdoses kunnen geven met minder risico op chronische darmproblemen.
Bronvermelding: Yang, Y., Hu, X., Pan, Y. et al. Numb mitigates intestinal epithelial cell senescence induced by radiation through a PLK1-dependent pathway. Sci Rep 16, 10876 (2026). https://doi.org/10.1038/s41598-026-44793-x
Trefwoorden: radiation enteritis, darmbarrière, cellulaire senescentie, Numb-eiwit, PLK1