Clear Sky Science · fr
Numb atténue la sénescence des cellules épithéliales intestinales induite par les radiations via une voie dépendante de PLK1
Pourquoi les radiations peuvent endommager l’intestin
La radiothérapie sauve des vies chez de nombreux patients atteints de cancer, mais elle peut être très agressive pour l’intestin. L’épithélium intestinal se renouvelle rapidement, ce qui le rend particulièrement sensible aux radiations. Quand cet épithélium est lésé, la barrière qui empêche normalement les bactéries et les toxines de quitter la lumière intestinale pour rejoindre la circulation commence à devenir perméable. Cette étude examine comment une protéine peu connue, appelée Numb, contribue à protéger la barrière intestinale des effets des radiations, et comment une autre protéine partenaire, PLK1, intervient dans cette protection. Comprendre cette relation pourrait ouvrir la voie à des traitements du cancer moins agressifs, avec moins d’effets digestifs chroniques.
La paroi protectrice de l’intestin sous attaque
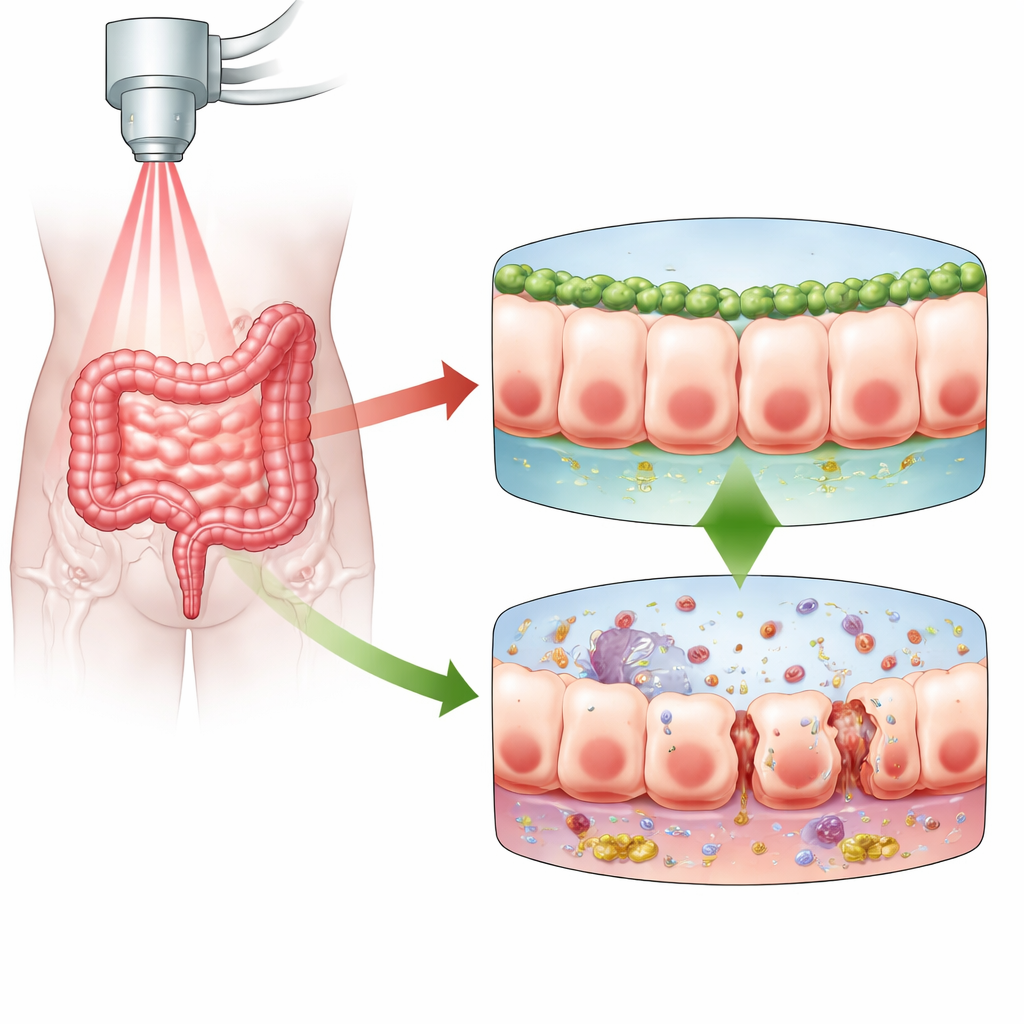
La barrière muqueuse intestinale est une couche unique de cellules étroitement assemblées qui sépare le contenu de l’intestin du reste du corps. Lorsque les radiations atteignent cette barrière, elles endommagent l’ADN des cellules. En réponse, les cellules meurent, s’arrêtent pour réparer leurs dommages, ou entrent dans un état dit de sénescence : elles cessent de se diviser tout en restant vivantes et deviennent souvent fortement pro‑inflammatoires. Les auteurs se sont penchés sur l’entérite radique, une complication douloureuse et parfois invalidante de la radiothérapie pelvienne. Ils ont émis l’hypothèse que Numb, une protéine déjà connue pour aider à maintenir la polarité cellulaire, l’adhérence et la réparation de l’épithélium intestinal, pourrait influencer la réponse des cellules intestinales aux radiations et déterminer si la barrière reste étanche ou devient fuyante.
Une protéine clé aggrave les lésions lorsqu’elle est supprimée
Pour tester le rôle de Numb, les chercheurs ont utilisé des souris et réduit les niveaux de Numb dans leur épithélium intestinal avant de les exposer à des radiations abdominales. Les souris dépourvues de Numb dans ces cellules ont eu des résultats bien pires : davantage en sont mortes, elles ont perdu plus de poids et les marqueurs de perméabilité intestinale dans le sang étaient plus élevés. La microscopie a montré que les jonctions normalement nettes et continues entre cellules voisines étaient perturbées, et que la couche de mucus qui recouvre et protège la surface était amincie et irrégulière. Parallèlement, les molécules inflammatoires dans le tissu intestinal ont fortement augmenté, et les cryptes abritant les cellules souches et assurant le renouvellement intestinal étaient moins nombreuses et plus endommagées. Ces changements convergent vers le constat d’une barrière incapable de se réparer efficacement ou de confiner les éléments nuisibles à l’intérieur de l’intestin.
Lorsque les cellules vieillissent prématurément
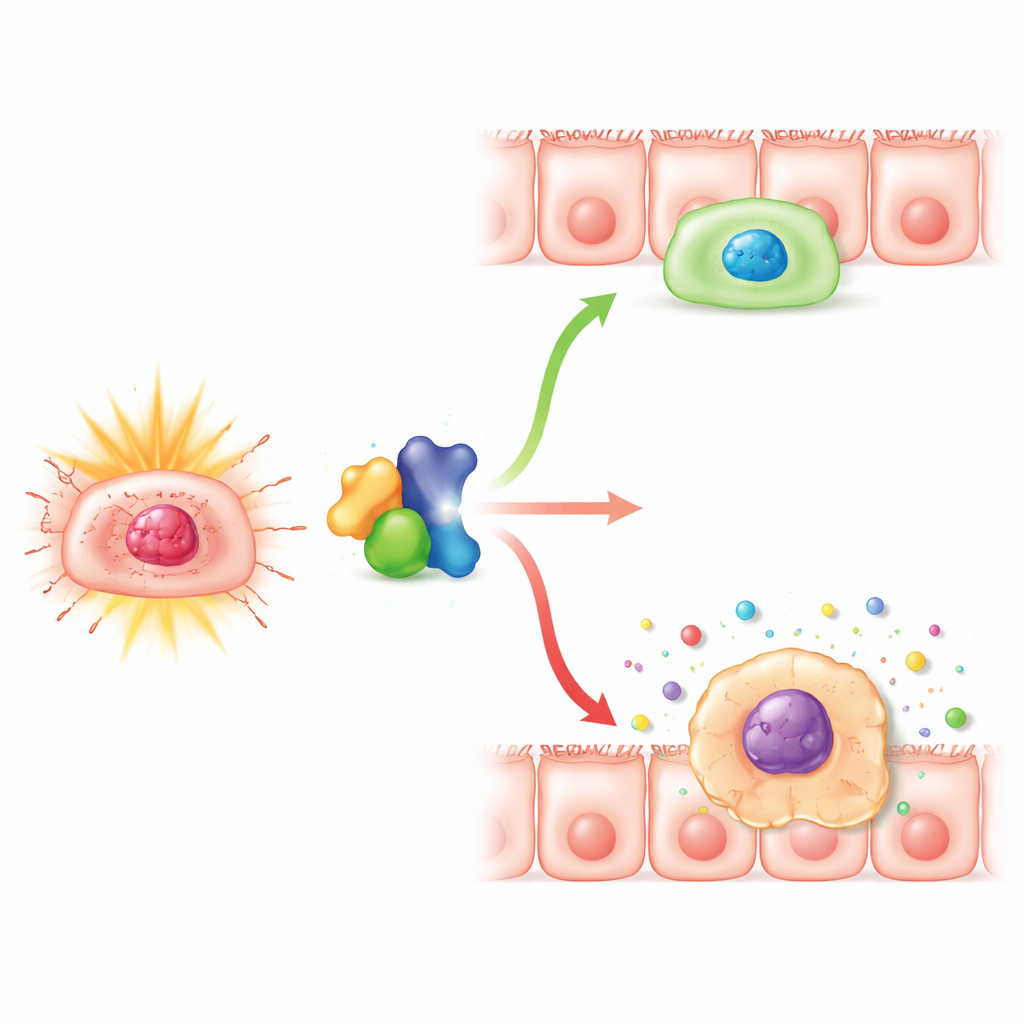
En approfondissant leur analyse, l’équipe a examiné ce qui se passait à l’intérieur des cellules épithéliales elles‑mêmes. Ils ont constaté qu’avec une réduction de Numb, les radiations déclenchaient des signaux persistants de dommages à l’ADN et une forte augmentation des marqueurs de sénescence cellulaire. Plus de cellules adoptaient l’aspect typique de la sénescence et étaient positives au test enzymatique standard de sénescence, alors que l’apoptose globale — la mort cellulaire nette — n’augmentait pas. Dans des lignées cellulaires humaines du côlon en culture, la suppression de Numb n’a pas augmenté la mort cellulaire après irradiation, mais a bien poussé un grand nombre de cellules à s’arrêter durablement dans le cycle cellulaire, surtout dans la phase juste avant la division. Ces cellules arrêtées accumulaient des dommages et des marqueurs de sénescence et commençaient à sécréter des niveaux plus élevés de facteurs inflammatoires, le fameux phénotype sécrétoire associé à la sénescence, qui peut affaiblir davantage le tissu et entretenir une inflammation chronique.
Un partenaire moléculaire qui fait basculer l’équilibre
Les chercheurs se sont ensuite intéressés à PLK1, une protéine qui aide les cellules à franchir les étapes finales de la division et à se remettre des arrêts de contrôle après un stress. Des travaux antérieurs suggéraient une interaction entre Numb et PLK1. Ici, l’équipe a confirmé que les deux protéines s’associent physiquement dans les cellules intestinales et que la diminution de Numb réduit également les niveaux de PLK1. Bloquer PLK1 seul rendait les cellules traitées par radiation plus enclines à la sénescence, tandis qu’augmenter PLK1 pouvait partiellement rétablir l’état de croissance arrêté et sénescent provoqué par la perte de Numb. La surexpression de PLK1 diminuait les marqueurs de sénescence, rétablissait la prolifération cellulaire, réduisait la proportion de cellules bloquées juste avant la division et atténuait la libération de molécules inflammatoires. Ces résultats suggèrent que Numb contribue à maintenir l’activité de PLK1 à un niveau permettant aux cellules de réparer les lésions et de réintégrer le cycle cellulaire au lieu de basculer dans un arrêt permanent et inflammatoire.
Ce que cela signifie pour les patients
L’étude propose que Numb, via PLK1, agit comme un gardien de la barrière intestinale pendant l’exposition aux radiations en limitant le vieillissement cellulaire prématuré de l’épithélium intestinal. Plutôt que de simplement empêcher la mort cellulaire, cette voie semble orienter les cellules endommagées vers la réparation et une récupération contrôlée, réduisant l’accumulation de cellules sénescentes pro‑inflammatoires qui peuvent compromettre la barrière à long terme. De nombreux détails restent à préciser, notamment chez l’animal et chez l’homme, mais ce travail met en lumière l’axe Numb–PLK1 comme une cible prometteuse pour des traitements visant à protéger l’intestin pendant la radiothérapie — ce qui pourrait permettre d’administrer des doses anticancéreuses efficaces tout en épargnant les patients de troubles intestinaux chroniques.
Citation: Yang, Y., Hu, X., Pan, Y. et al. Numb mitigates intestinal epithelial cell senescence induced by radiation through a PLK1-dependent pathway. Sci Rep 16, 10876 (2026). https://doi.org/10.1038/s41598-026-44793-x
Mots-clés: entérite radique, barrière intestinale, sénescence cellulaire, protéine Numb, PLK1