Clear Sky Science · he
נאמב מפחית הזדקנות אפיתל המעי המושרת על ידי קרינה דרך מסלול התלוי ב-PLK1
למה קרינה יכולה לפגוע במעי
טיפול בקרינה מציל חיים עבור סוגים רבים של סרטן, אך עלול להיות קשה עבור המעי. הציפוי של המעי מתחדש במהירות, מה שהופך אותו רגיש במיוחד לקרינה. כשהציפוי הזה נפגע, המחסום שמונע בדרך כלל מחיידקים ורעלנים לצאת מתוך המעי ולהיכנס למחזור הדם מתחיל לדלוף. המחקר בוחן כיצד חלבון כמותו־מעט בשם Numb מסייע להגן על מחסום המעי מפני נזק קרינתי, ואיך שותף חלבוני נוסף, PLK1, משתלב בהגנה זו. הבנת הקשר הזה עשויה להצביע על דרכים לטיפולים אונקולוגיים עדינים יותר עם פחות תופעות לוואי עיכוליות ארוכות טווח.
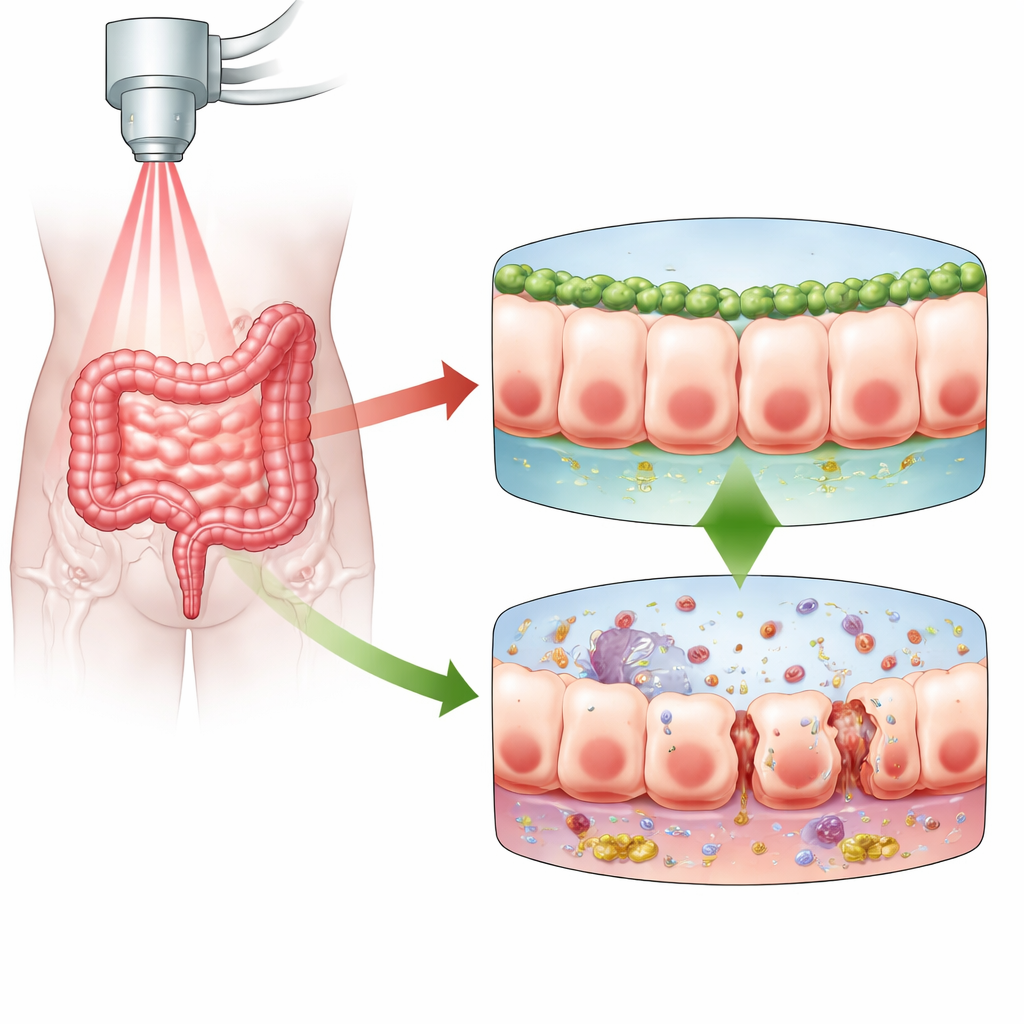
חומת ההגנה של המעי תחת התקפה
מחסום הרירית של המעי הוא שכבה יחידה, תאים צפופים מאוד, שמפרידה בין תכולת המעי לשאר הגוף. כאשר קרינה פוגעת במחסום זה, היא פוגעת ב-DNA שבתוך התאים. בתגובה, התאים ימותו, יעצרו לתקן את עצמם, או יכנסו למצב שנקרא הזדקנות תאית (סניסנס), שבו הם מפסיקים להתחלק אך נשארים חיים ולעתים הופכים דלקתיים מאוד. החוקרים התמקדו באנטריטיס קרינתי, סיבוך כואב ולעתים משתק של רדיותרפיה פלוויאלית. הם הניחו כי Numb, חלבון שידוע כבר כמשתתף בשמירה על קוטביות התא, דבקות ותיקון במעטפת המעי, עשוי להשפיע על תגובת תאי המעי לקרינה והאם המחסום נשמר הדוק או דולף.
חלבון מרכזי שמחמיר את הנזק כשהוא מושתק
כדי לבדוק את תפקידו של Numb, החוקרים השתמשו בעכברים וצמצמו את רמות Numb ברירית המעי לפני חשיפה לקרינה בטנית. עכברים חסרי Numb בתאים אלה עברו הרבה יותר גרוע: יותר מהם מתו, הם איבדו יותר משקל, ומדדים של דליפת מעי בדם היו גבוהים יותר. מיקרוסקופיה הראתה שהמפגשים הסדירים והמתמשכים בין תאים שכנים נותצו, ושכבת הריר שהצפה ומגנה על המשטח נעשתה דקה ומפוזרת. במקביל, מולקולות דלקתיות ברקמת המעי עלו באופן חזק, והשקעים הקטנים שמכילים תאי גזע ומניעים את חידוש המעי היו מועטים יותר ויותר פגועים. יחד, השינויים האלה ציירו תמונה של מחסום שכבר לא יכול לתקן את עצמו ביעילות או לשמור על התוכן המזיק בתוך המעי.
כשתאים מזדקנים מוקדם מדי
בחינה מעמיקה יותר הראתה מה התרחש בתוך תאי האפיתל עצמם. נמצאה עובדה שבמצב של רמות נמוכות של Numb, קרינה עוררה אותות נזק DNA מתמשכים ועלייה בולטת בסמנים של הזדקנות תאית. יותר תאים קיבלו את המאפיינים הקלאסיים של תאים מזדקנים ונבדקו חיוביים לצביעת אנזים סטנדרטית של סניסנס, בעוד שמסת התאים המתים (אפופטוזה) כלל לא עלתה. בתרביות של קווי תאי מעי אנושיים, הסרת Numb לא הגברה את מוות התאים לאחר קרינה, אך דחפה רבים מהם לעצירה ממושכת במחזור התא, במיוחד בשלב מיד לפני החלוקה. תאים תקועים אלה צברו נזקים וסמנים של סניסנס והחלו להפריש רמות גבוהות יותר של גורמי דלקת — התופעה המכונה פרופיל הפרשה מקושר-סניסנס (SASP) — שיכולה להחליש רקמה ולהבעיר דלקת כרונית.
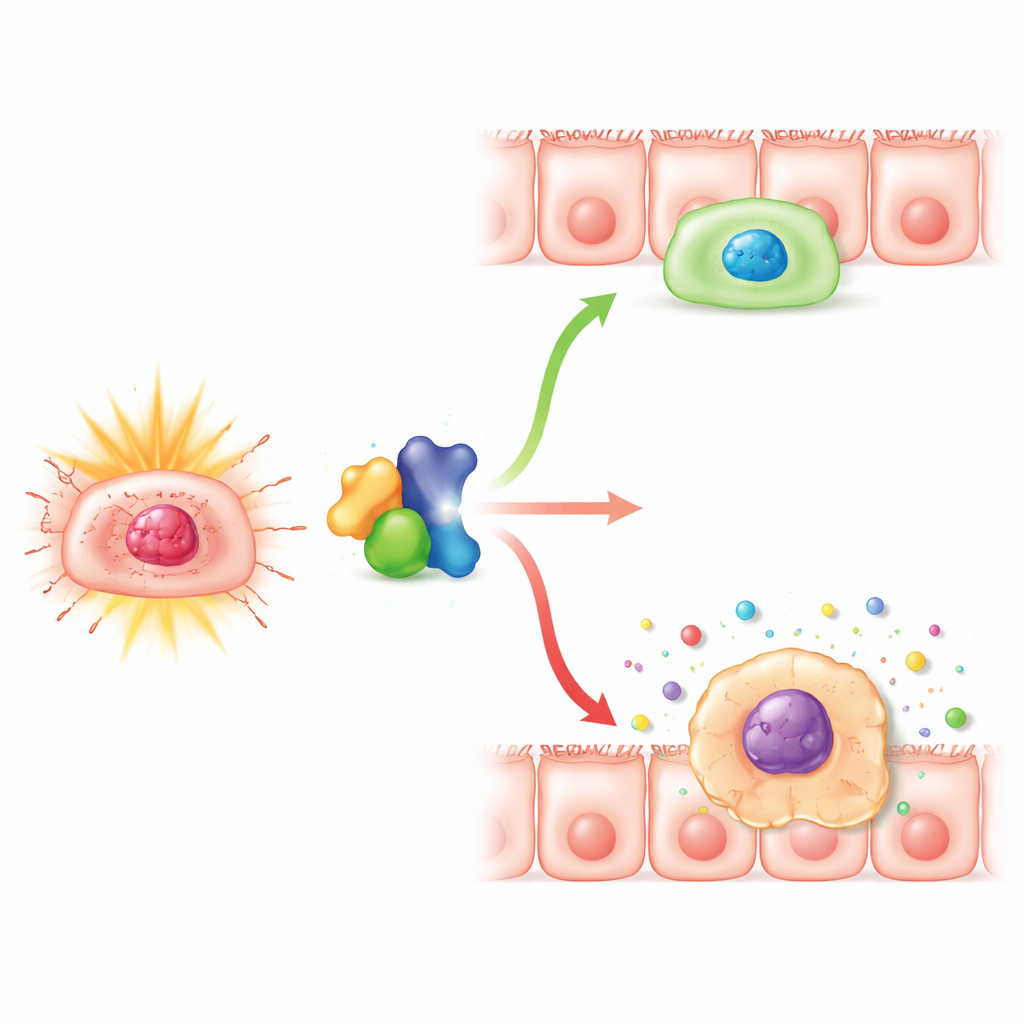
שותף מולקולרי שמשפיע על האיזון
החוקרים פנו אז ל-PLK1, חלבון המסייע לתאים לעבור את השלבים האחרונים של החלוקה ולהתאושש מעצירות צ'ק‑פוינט לאחר סטרס. עבודה קודמת רמזה כי Numb ו-PLK1 מתקשרים. כאן איששה הצוות כי שני החלבונים משויכים פיזית בתאי המעי וכי הורדת Numb גם הפחיתה את רמות PLK1. חסימת PLK1 לבדה הגבירה את הרגישות לסניסנס בתאים שטופלו בקרינה, בעוד הגברת PLK1 יכלה להקל חלקית על מצב הסניסנס ועצירת הגידול שנוצר בשל אובדן Numb. ביטוי יתר של PLK1 הוריד סמני סניסנס, השיב את גדילת התאים, צמצם את השבר של תאים התקועים לפני חלוקה והפחית שחרור מולקולות דלקת. ממצאים אלה מציעים ש-Numb מסייעת לשמור על פעילות PLK1 ברמה שמאפשרת לתאים לתקן נזקים ולחזור למחזור התא במקום ליפול למצב עמיד וקבוע של דלקת.
מה משמעות הדבר עבור מטופלים
המחקר מציע כי Numb, העובדת דרך PLK1, פועלת כשומרת של מחסום המעי במהלך חשיפה לקרינה על ידי הגבלת הזדקנות תאית מוקדמת ברירית המעי. במקום למנוע מוות תאי בלבד, המסלול הזה נראה כמכוון תאים פגועים לתיקון ולהחלמה מבוקרת, מה שמפחית את הצטברות התאים המזדקנים והמעוררי דלקת שעלולים לערער את המחסום עם הזמן. בעוד שפרטים רבים עוד נדרשים לבירור, במיוחד בחיות חיות ובמטופלים בני אדם, העבודה מצביעה על ציר Numb–PLK1 כמטרה מבטיחה לטיפולים שנועדו להגן על המעי במהלך רדיותרפיה — דבר שעשוי לאפשר לרופאים לתת מינוני סרטני יעילים ובו בזמן להקל על מטופלים מהתסמינים המעי הכרוניים.
ציטוט: Yang, Y., Hu, X., Pan, Y. et al. Numb mitigates intestinal epithelial cell senescence induced by radiation through a PLK1-dependent pathway. Sci Rep 16, 10876 (2026). https://doi.org/10.1038/s41598-026-44793-x
מילות מפתח: אנטריטיס קרינתי, מחסום המעי, הזדקנות תאית, חלבון Numb, PLK1