Clear Sky Science · pt
Numb mitiga a senescência de células epiteliais intestinais induzida por radiação através de uma via dependente de PLK1
Por que a radiação pode prejudicar o intestino
A radioterapia é um tratamento que salva vidas em muitos tipos de câncer, mas pode ser severa para o intestino. O revestimento das nossas entranhas se renova rapidamente, tornando-o especialmente sensível à radiação. Quando esse revestimento é danificado, a barreira que normalmente mantém bactérias e toxinas dentro do intestino e longe da corrente sanguínea começa a vazar. Este estudo investiga como uma proteína pouco conhecida chamada Numb ajuda a proteger a barreira intestinal do dano causado pela radiação e como outra parceira, a proteína PLK1, se enquadra nessa proteção. Compreender essa relação pode apontar caminhos para tratamentos contra o câncer mais suaves, com menos efeitos digestivos crônicos.
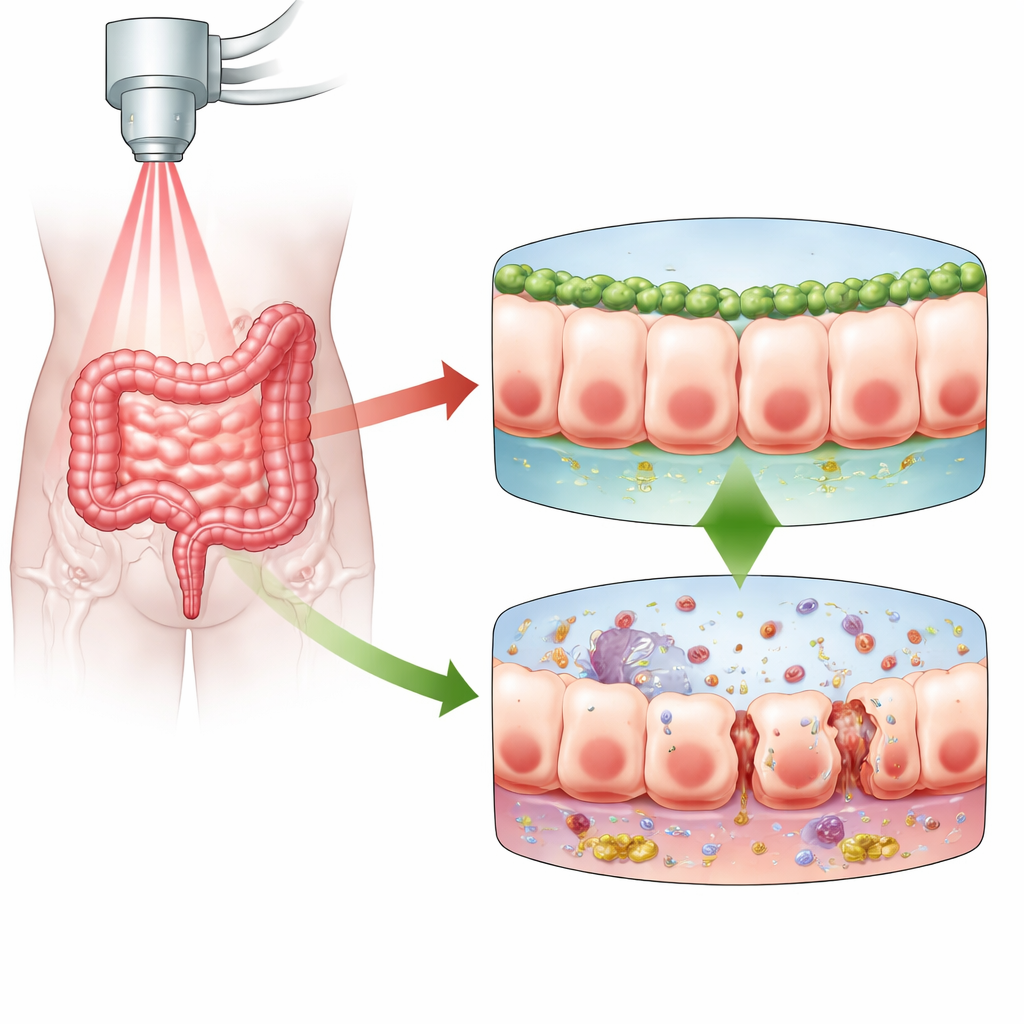
A muralha protetora do intestino sob ataque
A barreira mucosa intestinal é uma camada única e compacta de células que separa o conteúdo do intestino do resto do corpo. Quando a radiação atinge essa barreira, ela danifica o DNA dentro dessas células. Em resposta, as células ou morrem, fazem uma pausa para se reparar, ou entram em um estado chamado senescência, no qual deixam de se dividir, permanecem vivas e frequentemente se tornam altamente inflamatórias. Os autores focaram na enterite por radiação, uma complicação dolorosa e às vezes incapacitante da radioterapia pélvica. Eles levantaram a hipótese de que Numb, uma proteína já conhecida por ajudar a manter a polaridade celular, adesão e reparo no revestimento intestinal, poderia influenciar como as células intestinais respondem à radiação e se a barreira se mantém estanque ou passa a vazar.
Uma proteína chave piora o dano quando é silenciada
Para testar o papel de Numb, os pesquisadores usaram camundongos e reduziram os níveis de Numb no revestimento intestinal antes de expô-los à radiação abdominal. Camundongos sem Numb nessas células se saíram muito pior: mais deles morreram, perderam mais peso e medidas de permeabilidade intestinal no sangue foram maiores. A microscopia mostrou que as junções normalmente ordenadas e contínuas entre células vizinhas foram perturbadas, e a camada de muco que reveste e protege a superfície tornou-se fina e irregular. Ao mesmo tempo, moléculas inflamatórias no tecido intestinal aumentaram acentuadamente, e as pequenas criptas que abrigam as células-tronco e impulsionam a renovação intestinal estavam menos numerosas e mais danificadas. Em conjunto, essas alterações desenharam o retrato de uma barreira que não conse-gue mais se reparar eficientemente nem manter conteúdos nocivos confinados ao intestino.
Quando as células envelhecem cedo demais
Aprofundando, a equipe examinou o que ocorria dentro das próprias células epiteliais. Eles descobriram que, com Numb reduzido, a radiação desencadeou sinais mais persistentes de dano ao DNA e um forte aumento em marcadores de senescência celular. Mais células assumiram a aparência clássica de senescentes e testaram positivo para uma coloração enzimática padrão de senescência, embora a apoptose geral — morte celular direta — não tenha aumentado. Em linhagens de células de cólon humano em cultura, remover Numb não aumentou a morte celular após a radiação, mas empurrou muitas delas para uma parada prolongada do ciclo celular, especialmente na fase imediatamente anterior à divisão. Essas células paradas acumularam danos e marcadores de senescência e passaram a secretar níveis maiores de fatores inflamatórios, o chamado fenótipo secretor associado à senescência, que pode enfraquecer ainda mais o tecido e alimentar inflamação crônica.
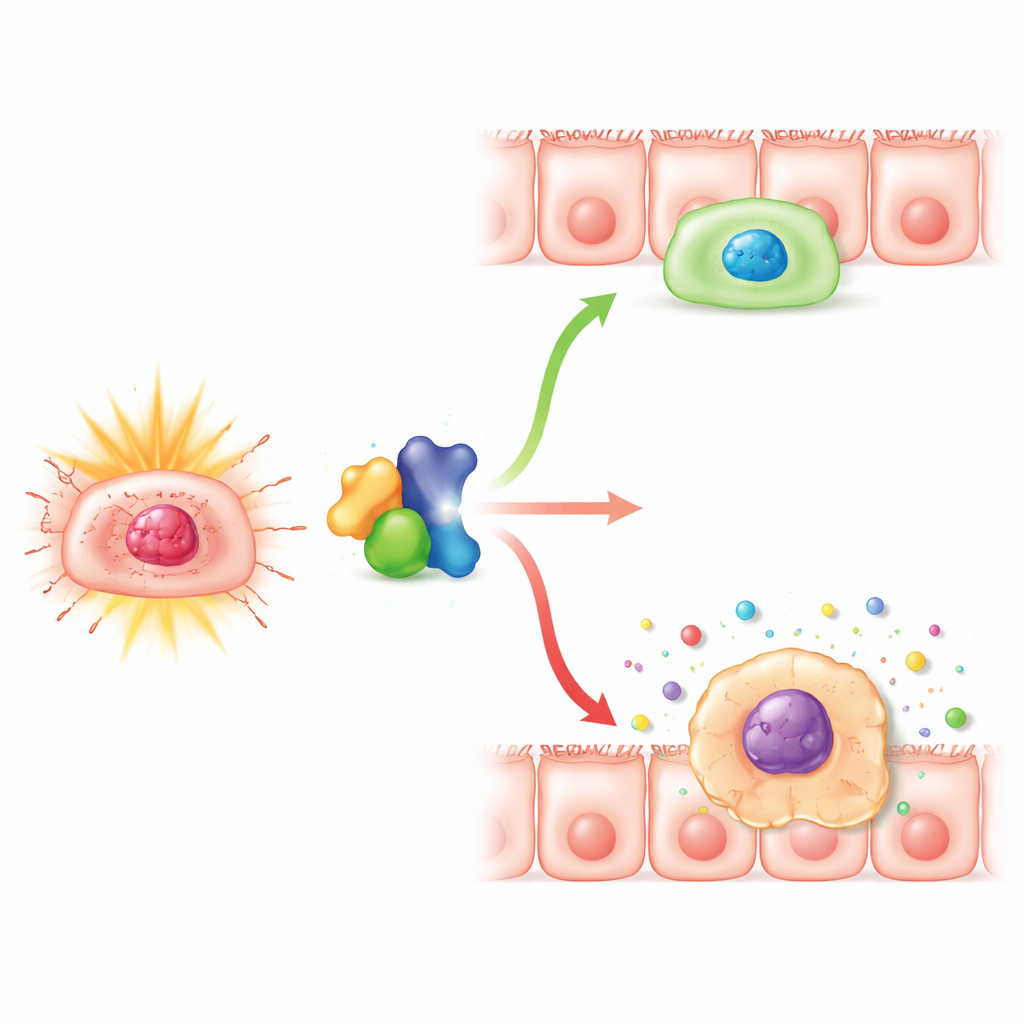
Uma parceira molecular que muda o equilíbrio
Os pesquisadores então voltaram sua atenção para PLK1, uma proteína que ajuda as células a completar os passos finais da divisão e a se recuperar de pausas de checagem após o estresse. Trabalhos anteriores já sugeriam que Numb e PLK1 interagem. Aqui, a equipe confirmou que as duas proteínas se associam fisicamente em células intestinais e que reduzir Numb também diminuiu os níveis de PLK1. Bloquear PLK1 sozinho tornou as células tratadas com radiação mais propensas à senescência, enquanto aumentar PLK1 pôde resgatar em parte o estado senescente e de parada de crescimento causado pela perda de Numb. Superexpressar PLK1 reduziu marcadores de senescência, restaurou o crescimento celular, diminuiu a fração de células presas antes da divisão e atenuou a liberação de moléculas inflamatórias. Esses achados sugerem que Numb ajuda a manter a atividade de PLK1 em um nível que permita às células reparar danos e reentrar no ciclo celular em vez de deslizar para uma paralisa permanente e inflamatória.
O que isso significa para pacientes
O estudo propõe que Numb, agindo por meio de PLK1, funciona como um guardião da barreira intestinal durante a exposição à radiação ao limitar o envelhecimento celular precoce no revestimento do intestino. Em vez de simplesmente prevenir a morte celular, essa via parece orientar células danificadas para o reparo e a recuperação controlada, reduzindo o acúmulo de células senescentes que promovem inflamação e podem comprometer a barreira ao longo do tempo. Embora muitos detalhes ainda precisem ser esclarecidos, especialmente em animais vivos e em pacientes humanos, o trabalho aponta o eixo Numb–PLK1 como um alvo promissor para tratamentos destinados a proteger o intestino durante a radioterapia — potencialmente permitindo que os médicos administrem doses eficazes contra o câncer enquanto poupam os pacientes de problemas intestinais crônicos.
Citação: Yang, Y., Hu, X., Pan, Y. et al. Numb mitigates intestinal epithelial cell senescence induced by radiation through a PLK1-dependent pathway. Sci Rep 16, 10876 (2026). https://doi.org/10.1038/s41598-026-44793-x
Palavras-chave: enterite por radiação, barreira intestinal, senescência celular, proteína Numb, PLK1