Clear Sky Science · de
Numb mindert die durch Strahlung ausgelöste Seneszenz intestinaler Epithelzellen über einen PLK1‑abhängigen Weg
Warum Strahlung dem Darm schaden kann
Strahlentherapie rettet vielen Krebspatienten das Leben, kann aber dem Darm stark zusetzen. Das Epithel der Darmschleimhaut erneuert sich sehr schnell und ist daher besonders strahlenempfindlich. Wird diese Schleimhautschicht geschädigt, beginnt die Barriere, die normalerweise Bakterien und Toxine im Darm hält und vom Blutkreislauf fernhält, zu lecken. Diese Studie untersucht, wie ein wenig untersuchtes Protein namens Numb die intestinale Barriere vor Strahlenschäden schützt und welche Rolle ein weiterer Partner, PLK1, in diesem Schutzmechanismus spielt. Das Verständnis dieser Beziehung könnte Wege zu verträglicheren Krebstherapien mit weniger langfristigen Verdauungsnebenwirkungen eröffnen. 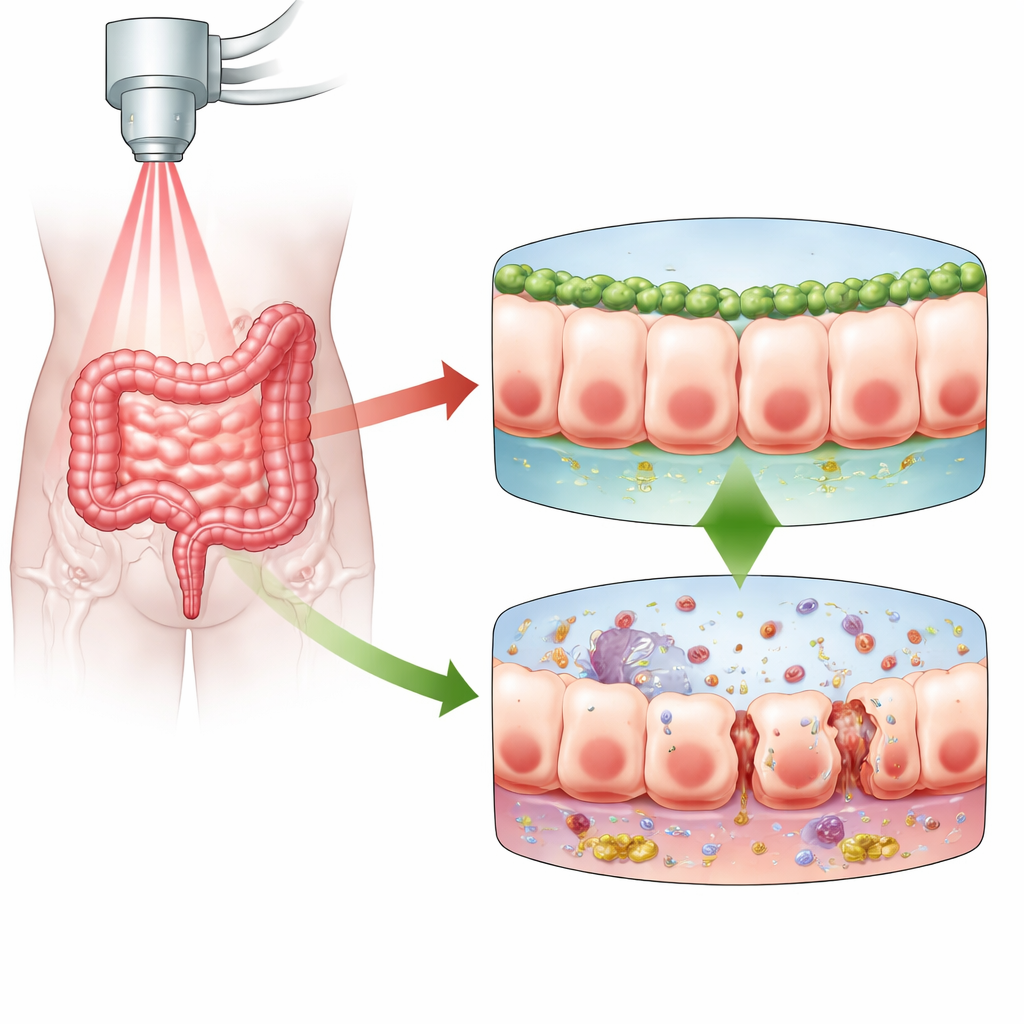
Die Schutzmauer des Darms unter Beschuss
Die intestinale mukosale Barriere besteht aus einer einzigen, dicht gepackten Zellschicht, die den Inhalt des Darms vom restlichen Körper trennt. Trifft Strahlung auf diese Barriere, schädigt sie die DNA in diesen Zellen. Als Reaktion darauf sterben Zellen, stellen ihre Teilung vorübergehend ein, um sich zu reparieren, oder sie treten in einen Zustand der Seneszenz ein, in dem sie nicht mehr teilen, aber weiterleben und häufig stark proinflammatorisch werden. Die Autoren konzentrierten sich auf die Strahlenenteritis, eine schmerzhafte und mitunter behindernde Komplikation bei Beckenbestrahlungen. Sie vermuteten, dass Numb — ein Protein, das bereits dafür bekannt ist, Zellpolarität, Zelladhäsion und Reparatur in der Darmwand zu unterstützen — beeinflussen könnte, wie Darmepithelzellen auf Strahlung reagieren und ob die Barriere dicht bleibt oder undicht wird.
Ein Schlüsselprotein verschlechtert Schäden, wenn es ausgeschaltet ist
Um die Rolle von Numb zu prüfen, reduzierten die Forschenden in Mäusen die Numb‑Spiegel im Darmepithel, bevor sie Bestrahlungen des Bauchraums durchführten. Mäuse ohne Numb in diesen Zellen kamen deutlich schlechter zurecht: mehr Tiere starben, sie verloren mehr Gewicht und im Blut zeigten sich höhere Werte für Darmdurchlässigkeit. Die Mikroskopie offenbarte, dass die normalerweise ordentlichen, durchgehenden Verbindungen zwischen Nachbarzellen gestört waren und die Schleimschicht, die die Oberfläche schützt, dünn und fleckig wurde. Gleichzeitig stiegen entzündliche Moleküle im Darmgewebe stark an, und die winzigen Krypten, die Stammzellen beherbergen und die Darmerneuerung antreiben, waren seltener und stärker geschädigt. Zusammengenommen zeichneten diese Veränderungen das Bild einer Barriere, die sich nicht mehr effizient reparieren oder schädliche Inhalte im Darm halten kann.
Wenn Zellen zu früh altern
Bei genaueren Untersuchungen in den Epithelzellen stellten die Forschenden fest, dass bei reduziertem Numb Strahlung anhaltendere DNA‑Schadenssignale auslöste und die Marker der zellulären Seneszenz deutlich anstiegen. Mehr Zellen nahmen das typische Erscheinungsbild seneszenter Zellen an und testeten positiv auf einen gängigen Seneszenzenzym‑Farbtest, während die Gesamtapoptose — also der vollständige Zelltod — nicht zunahm. In kultivierten humanen Kolonzelllinien führte das Entfernen von Numb nicht zu mehr Strahlungs‑induziertem Zelltod, drängte aber viele Zellen in einen lang anhaltenden Stillstand im Zellzyklus, insbesondere in die Phase unmittelbar vor der Teilung. Diese blockierten Zellen häuften Schäden und Seneszenzmarker an und begannen, vermehrt entzündungsfördernde Faktoren auszuschütten — das sogenannte seneszenz‑assoziierte sekretorische Phänotyp —, was Gewebe weiter schwächen und chronische Entzündungen anheizen kann. 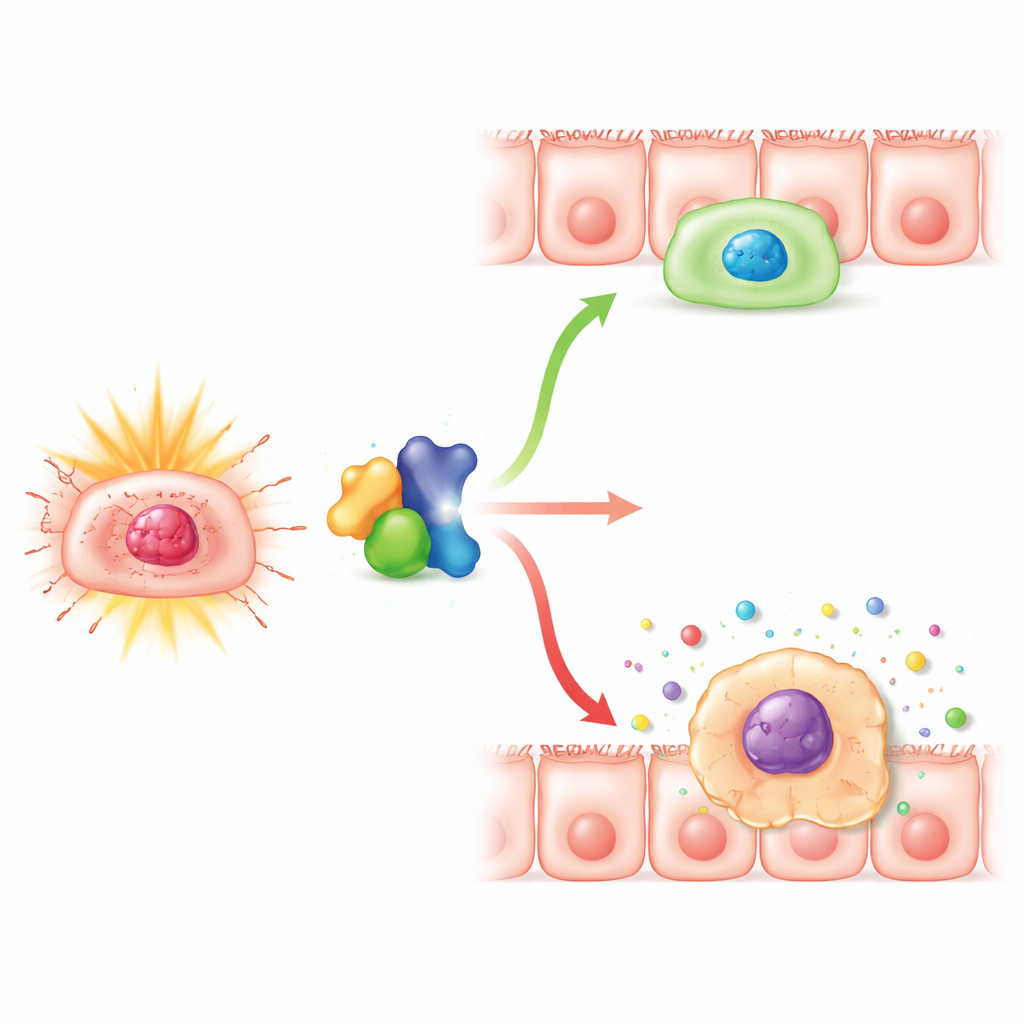
Ein molekularer Partner, der das Gleichgewicht kippt
Die Forschenden richteten anschließend ihren Fokus auf PLK1, ein Protein, das Zellen hilft, die letzten Schritte der Zellteilung zu durchlaufen und sich nach Stress‑bedingten Kontrollpunktpausen zu erholen. Frühere Arbeiten deuteten bereits auf eine Interaktion zwischen Numb und PLK1 hin. Hier bestätigte das Team, dass die beiden Proteine in Darmzellen physisch assoziieren und dass die Reduktion von Numb auch die PLK1‑Spiegel senkt. Eine alleinige Hemmung von PLK1 machte bestrahlte Zellen anfälliger für Seneszenz, während eine Erhöhung von PLK1 den seneszenten, wachstumsarrestierten Zustand, der durch Numb‑Verlust entstand, teilweise rückgängig machen konnte. Die Überexpression von PLK1 verringerte Seneszenzmarker, stellte das Zellwachstum wieder her, reduzierte den Anteil der vor der Teilung blockierten Zellen und dämpfte die Freisetzung entzündlicher Moleküle. Diese Befunde legen nahe, dass Numb hilft, die PLK1‑Aktivität auf einem Niveau zu halten, das Zellen erlaubt, Schäden zu reparieren und wieder in den Zellzyklus einzutreten, statt in einen dauerhaften, entzündungsfördernden Stillstand zu verfallen.
Was das für Patientinnen und Patienten bedeutet
Die Studie schlägt vor, dass Numb über PLK1 als Wächter der intestinalen Barriere bei Strahlenexposition wirkt, indem es ein vorzeitiges Altern der Darmschleimhautzellen begrenzt. Anstatt nur den Zelltod zu verhindern, scheint dieser Weg beschädigte Zellen in Richtung Reparatur und kontrollierter Erholung zu lenken und so die Anhäufung seneszenter, entzündungsfördernder Zellen zu verringern, die die Barriere im Verlauf unterminieren können. Zwar sind noch viele Details zu klären, insbesondere in lebenden Tiermodellen und bei Patientinnen und Patienten, doch die Arbeit macht die Numb–PLK1‑Achse zu einem vielversprechenden Ziel für Therapien, die den Darm während der Strahlentherapie schützen könnten — womit Ärzten möglicherweise wirksame Krebsdosen verabreicht werden können, ohne die Patienten langfristig an chronische Darmprobleme zu binden.
Zitation: Yang, Y., Hu, X., Pan, Y. et al. Numb mitigates intestinal epithelial cell senescence induced by radiation through a PLK1-dependent pathway. Sci Rep 16, 10876 (2026). https://doi.org/10.1038/s41598-026-44793-x
Schlüsselwörter: Strahlenenteritis, intestinaler Barrier, zelluläre Seneszenz, Numb‑Protein, PLK1