Clear Sky Science · ru
Numb снижает старение эпителиальных клеток кишечника, вызванное радиацией, через путь, зависящий от PLK1
Почему радиация может повредить кишечник
Лучевая терапия спасает жизни при многих видах рака, но может быть жесткой для кишечника. Слой клеток, выстилающий кишечник, обновляется очень быстро, поэтому он особенно чувствителен к радиации. Когда эта оболочка повреждается, барьер, который обычно удерживает бактерии и токсины внутри кишечника и не допускает их в кровоток, начинает пропускать. В этом исследовании изучают, как малоизвестный белок Numb помогает защищать кишечный барьер от радиационного повреждения и какую роль в этой защите играет его партнёр PLK1. Понимание этой взаимосвязи может указать путь к более мягким методам лечения рака с меньшими долгосрочными побочными эффектами для пищеварения. 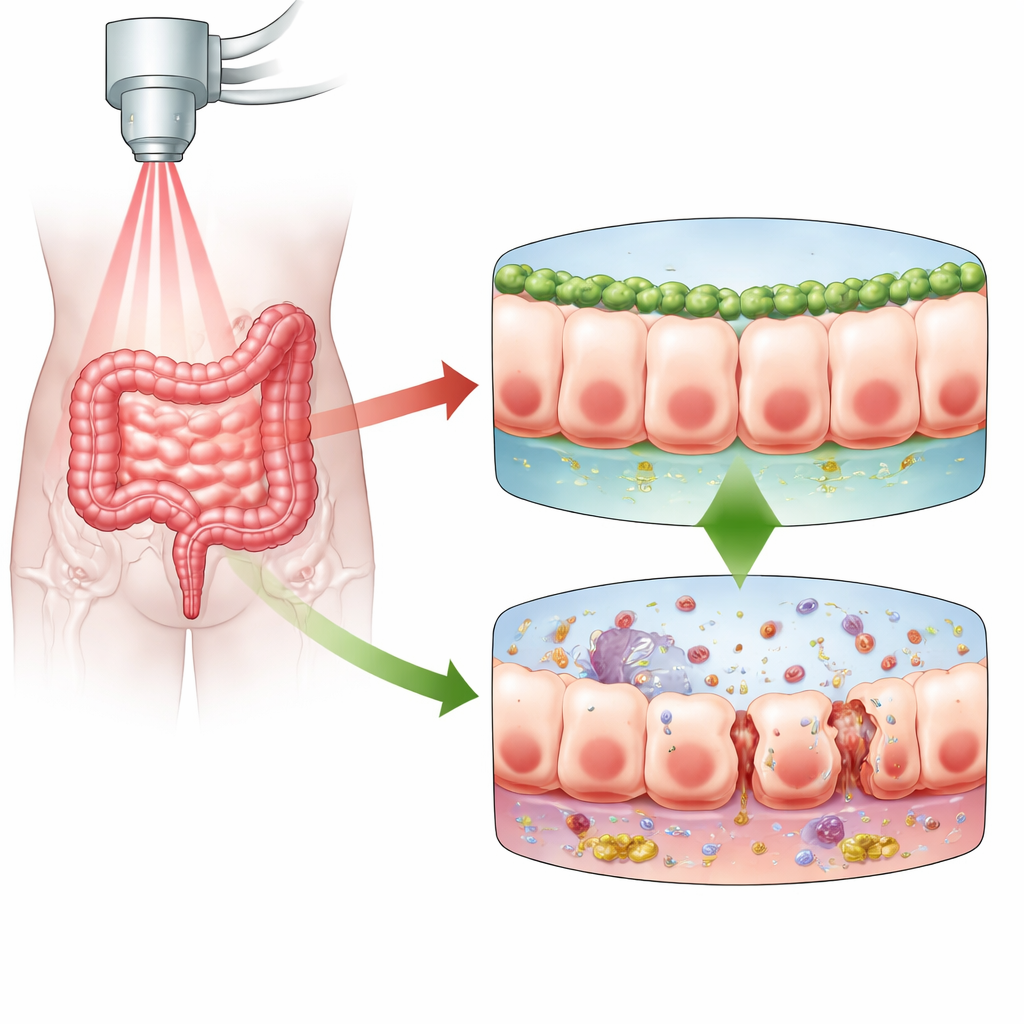
Защитная стенка кишечника под ударом
Муцинозный (слизистый) барьер кишечника — это однослойный, плотно упакованный слой клеток, отделяющий содержимое кишечника от остального организма. При облучении этот барьер получает повреждение ДНК в клетках. В ответ клетки либо погибают, либо останавливаются для ремонта, либо входят в состояние, называемое сенесценцией, при котором они перестают делиться, оставаясь живыми и часто становясь высоко воспалительными. Авторы сосредоточились на радиационном энтерите — болезненном и иногда инвалидизирующем осложнении тазовой лучевой терапии. Они предположили, что Numb, белок, уже известный своей ролью в поддержании полярности клеток, адгезии и ремонта слизистой, может влиять на реакцию кишечных клеток на радиацию и на то, останется ли барьер плотным или станет проницаемым.
Ключевой белок усугубляет повреждение при его подавлении
Чтобы проверить роль Numb, исследователи использовали мышей и уменьшали уровень Numb в эпителии кишечника перед воздействием абдоминального облучения. Мыши с дефицитом Numb в этих клетках переносили облучение гораздо хуже: у них повышалась смертность, они теряли больше веса, а показатели проницаемости кишечника в крови были выше. Микроскопия показала, что обычно аккуратные, непрерывные контакты между соседними клетками нарушались, а слизистый слой, покрывающий поверхность, становился тонким и пятнистым. Одновременно в ткани кишечника резко возрастали уровни воспалительных молекул, а крошечные крипты, где находятся стволовые клетки и происходит обновление кишечника, сокращались и повреждались. В совокупности эти изменения рисовали картину барьера, который уже не мог эффективно восстанавливаться или удерживать вредное содержимое внутри кишечника.
Когда клетки стареют слишком рано
Углубившись, команда изучила, что происходило внутри самих эпителиальных клеток. Они обнаружили, что при снижении Numb радиация вызывала более стойкие сигналы о повреждении ДНК и резкое повышение маркеров клеточной сенесценции. Больше клеток приобретали типичный для сенесцентных клеток вид и давали положительную реакцию на стандартное окрашивание фермента старения, при этом общая апоптозная гибель клеток не увеличивалась. В культурах человеческих клеточных линий колоректального эпителия удаление Numb не повышало гибель клеток после облучения, но приводило многие клетки к продолжительной остановке клеточного цикла, особенно на стадии непосредственно перед делением. Эти задержанные клетки накапливали повреждения и маркеры сенесценции и начинали секретировать повышенные уровни воспалительных факторов — так называемый сенесценцией‑ассоциированный секреторный фенотип, который дополнительно ослабляет ткань и подпитывает хроническое воспаление. 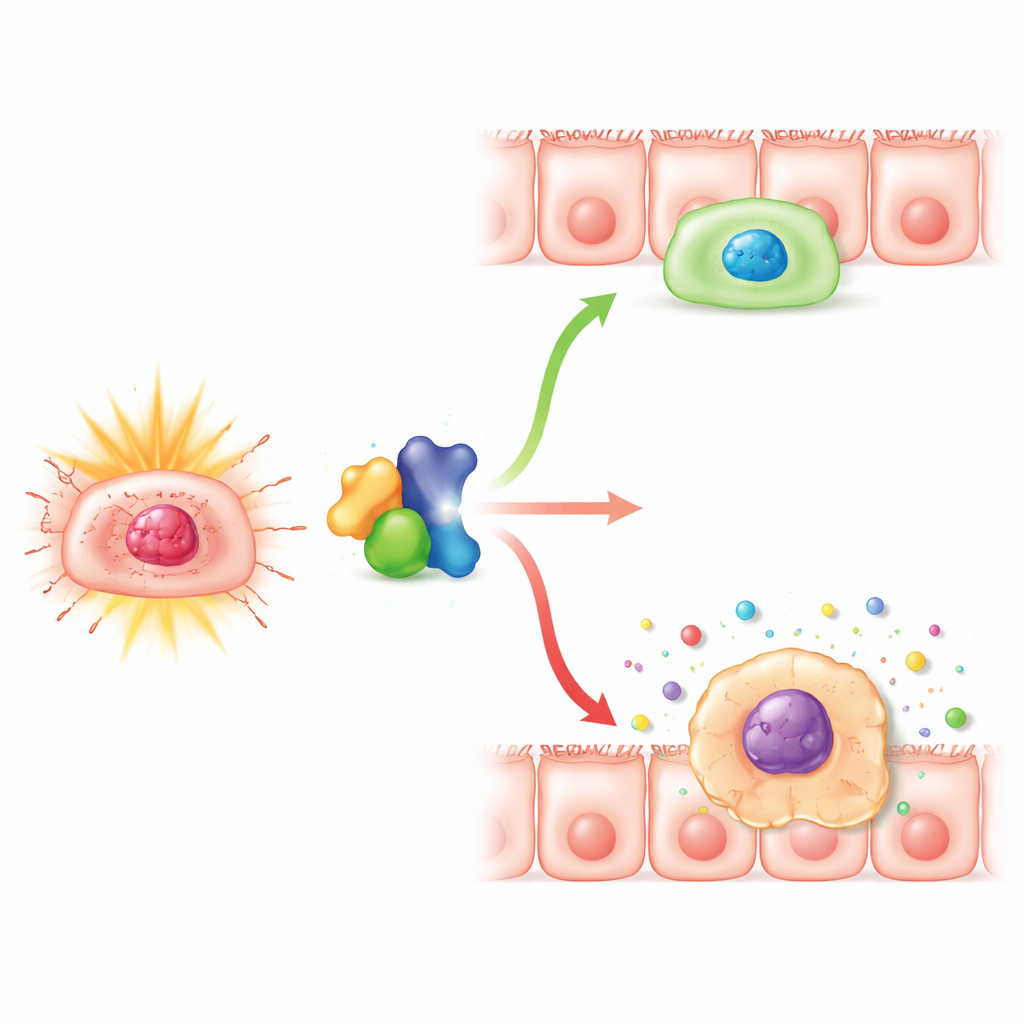
Молекулярный партнёр, который меняет баланс
Затем исследователи обратились к PLK1 — белку, который помогает клеткам завершать последние этапы деления и восстанавливаться после остановок на контрольных точках при стрессе. Ранее имелась подсказка, что Numb и PLK1 взаимодействуют. Здесь команда подтвердила, что оба белка физически ассоциируют в кишечных клетках и что снижение Numb также уменьшает уровни PLK1. Блокада PLK1 сама по себе делала облучённые клетки более склонными к сенесценции, в то время как усиление PLK1 могло частично обратить сенесцентное состояние и остановку роста, вызванные потерей Numb. Переэкспрессия PLK1 снижала маркеры сенесценции, восстанавливала рост клеток, уменьшала долю клеток, застрявших перед делением, и снижала выброс воспалительных молекул. Эти данные предполагают, что Numb помогает поддерживать активность PLK1 на уровне, который позволяет клеткам ремонтировать повреждения и возвращаться в клеточный цикл, вместо того чтобы увязнуть в постоянной воспалительной стазе.
Что это значит для пациентов
В исследовании выдвинута гипотеза, что Numb, действуя через PLK1, выступает хранителем кишечного барьера при воздействии радиации, ограничивая преждевременное старение клеток в слизистой. Вместо простого предотвращения гибели клеток этот путь, по-видимому, направляет повреждённые клетки к ремонту и контролируемому восстановлению, уменьшая накопление сенесцентных, провоцирующих воспаление клеток, которые со временем могут подорвать барьер. Хотя остаётся много деталей, которые нужно уточнить, особенно в живых животных и у пациентов, работа указывает на ось Numb–PLK1 как перспективную мишень для препаратов, предназначенных защищать кишечник во время радиотерапии — потенциально позволяя врачам проводить эффективные курсы лечения рака, снижая риск хронических проблем с кишечником у пациентов.
Цитирование: Yang, Y., Hu, X., Pan, Y. et al. Numb mitigates intestinal epithelial cell senescence induced by radiation through a PLK1-dependent pathway. Sci Rep 16, 10876 (2026). https://doi.org/10.1038/s41598-026-44793-x
Ключевые слова: радиационный энтерит, кишечный барьер, клеточное старение, белок Numb, PLK1