Clear Sky Science · zh
整合湿实验室与计算方法发现并表征与抗生素协同作用的溶藻噬菌体,用以对抗多药耐药的鲍曼不动杆菌
旧有细菌敌人获得新盟友
耐药感染使曾经例行的医院治疗变得危险,尤其当罪魁祸首是鲍曼不动杆菌——一种能抵抗多种抗生素、难以根除的细菌。本研究探讨了捕食细菌的病毒(称为噬菌体或噬菌病毒)如何在日常污水中被发现,随后在实验室与计算分析中被训练和测试,以便与现代抗生素联手对抗这些顽固的医院病原体。 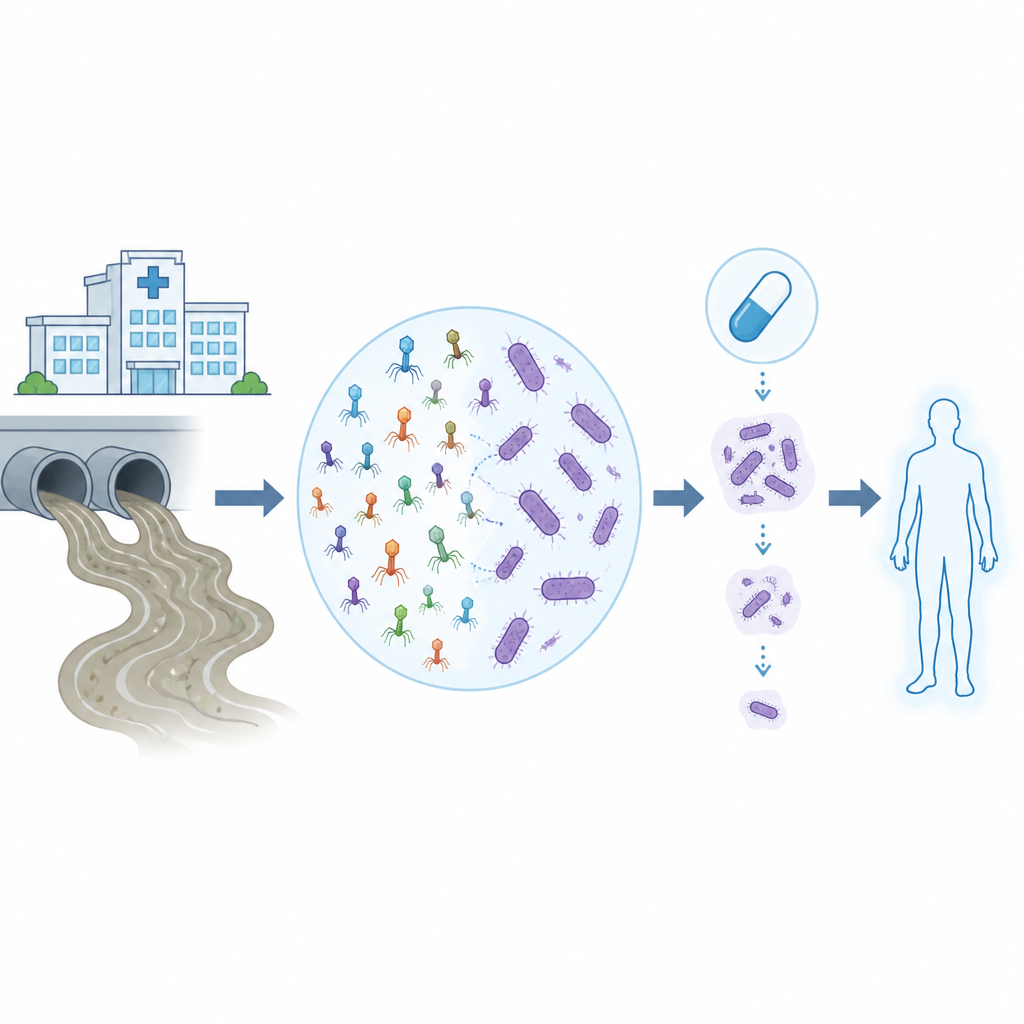
在污水中寻找有用的病毒
研究人员首先组建了来自意大利多家医院的二十株多药耐药A. baumannii菌株库。通过基因指纹识别,他们选择了两株代表性菌株作为诱饵,将其暴露于未经处理的污水中——这是噬菌体的丰富天然库。只有一株,称为Abau1,能培养出在平板上形成明显细菌坏死斑点的噬菌体。电子显微镜显示了四种相关噬菌体,均属于同一大类病毒,但呈现两种不同的形态,提示其生活方式和行为可能各异。
将有力杀手与安静搭便车者区分开来
并非所有噬菌体都适合治疗,因为有些噬菌体倾向于安静地嵌入细菌DNA中,而不是摧毁宿主。团队对噬菌体基因组进行了测序,并将其与宿主细菌的基因组进行比对。结果显示两种噬菌体几乎与嵌入Abau1染色体的片段相同,表明它们是来源于宿主的搭便车者,可能会转为温和(溶原)生活方式。另两种被命名为ΦAb1-SL1和ΦAb1-SL2,则未与宿主DNA重叠,且未携带已知的毒性或抗生素抗性基因,标志着它们是纯粹的裂解型噬菌体,能够可靠地裂解并杀死目标细菌。
测试强度、适应范围与与药物的协同
接着科学家评估了这两种裂解噬菌体的耐受力与多面性。两者在广泛的温度与酸碱条件下均保持感染性,包括类似人体某些部位的环境,并能在细菌内高效增殖。然而,它们只能感染一小群共享特定外膜荚膜类型的A. baumannii菌株,这强调了噬菌体常像锁与钥匙那样的特异性。最引人注意的是,噬菌体ΦAb1-SL1与几种头孢类抗生素,尤其是cefiderocol,显示出强烈的协同效应。体外实验表明,将该噬菌体与低剂量cefiderocol联合使用,比单独任何一种处理都能更显著抑制细菌生长,并将该菌株从耐药范围中移出所需的抗生素剂量降低,而这种帮助在碳青霉烯类药物美洛培南(meropenem)中未见显著表现。 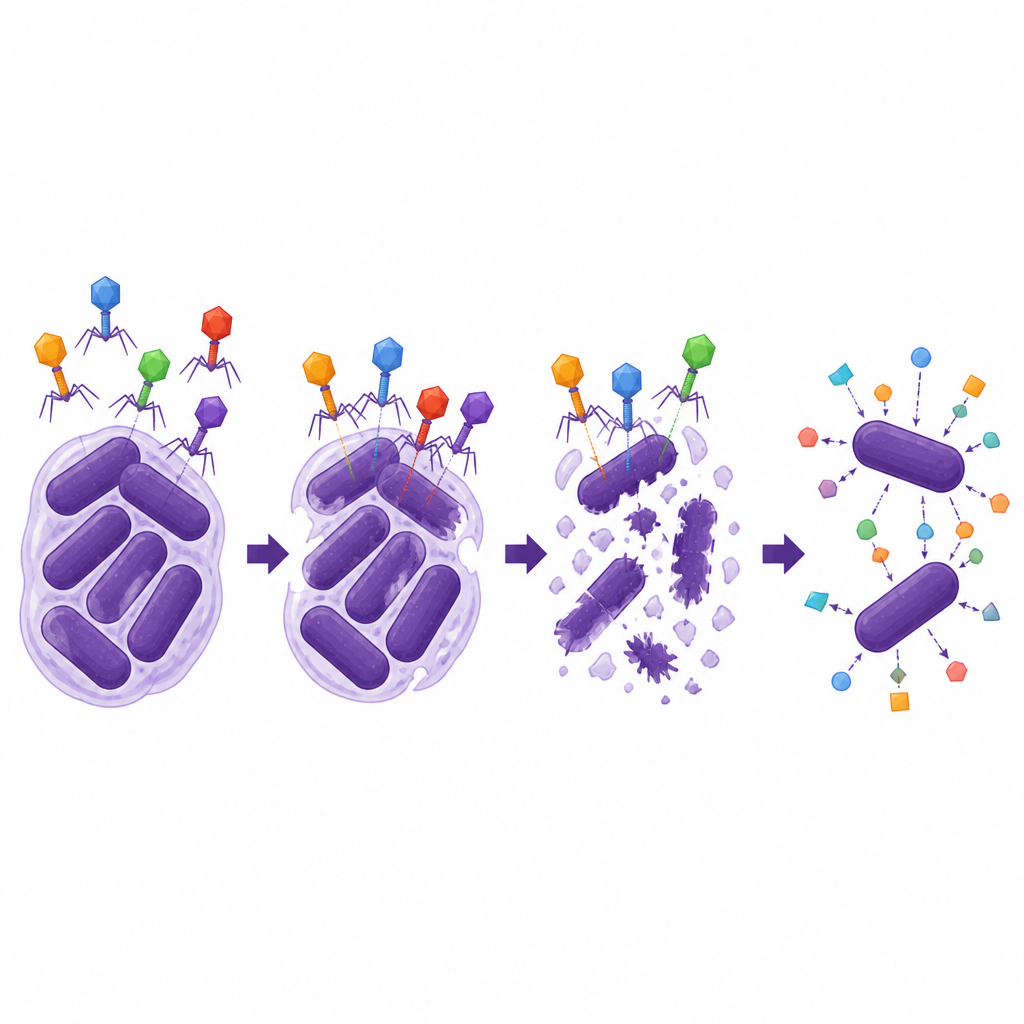
训练病毒识别新靶标
由于单一噬菌体的狭窄宿主范围限制了其临床用途,团队尝试促使ΦAb1-SL1和ΦAb1-SL2去感染另一株最初耐受的菌株Abau2。通过反复与该新宿主共同培养噬菌体,他们最终获得了一个适应性变体ΦAb2-SL1,能够攻击原始菌株和新菌株,尽管在Abau2上增殖效率较低。基因组测序仅发现了少量遗传微调,主要集中在可能接触细菌表面的尾部蛋白,这些细微变化扩展了噬菌体的宿主范围,同时保留了其基本生长特性和稳定性。
这对未来治疗意味着什么
简言之,这项工作表明,可对高风险医院病原体有用的噬菌体可以从污水中获取,利用现代基因工具筛选和“净化”,然后训练以识别额外的细菌靶标。其中一种噬菌体在与先进抗生素cefiderocol联用时表现尤为出色,这提示此类组合可能恢复抗药菌株对药物的敏感性,而不必完全替代抗生素。尽管这些实验仅在试管中完成且噬菌体仍只感染有限的菌株集合,但这里所描述的逐步工作流程指向建立区域性噬菌体库的前景,临床医生在治疗多药耐药A. baumannii及未来其他顽固细菌时可加以利用。
引用: Nicolosi, A., Bonanno Ferraro, G., Brandtner, D. et al. Integrated wet lab and in silico discovery and characterization of bacteriophages with antibiotic synergy against multidrug resistant Acinetobacter baumannii. Sci Rep 16, 15091 (2026). https://doi.org/10.1038/s41598-026-44506-4
关键词: 噬菌体疗法, 鲍曼不动杆菌, 抗生素协同, 头孢他啶类(cefiderocol), 多药耐药