Clear Sky Science · es
Descubrimiento y caracterización integrados, en laboratorio húmedo e in silico, de bacteriófagos con sinergia antibiótica frente a Acinetobacter baumannii multirresistente
Viejos enemigos germinales consiguen nuevos aliados
Las infecciones resistentes a fármacos hacen que tratamientos hospitalarios que antes eran rutinarios resulten mucho más arriesgados, especialmente cuando el causante es Acinetobacter baumannii, una bacteria difícil de eliminar que resiste muchos antibióticos. Este estudio explora cómo los virus que atacan bacterias, llamados bacteriófagos o fagos, pueden encontrarse en aguas residuales corrientes y luego ser entrenados y probados en el laboratorio y por computadora para trabajar junto con antibióticos modernos contra estos persistentes gérmenes hospitalarios. 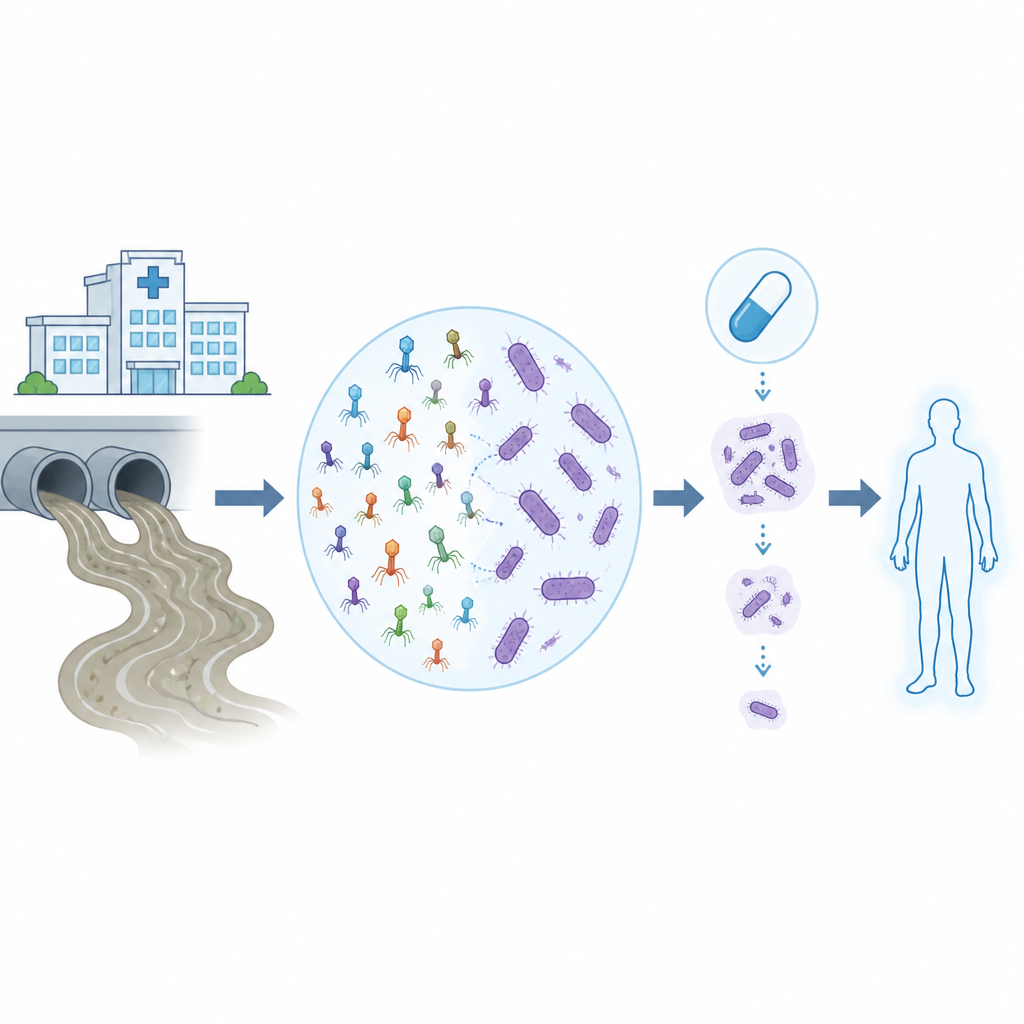
Buscando virus útiles en aguas residuales
Los investigadores empezaron por reunir un panel de veinte cepas de A. baumannii multirresistentes recogidas en hospitales de toda Italia. Usando huellas genéticas, eligieron dos cepas representativas como cebo para fagos y las expusieron a aguas residuales sin tratar, un reservorio natural rico en estos virus. Solo una cepa, denominada Abau1, permitió aislar fagos que producían manchas claras de bacterias muertas en placas de laboratorio. La microscopía electrónica mostró cuatro fagos relacionados, todos del mismo grupo viral amplio, pero con dos morfologías corporales distintas que apuntan a estilos de vida y comportamientos diferentes.
Separando buenos asesinos de huéspedes silenciosos
No todos los fagos son útiles para terapia, porque algunos tienden a ocultarse silenciosamente dentro del ADN bacteriano en lugar de destruir su hospedador. El equipo secuenció los genomas de los fagos y los comparó con el material genético de la propia bacteria hospedadora. Dos fagos resultaron casi idénticos a fragmentos ya incrustados en el cromosoma de Abau1, lo que significa que eran parásitos derivados del hospedador que podrían cambiar a un modo de vida temperado y silencioso. Los otros dos, llamados ΦAb1-SL1 y ΦAb1-SL2, no mostraron solapamientos con el ADN del hospedador y no portaban genes conocidos de producción de toxinas ni de resistencia a antibióticos, lo que los identifica como fagos líticos puros que rompen y matan de forma fiable a sus objetivos.
Probando fortaleza, alcance y trabajo en equipo con fármacos
Los científicos preguntaron entonces cuán robustos y versátiles eran los dos fagos líticos. Ambos permanecieron infecciosos en un amplio rango de temperaturas y acidez, incluidas condiciones similares a las de partes del cuerpo humano, y se multiplicaron eficientemente una vez dentro de las bacterias. Sin embargo, solo podían infectar un conjunto estrecho de cepas de A. baumannii que compartían un tipo específico de cápsula exterior, lo que subraya cómo los fagos a menudo actúan como sistemas de cerradura y llave. De forma más llamativa, un fago, ΦAb1-SL1, mostró fuerte sinergia con varios antibióticos cefalosporínicos, especialmente con cefiderocol. En pruebas de laboratorio, combinar este fago con dosis bajas de cefiderocol redujo el crecimiento bacteriano mucho más que cualquiera de los tratamientos por separado y disminuyó la dosis de antibiótico necesaria para sacar la cepa del rango de resistencia, mientras que una ayuda parecida no se observó con el carbapenémico meropenem. 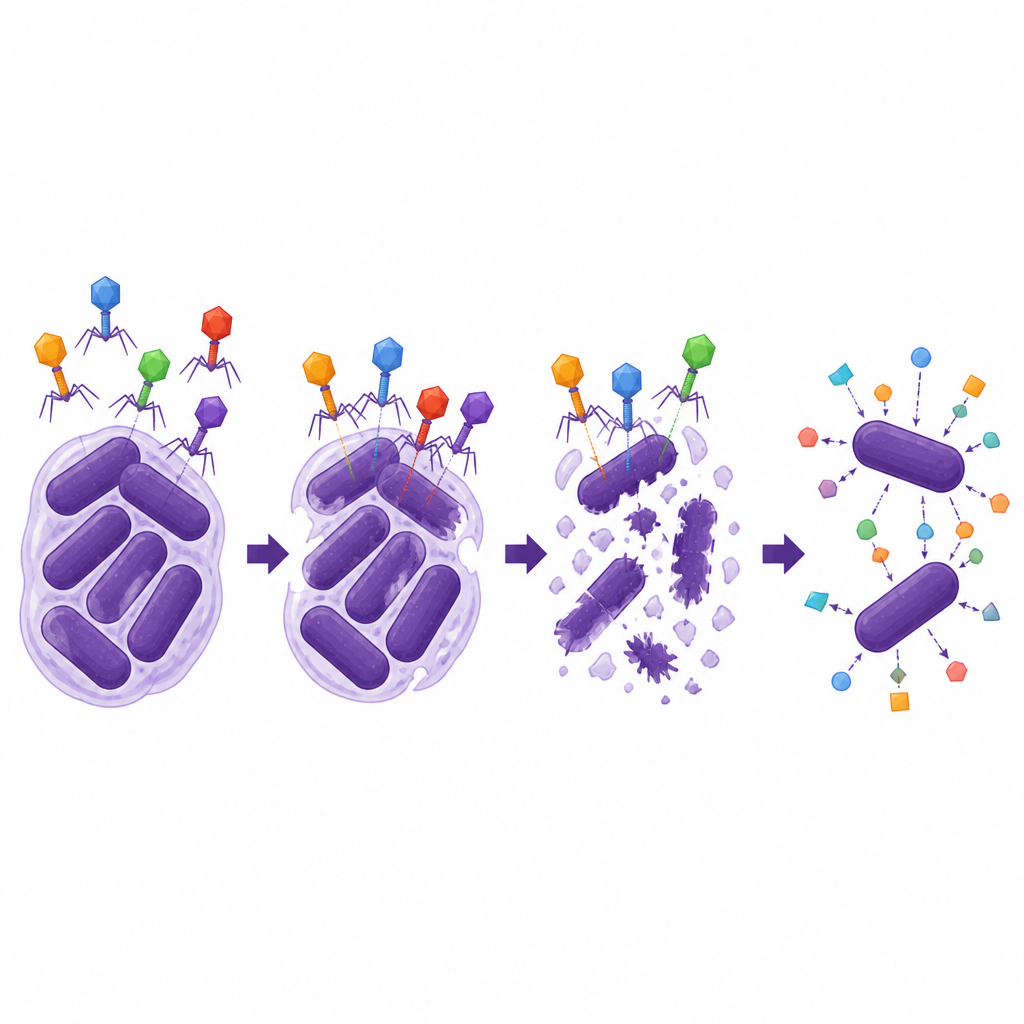
Entrenando un virus para reconocer nuevos objetivos
Dado que el alcance estrecho de un solo fago limita su utilidad médica, el equipo intentó forzar a ΦAb1-SL1 y ΦAb1-SL2 a infectar una segunda cepa inicialmente resistente llamada Abau2. Al cultivar repetidamente los fagos con este nuevo hospedador, finalmente obtuvieron una variante adaptada, ΦAb2-SL1, capaz de atacar tanto la cepa original como la nueva, aunque se multiplicaba menos eficientemente en Abau2. La secuenciación del genoma reveló solo pequeños ajustes genéticos, principalmente en proteínas de la cola que probablemente contactan la superficie bacteriana; sin embargo, estos cambios sutiles ampliaron el rango de hospedadores del fago sin alterar sus características básicas de crecimiento y estabilidad.
Qué significa esto para tratamientos futuros
En términos sencillos, este trabajo muestra que se pueden pescar fagos útiles frente a un germen hospitalario de alto riesgo en aguas residuales, cribarlos y purificarlos con herramientas genéticas modernas y luego entrenarlos para reconocer objetivos bacterianos adicionales. Uno de estos fagos funcionó especialmente bien cuando se combinó con el antibiótico avanzado cefiderocol, lo que sugiere que tales combinaciones podrían restaurar la actividad de los fármacos contra infecciones persistentes en lugar de reemplazar por completo a los antibióticos. Aunque los experimentos se realizaron solo en tubos de ensayo y los fagos siguen infectando un conjunto limitado de cepas, la línea de trabajo paso a paso aquí descrita apunta a la creación de bancos regionales de fagos de los que los clínicos podrían recurrir al tratar A. baumannii multirresistente y, eventualmente, otros difíciles enemigos bacterianos.
Cita: Nicolosi, A., Bonanno Ferraro, G., Brandtner, D. et al. Integrated wet lab and in silico discovery and characterization of bacteriophages with antibiotic synergy against multidrug resistant Acinetobacter baumannii. Sci Rep 16, 15091 (2026). https://doi.org/10.1038/s41598-026-44506-4
Palabras clave: terapia con bacteriófagos, Acinetobacter baumannii, sinergia antibiótica, cefiderocol, multirresistencia