Clear Sky Science · ru
Интегрированное мокрое лабораторное и in silico обнаружение и характеристика бактериофагов с антибактериальным синергизмом против мультирезистентного Acinetobacter baumannii
Старые враги получают новых союзников
Инфекции, устойчивые к препаратам, делают когда-то рутинные больничные процедуры гораздо более рискованными, особенно если виновником является Acinetobacter baumannii — трудноубиваемая бактерия, которая противостоит многим антибиотикам. В этом исследовании изучается, как вирусы, поедающие бактерии — бактериофаги или фаги — могут быть найдены в обычных сточных водах, затем отобраны и протестированы в лаборатории и с помощью вычислительных методов для совместной работы с современными антибиотиками против этих упрямых госпитальных патогенов. 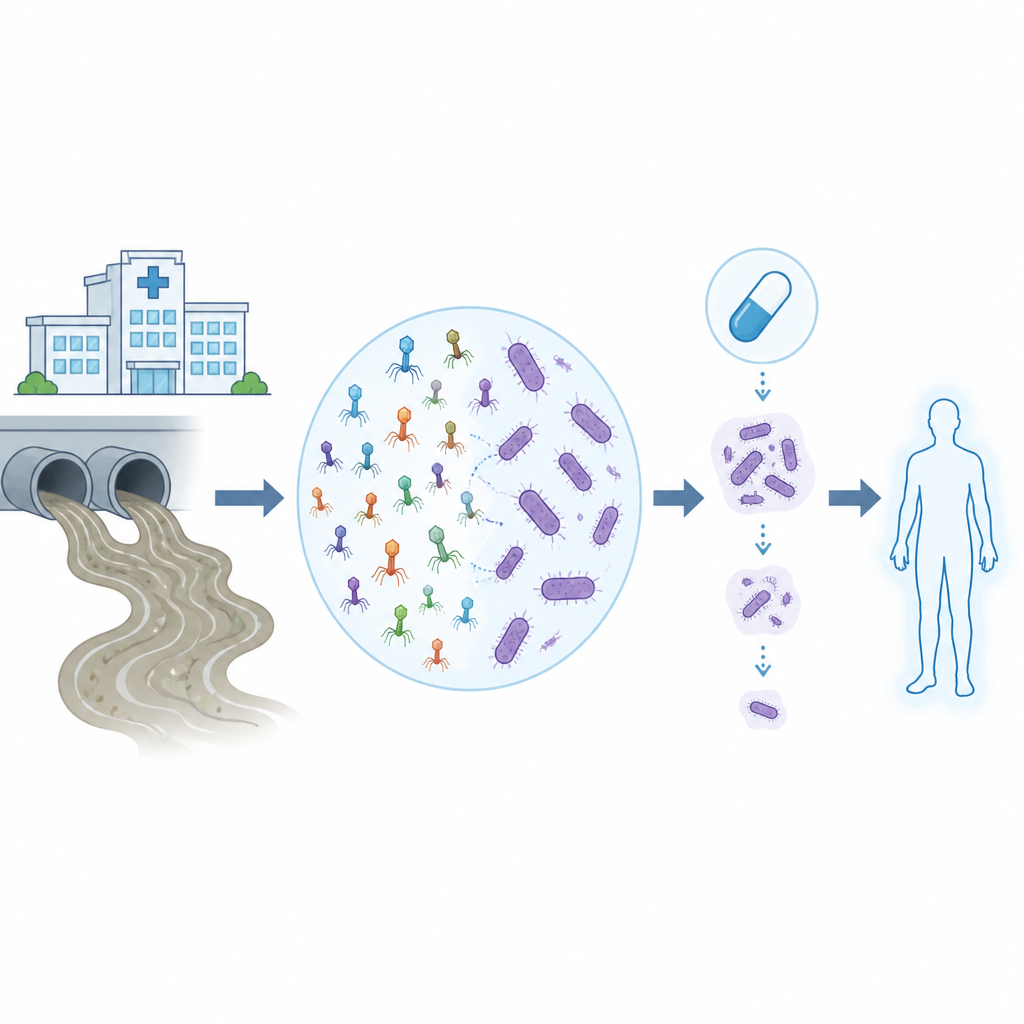
Поиск полезных вирусов в сточных водах
Исследователи начали со сборки панели из двадцати штаммов мультирезистентного A. baumannii, выделенных в больницах по всей Италии. Используя генетические отпечатки, они выбрали два представительских штамма в качестве приманки для фагов и подвергли их воздействию неочищенных сточных вод — богатого природного резервуара этих вирусов. Только один штамм, названный Abau1, дал фаги, которые образовывали на агарных планшетах четкие зоны гибели бактерий. Электронная микроскопия показала четыре родственных фага, все из одной широкой вирусной группы, но с двумя различными формами строения, что намекало на разные образ жизни и поведение.
Отбор эффективных убийц и тихих попутчиков
Не каждый фаг пригоден для терапии, потому что некоторые склонны скрываться внутри бактериальной ДНК вместо того, чтобы разрушать хозяина. Команда секвенировала геномы фагов и сравнила их с генетическим материалом хозяина-бактерии. Два фага оказались почти идентичны фрагментам, уже встроенным в хромосому Abau1, то есть были производными хозяина попутчиками, которые могут переходить в тихий, темперный образ жизни. Другие два, названные ΦAb1-SL1 и ΦAb1-SL2, не показали совпадений с ДНК хозяина и не несли известных генов, отвечающих за токсичность или устойчивость к антибиотикам, что обозначило их как чисто литические фаги, которые надёжно разрывают и убивают свои цели.
Оценка прочности, диапазона и командной работы с препаратами
Учёные затем проверили, насколько устойчивы и универсальны два литических фага. Оба сохраняли инфекциозность в широком диапазоне температур и кислотности, включая условия, похожие на встречающиеся в частях человеческого тела, и эффективно размножались внутри бактерий. Однако они могли инфицировать только узкий набор штаммов A. baumannii, которые имели специфический тип внешней капсулы, что подчёркивает, как фаги часто ведут себя по принципу «ключ — замок». Наиболее примечательно, что один фаг, ΦAb1-SL1, проявил сильный синергизм с несколькими цефалоспориновыми антибиотиками, особенно с цефидероколом. В лабораторных тестах сочетание этого фага с низкими дозами цефидерокола значительно сильнее подавляло рост бактерий, чем любое из лечений по отдельности, и снижало дозу антибиотика, необходимую для вывода штамма из зоны резистентности, в то время как подобного эффекта не наблюдалось с карбапенемом меропенемом. 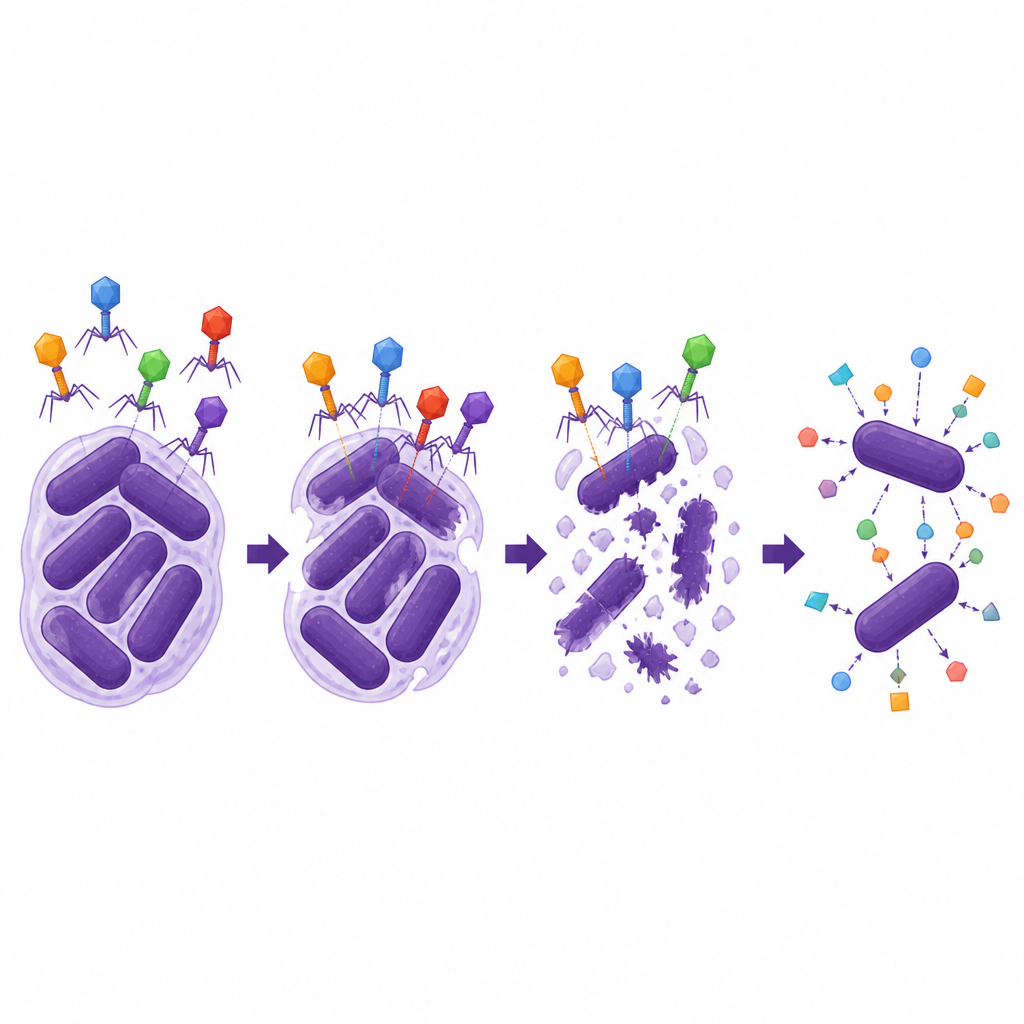
Обучение вируса распознавать новые мишени
Поскольку узкий диапазон одного фага ограничивает его клиническую полезность, команда попыталась заставить ΦAb1-SL1 и ΦAb1-SL2 инфицировать второй, изначально резистентный штамм, названный Abau2. Повторно выращивая фаги с этим новым хозяином, они в конце концов получили адаптированный вариант, ΦAb2-SL1, который мог атаковать как исходный, так и новый штамм, хотя размножался менее эффективно на Abau2. Секвенирование геномов показало лишь небольшие генетические изменения, главным образом в белках хвоста, которые вероятно контактируют с поверхностью бактерии; эти тонкие изменения расширили спектр хозяев фага, сохранив при этом его основные характеристики роста и стабильность.
Что это значит для будущего лечения
Проще говоря, эта работа показывает, что полезные фаги против высокоопасного госпитального патогена можно извлечь из сточных вод, отскринить и очистить с помощью современных генетических инструментов, а затем натренировать на распознавание дополнительных бактериальных мишеней. Один из этих фагов оказался особенно эффективен в сочетании с продвинутым антибиотиком цефидероколом, что намекает на то, что такие комбинации могут восстановить активность лекарств против упрямых инфекций, а не полностью заменить антибиотики. Хотя эксперименты проводились только в пробирках и фаги по‑прежнему инфицируют ограниченный набор штаммов, описанная поэтапная схема указывает путь к созданию региональных банков фагов, к которым клиницисты могли бы обращаться при лечении мультирезистентного A. baumannii и, в перспективе, других трудных бактериальных врагов.
Цитирование: Nicolosi, A., Bonanno Ferraro, G., Brandtner, D. et al. Integrated wet lab and in silico discovery and characterization of bacteriophages with antibiotic synergy against multidrug resistant Acinetobacter baumannii. Sci Rep 16, 15091 (2026). https://doi.org/10.1038/s41598-026-44506-4
Ключевые слова: терапия бактериофагами, Acinetobacter baumannii, антибиотический синергизм, цефидерокол, мультирезистентность