Clear Sky Science · nl
Geïntegreerde natte-lab- en in silico-ontdekking en karakterisering van bacteriofagen met antibioticasynergie tegen multiresistente Acinetobacter baumannii
Oude ziekteverwekkers krijgen nieuwe bondgenoten
Infecties met resistentie tegen medicijnen maken vroeger routineuze ziekenhuisbehandelingen veel risicovoller, vooral wanneer de veroorzaker Acinetobacter baumannii is, een moeilijk te doden bacterie die vele antibiotica negeert. Deze studie onderzoekt hoe virussen die op bacteriën parasiteren, bacteriofagen of fagen genoemd, in gewoon afvalwater gevonden en vervolgens in het laboratorium en op computers getraind en getest kunnen worden om samen te werken met moderne antibiotica tegen deze hardnekkige ziekenhuiskiemen. 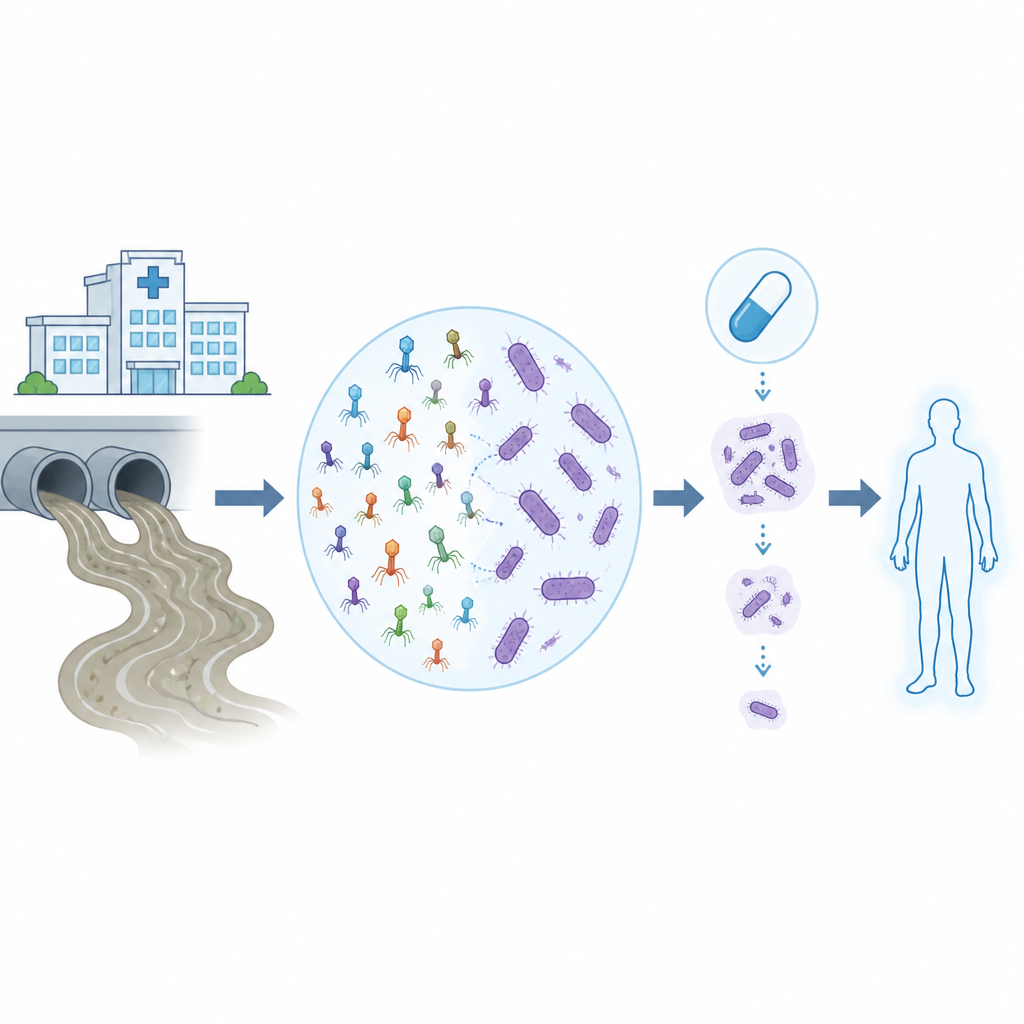
Op zoek naar nuttige virussen in afvalwater
De onderzoekers begonnen met het samenstellen van een panel van twintig multiresistente A. baumannii-stammen die in ziekenhuizen door heel Italië waren verzameld. Met behulp van genetische vingerafdrukken kozen ze twee representatieve stammen als lokaas voor fagen en stelden ze bloot aan onverwerkt afvalwater, een rijke natuurlijke bron van deze virussen. Slechts één stam, genoemd Abau1, leverde fagen op die duidelijke vlekken van gedode bacteriën op petrischalen vormden. Elektronenmicroscopie toonde vier verwante fagen, alle behorend tot dezelfde brede virusgroep, maar met twee verschillende lichaamsvormen die op verschillende levenswijzen en gedragingen wezen.
Goede doders scheiden van stille meelopers
Niet elke faag is bruikbaar voor therapie, omdat sommige de neiging hebben zich stil te verbergen in bacterieel DNA in plaats van hun gastheer te vernietigen. Het team sequeende de faaggenomen en vergeleek ze met het genetische materiaal van de gastheerbacterie. Twee fagen bleken bijna identiek te zijn aan stukken die al in het Abau1-chromosoom ingebed waren, wat betekent dat het gastheerafgeleide meelopers waren die konden overschakelen naar een rustige, temperante levensstijl. De andere twee, genoemd ΦAb1-SL1 en ΦAb1-SL2, toonden geen overlap met gastheer-DNA en droegen geen bekende genen voor toxineproductie of antibioticumresistentie, wat hen markeerde als puur lytische fagen die hun doelen betrouwbaar laten barsten en doden.
Kracht, reikwijdte en samenwerking met medicijnen testen
De wetenschappers stelden vervolgens vast hoe robuust en veelzijdig de twee lytische fagen waren. Beide bleven infectieus bij een breed scala aan temperaturen en zuurgraad, inclusief omstandigheden vergelijkbaar met die in delen van het menselijk lichaam, en ze vermenigvuldigden zich efficiënt eenmaal binnen bacteriën. Ze konden echter slechts een beperkte set A. baumannii-stammen infecteren die een specifiek type buitenste kapsel deelden, wat benadrukt hoe fagen vaak als sleutel-en-slotsystemen werken. Het meest opvallend toonde één faag, ΦAb1-SL1, sterke synergie met meerdere cefalosporine-antibiotica, vooral cefiderocol. In laboratoriumtesten verminderde de combinatie van deze faag met lage doses cefiderocol de bacteriegroei veel sterker dan elke behandeling afzonderlijk en verlaagde het de benodigde antibioticadosis om de stam uit het resistente bereik te halen, terwijl dergelijke hulp niet werd gezien met het carbapenem-middel meropenem. 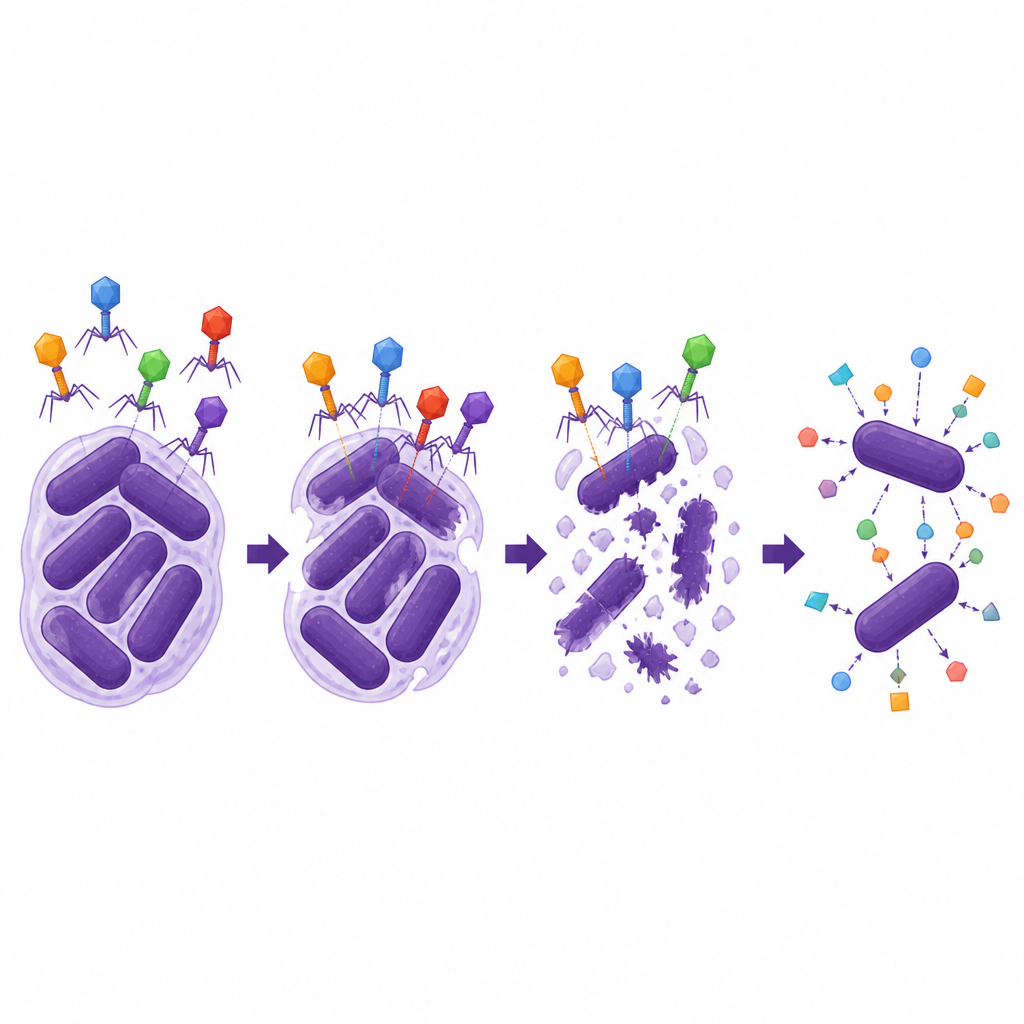
Een virus trainen om nieuwe doelen te herkennen
Aangezien de beperkte reikwijdte van een enkele faag de medische bruikbaarheid beperkt, probeerde het team ΦAb1-SL1 en ΦAb1-SL2 ertoe te brengen een tweede, aanvankelijk resistente stam genaamd Abau2 te infecteren. Door de fagen herhaaldelijk met deze nieuwe gast te laten groeien, verkregen ze uiteindelijk een aangepaste variant, ΦAb2-SL1, die zowel de oorspronkelijke als de nieuwe stam kon aanvallen, hoewel hij zich minder efficiënt vermeerderde op Abau2. Genoomsequencing toonde slechts kleine genetische aanpassingen, voornamelijk in staartproteïnen die waarschijnlijk het bacteriële oppervlak aanraken, maar deze subtiele veranderingen vergrootten het gastbereik van de faag terwijl de basisgroei-eigenschappen en stabiliteit behouden bleven.
Wat dit betekent voor toekomstige behandelingen
In eenvoudige bewoordingen toont dit werk aan dat nuttige fagen tegen een hoogrisico-ziektekiem uit het ziekenhuis gevonden kunnen worden in afvalwater, gescreend en gezuiverd met moderne genetische hulpmiddelen, en vervolgens getraind om extra bacteriële doelen te herkennen. Een van deze fagen werkte bijzonder goed in combinatie met het geavanceerde antibioticum cefiderocol, wat suggereert dat dergelijke combinaties de werkzaamheid van medicijnen tegen hardnekkige infecties zouden kunnen herstellen in plaats van antibiotica volledig te vervangen. Hoewel de experimenten alleen in reageerbuizen zijn uitgevoerd en de fagen nog steeds slechts een beperkte reeks stammen infecteren, wijst de stapsgewijze pijplijn die hier wordt beschreven op het opbouwen van regionale faagbanken waar clinici uit kunnen putten bij de behandeling van multiresistente A. baumannii en uiteindelijk ook andere moeilijk te bestrijden bacteriën.
Bronvermelding: Nicolosi, A., Bonanno Ferraro, G., Brandtner, D. et al. Integrated wet lab and in silico discovery and characterization of bacteriophages with antibiotic synergy against multidrug resistant Acinetobacter baumannii. Sci Rep 16, 15091 (2026). https://doi.org/10.1038/s41598-026-44506-4
Trefwoorden: bacteriofaagtherapie, Acinetobacter baumannii, antibioticasynergie, cefiderocol, multidrugresistentie