Clear Sky Science · pl
Zintegrowane laboratorium mokre i odkrycia in silico oraz charakterystyka bakteriofagów wykazujących synergizm z antybiotykami przeciwko wielolekowo opornemu Acinetobacter baumannii
Stare wrogie zarazki zyskują nowych sojuszników
Infekcje oporne na leki sprawiają, że kiedyś rutynowe zabiegi szpitalne stają się znacznie bardziej ryzykowne, szczególnie gdy sprawcą jest Acinetobacter baumannii — trudna do zwalczenia bakteria, która „odrzuca” wiele antybiotyków. W tym badaniu zbadano, jak wirusy pasożytujące na bakteriach, zwane bakteriofagami lub fagami, można znaleźć w codziennych ściekach, a następnie wytrenować i przetestować w laboratorium oraz za pomocą narzędzi komputerowych, aby współdziałały z nowoczesnymi antybiotykami przeciwko tym uparcie utrzymującym się szpitalnym zarazkom. 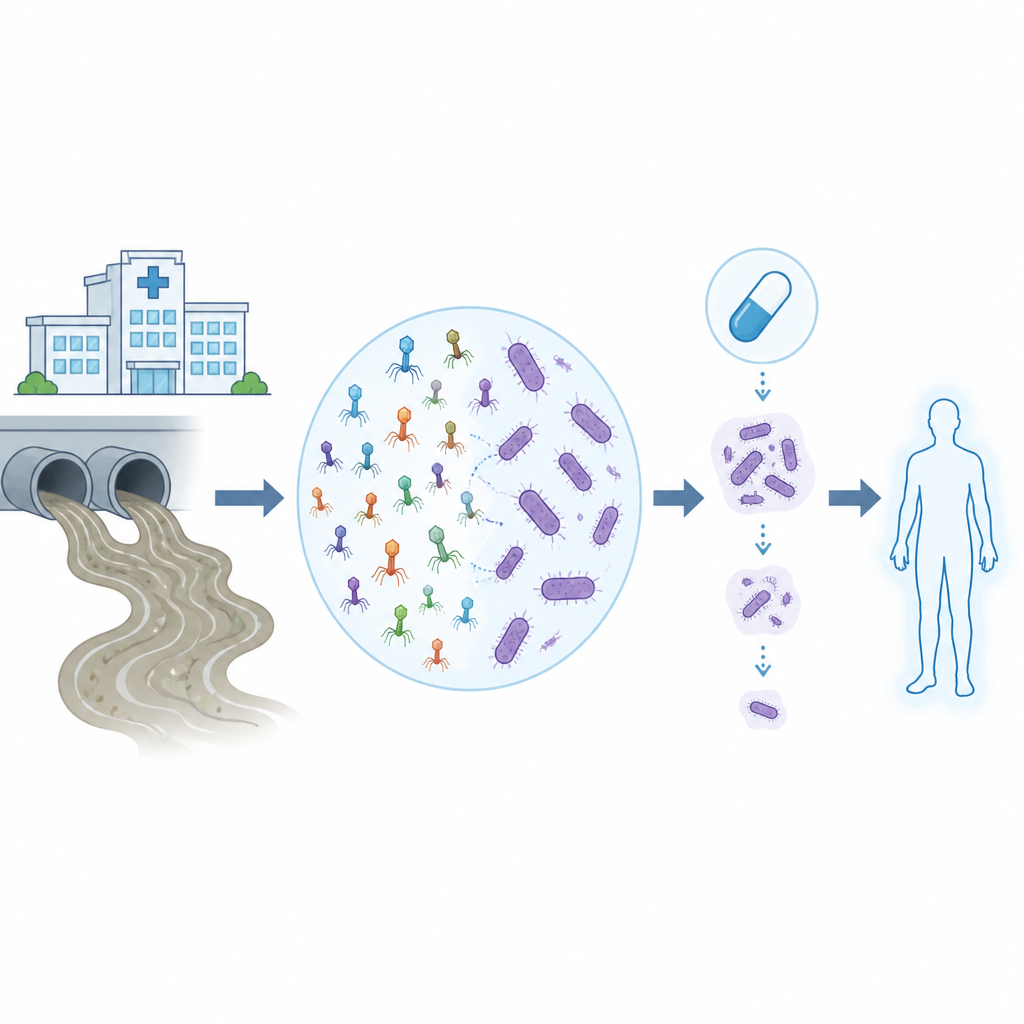
Polowanie na przydatne wirusy w ściekach
Naukowcy zaczęli od skompletowania panelu dwudziestu szczepów wielolekowo opornych A. baumannii zebranych ze szpitali w całych Włoszech. Na podstawie genetycznych odcisków palców wybrali dwa reprezentatywne szczepy jako przynętę dla fagów i wystawili je na działanie nieoczyszczonych ścieków, bogatego naturalnego rezerwuaru tych wirusów. Tylko jeden szczep, nazwany Abau1, dał fagii tworzące wyraźne ogniska martwych bakterii na płytkach hodowlanych. Mikroskopia elektronowa ukazała cztery spokrewnione fagii, wszystkie z tej samej szerokiej grupy wirusowej, ale o dwóch odmiennych kształtach budowy, co sugerowało różne style życia i zachowania.
Oddzielanie dobrych zabójców od cichych pasażerów
Niekoniecznie każdy fag nadaje się do terapii, ponieważ niektóre mają skłonność do ukrywania się w DNA bakterii zamiast niszczenia gospodarza. Zespół zsekwencjonował genom fagów i porównał je z materiałem genetycznym gospodarza. Dwa fagii okazały się niemal identyczne z fragmentami już wbudowanymi w chromosom Abau1, co oznaczało, że były pochodzenia bakteryjnego — pasażerami, które mogą przejść w cichy, temperowany tryb życia. Pozostałe dwa, nazwane ΦAb1-SL1 i ΦAb1-SL2, nie wykazywały nakładania się z DNA gospodarza i nie niosły znanych genów toksyn ani oporności na antybiotyki, co klasyfikowało je jako fagii lityczne, które niezawodnie powodują lizę i zabijają swoje cele.
Testowanie siły, zasięgu i współpracy z lekami
Następnie naukowcy sprawdzili, jak wytrzymałe i wszechstronne są te dwa lityczne fagii. Oba pozostawały zakaźne w szerokim zakresie temperatur i kwasowości, w tym w warunkach podobnych do niektórych środowisk w ludzkim ciele, i efektywnie mnożyły się po wejściu do bakterii. Mogły jednak zakażać jedynie wąski zestaw szczepów A. baumannii, które miały ten sam typ zewnętrznej otoczki, podkreślając, że fagii często działają jak system zamek i klucz. Najbardziej uderzające było to, że jeden fag, ΦAb1-SL1, wykazał silny synergizm z kilkoma antybiotykami z grupy cefalosporyn, zwłaszcza z cefiderokolem. W testach laboratoryjnych połączenie tego faga z niskimi dawkami cefiderokolu hamowało wzrost bakterii znacznie bardziej niż każde z tych działań osobno i obniżało dawkę antybiotyku potrzebną, aby wyprowadzić szczep z zakresu oporności, podczas gdy podobnego wzmocnienia nie zaobserwowano z karbapenemem meropenemem. 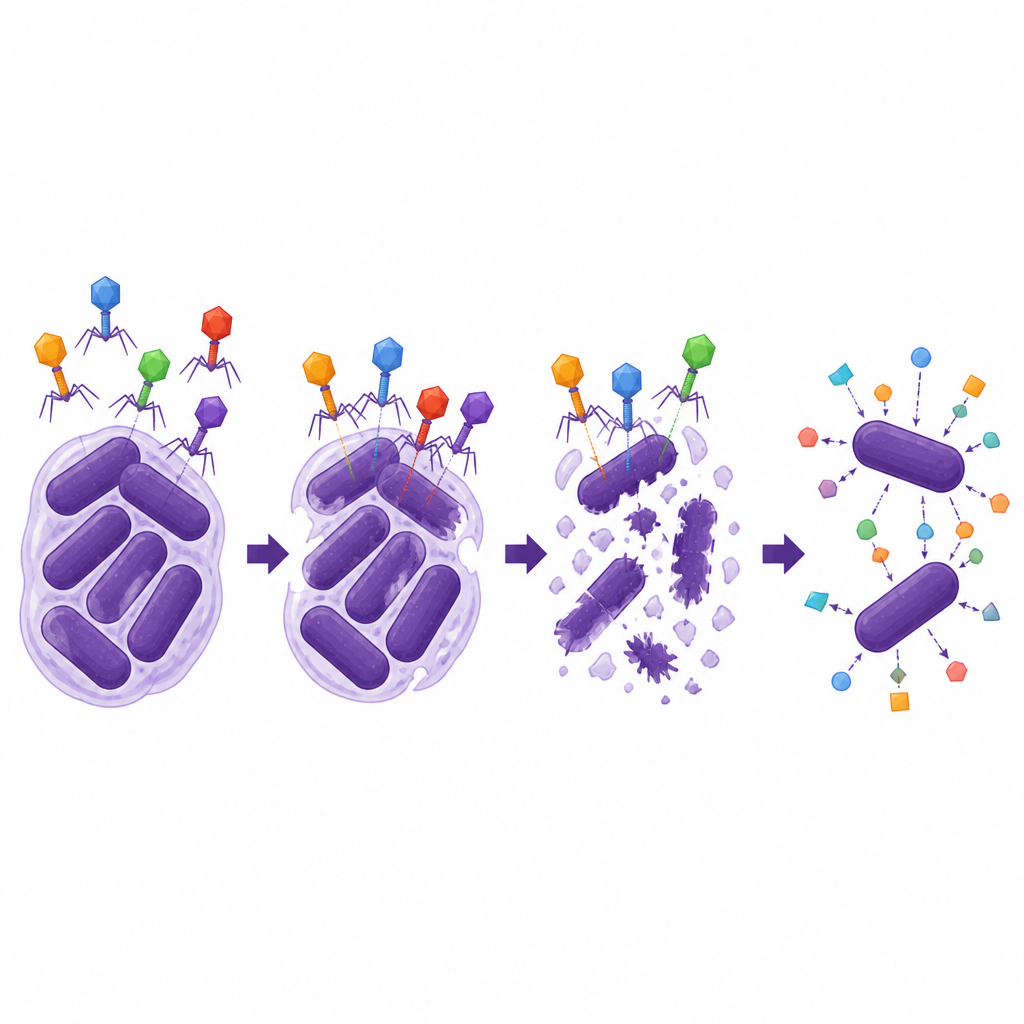
Trenowanie wirusa do rozpoznawania nowych celów
Z uwagi na to, że wąski zasięg pojedynczego faga ogranicza jego zastosowanie medyczne, zespół próbował wymusić, by ΦAb1-SL1 i ΦAb1-SL2 zakażały drugi, początkowo oporny szczep nazwany Abau2. Poprzez wielokrotne namnażanie fagów razem z nowym gospodarzem uzyskano w końcu zaadaptowany wariant, ΦAb2-SL1, który potrafił atakować zarówno szczep oryginalny, jak i nowy, chociaż rozmnażał się mniej efektywnie na Abau2. Sekwencjonowanie genomu wykazało jedynie niewielkie korekty genetyczne, głównie w białkach ogonkowych prawdopodobnie stykających się z powierzchnią bakterii, jednak te subtelne zmiany rozszerzyły zakres gospodarzy faga przy zachowaniu jego podstawowych cech wzrostu i stabilności.
Co to oznacza dla przyszłych terapii
Mówiąc prosto, ta praca pokazuje, że przydatne fagii przeciwko groźnemu szpitalnemu patogenowi można wyłowić ze ścieków, przesiewać i oczyszczać za pomocą nowoczesnych narzędzi genetycznych, a następnie trenować, by rozpoznawały dodatkowe cele bakteryjne. Jeden z tych fagów działał szczególnie dobrze w połączeniu z zaawansowanym antybiotykiem cefiderokolem, co sugeruje, że takie kombinacje mogłyby przywrócić skuteczność leków przeciw uporczywym zakażeniom, zamiast całkowicie zastępować antybiotyki. Chociaż eksperymenty przeprowadzono jedynie w probówkach, a fagii nadal zakażają ograniczony zestaw szczepów, opisana tu krok po kroku procedura wskazuje na możliwość budowy regionalnych banków fagów, z których klinicyści mogliby korzystać przy leczeniu wielolekowo opornego A. baumannii, a ostatecznie także innych trudnych przeciwników bakteryjnych.
Cytowanie: Nicolosi, A., Bonanno Ferraro, G., Brandtner, D. et al. Integrated wet lab and in silico discovery and characterization of bacteriophages with antibiotic synergy against multidrug resistant Acinetobacter baumannii. Sci Rep 16, 15091 (2026). https://doi.org/10.1038/s41598-026-44506-4
Słowa kluczowe: terapia bakteriofagowa, Acinetobacter baumannii, synergia antybiotyków, cefiderokol, wielolekowa oporność