Clear Sky Science · sv
Integrerad våt-labb- och in silico-upptäckt och karakterisering av bakteriofager med antibiotikasynergi mot multiresistent Acinetobacter baumannii
Gamla bakteriefiender får nya allierade
Infektioner med läkemedelsresistenta bakterier gör tidigare rutinmässiga sjukhusbehandlingar mycket riskablare, särskilt när boven är Acinetobacter baumannii, en svårutrotad bakterie som motstår många antibiotika. Denna studie utforskar hur virus som angriper bakterier, kallade bakteriofager eller fager, kan hittas i vanligt avloppsvatten och därefter tränas och testas i laboratorium och på dator för att samverka med moderna antibiotika mot dessa svårbekämpade sjukhusbakterier. 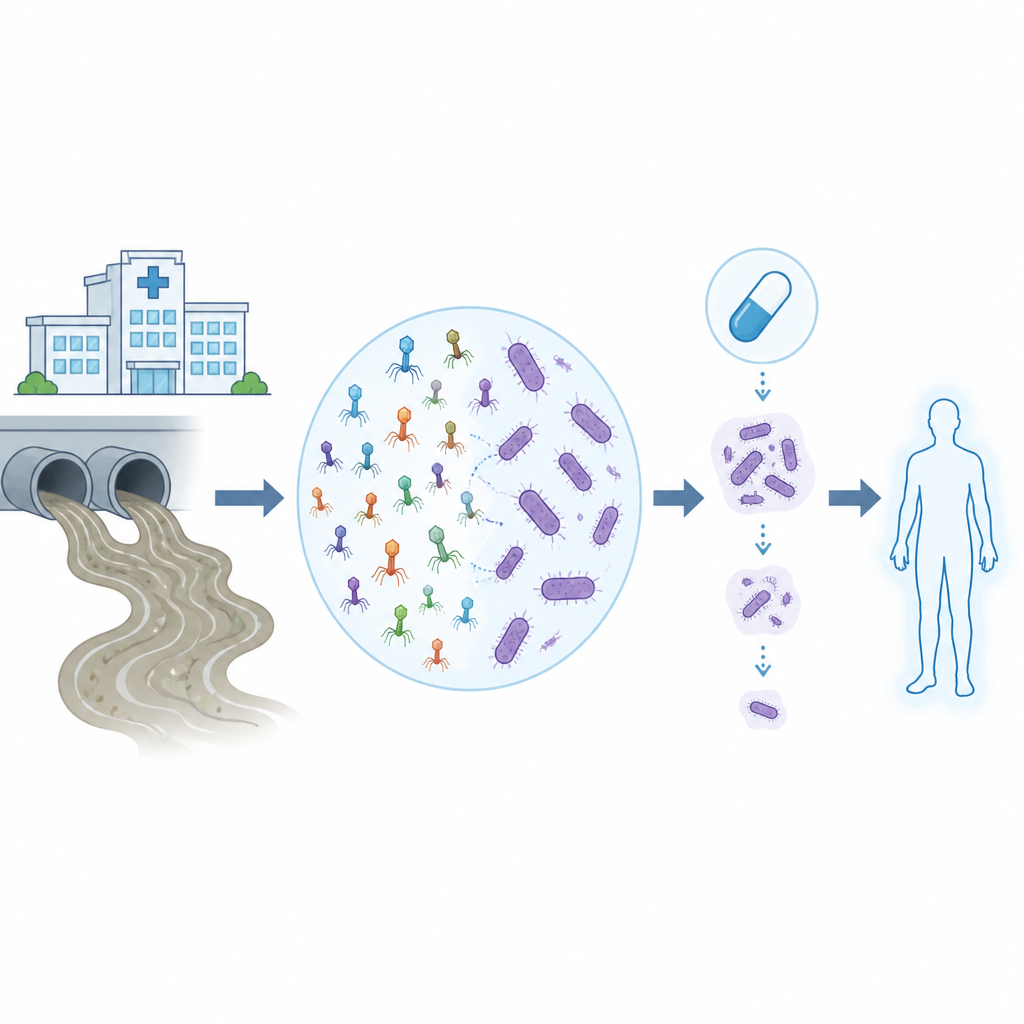
Jakt på användbara virus i avloppsvatten
Forskarna började med att samla en panel av tjugo multiresistenta A. baumannii-stammar insamlade från sjukhus runt om i Italien. Med hjälp av genetiska fingeravtryck valde de två representativa stammar som lockbete för fager och exponerade dem för obehandlat avloppsvatten, en rik naturlig reservoar för dessa virus. Endast en stam, kallad Abau1, gav upphov till fager som skapade tydliga zoner med döda bakterier på agarplattor. Elektronmikroskopi visade fyra närbesläktade fager, alla från samma breda virusgrupp, men med två olika kroppsformer som antyder skilda livsstilar och beteenden.
Sortera skickliga mördare från tysta hitchhikers
Inte alla fager är användbara för terapi, eftersom vissa tenderar att gömma sig tyst inne i bakteriens DNA istället för att förstöra sin värd. Gruppen sekvenserade fagernas genom och jämförde dem med värdbakteriens eget genetiska material. Två fager visade sig vara nästan identiska med bitar som redan var inbäddade i Abau1-kromosomen, vilket betyder att de var värdderiverade hitchhikers som kan gå över till en tyst, temperat livsstil. De andra två, kallade ΦAb1-SL1 och ΦAb1-SL2, visade ingen överlappning med värd-DNA och bar inga kända gener för toxiner eller antibiotikaresistens, vilket markerar dem som rent lytiska fager som pålitligt lyserar och dödar sina mål.
Test av styrka, räckvidd och samverkan med läkemedel
Forskarna frågade sig sedan hur robusta och mångsidiga de två lytiska fagerna var. Båda förblev infektiösa över ett brett spektrum av temperaturer och pH, inklusive förhållanden liknande de som finns i delar av människokroppen, och de multiplicerade effektivt inne i bakterier. Däremot kunde de bara infektera en snäv uppsättning A. baumannii-stammar som delade en specifik yttre kapseltyp, vilket understryker hur fager ofta fungerar som lås-och-nyckel-system. Mest anmärkningsvärt visade en fag, ΦAb1-SL1, stark synergi med flera cefalosporinantibiotika, särskilt cefiderocol. I laboratorietester gav kombinationen av denna fag med låga doser cefiderocol en mycket större minskning av bakteriell tillväxt än någon av behandlingarna ensamt och sänkte den antibiotikados som krävdes för att flytta stammen ur det resistenta intervallet, medan sådan hjälp inte sågs med karbapenemet meropenem. 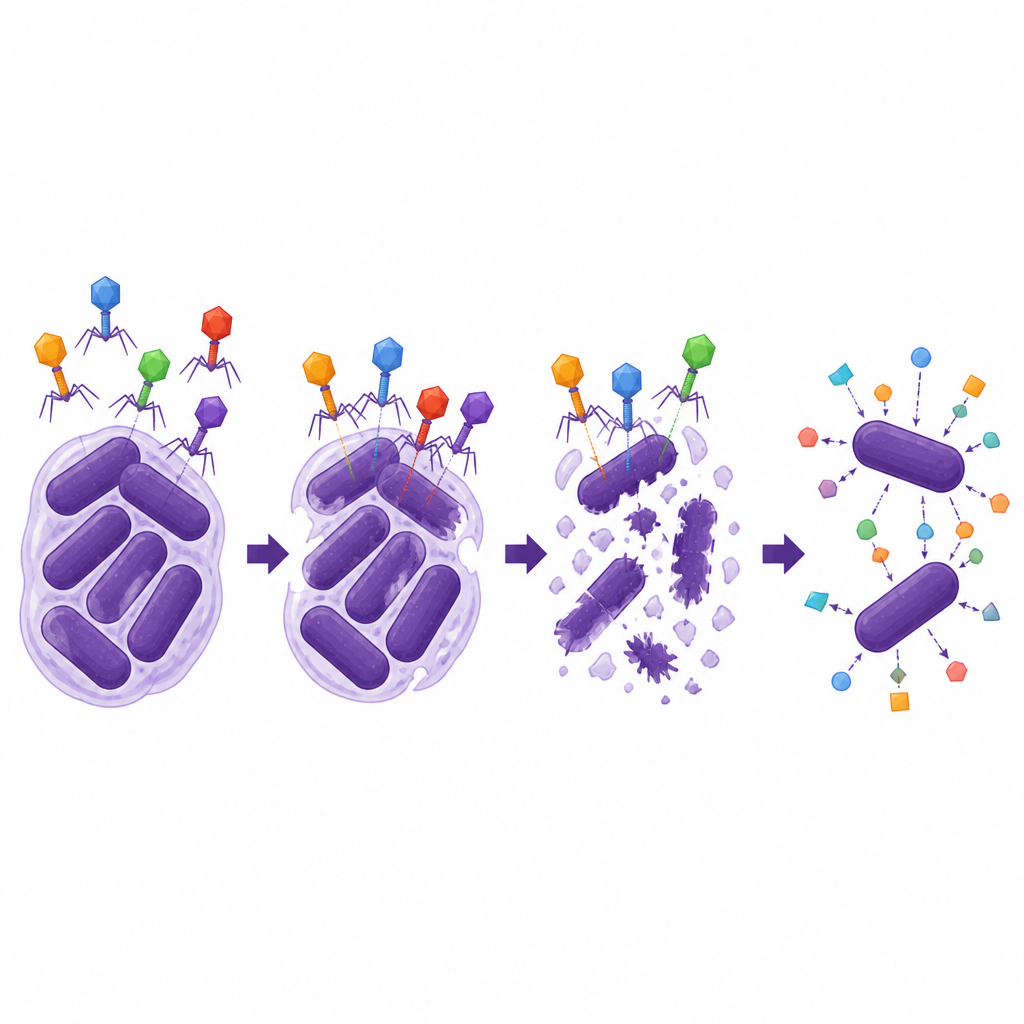
Träna ett virus att känna igen nya mål
Eftersom en enskild fags snäva räckvidd begränsar dess medicinska användbarhet försökte teamet få ΦAb1-SL1 och ΦAb1-SL2 att infektera en andra, initialt resistent stam kallad Abau2. Genom att upprepade gånger odla fager tillsammans med denna nya värd frambringade de så småningom en anpassad variant, ΦAb2-SL1, som kunde angripa både den ursprungliga och den nya stammen, även om den multiplicerade mindre effektivt på Abau2. Genomsekvensering avslöjade endast små genetiska förändringar, främst i svansproteiner som sannolikt rör vid bakterieytan, men dessa subtila förändringar utvidgade fagets värdintervall samtidigt som dess grundläggande växtegenskaper och stabilitet bevarades.
Vad detta betyder för framtida behandlingar
Enkelt uttryckt visar detta arbete att användbara fager mot en högrisk sjukhusbakterie kan fiskas upp från avloppsvatten, screenas och renas med moderna genetiska verktyg och därefter tränas att känna igen ytterligare bakteriella mål. En av dessa fager fungerade särskilt väl i kombination med det avancerade antibiotikumet cefiderocol, vilket antyder att sådana kombinationer kan återuppliva läkemedelseffektivitet mot envisa infektioner i stället för att helt ersätta antibiotika. Även om experimenten utfördes endast i provrör och fagerna fortfarande infekterar ett begränsat antal stammar, pekar den stegvisa pipeline som beskrivs här mot att bygga regionala fagbanker som kliniker kan dra nytta av vid behandling av multiresistent A. baumannii och så småningom andra svåra bakteriella fiender.
Citering: Nicolosi, A., Bonanno Ferraro, G., Brandtner, D. et al. Integrated wet lab and in silico discovery and characterization of bacteriophages with antibiotic synergy against multidrug resistant Acinetobacter baumannii. Sci Rep 16, 15091 (2026). https://doi.org/10.1038/s41598-026-44506-4
Nyckelord: bakteriofagterapi, Acinetobacter baumannii, antibiotikasynergi, cefiderocol, multiresistens