Clear Sky Science · ar
اكتشاف وتوصيف متكامل بالمختبر الرطب والمحاكاة الحاسوبية للفاجات البكتيرية وتكاملها مع مضادات حيوية ضد Acinetobacter baumannii المقاومة للعديد من الأدوية
أعداء قدامى يكتسبون حلفاء جدد
تجعل العدوى المقاومة للأدوية علاجات المستشفيات التي كانت روتينية سابقًا أكثر خطورة، لا سيما عندما يكون المسبب هو Acinetobacter baumannii، بكتيريا يصعب قتلها وتقاوم العديد من المضادات الحيوية. تستكشف هذه الدراسة كيف أن الفيروسات التي تفترس البكتيريا، المعروفة بالفاجات البكتيرية أو الفاجات، يمكن العثور عليها في مياه الصرف اليومية ثم تهيئتها واختبارها في المختبر وعلى الحواسيب للعمل جنبًا إلى جنب مع المضادات الحيوية الحديثة ضد هذه الجراثيم المستعصية في المستشفيات. 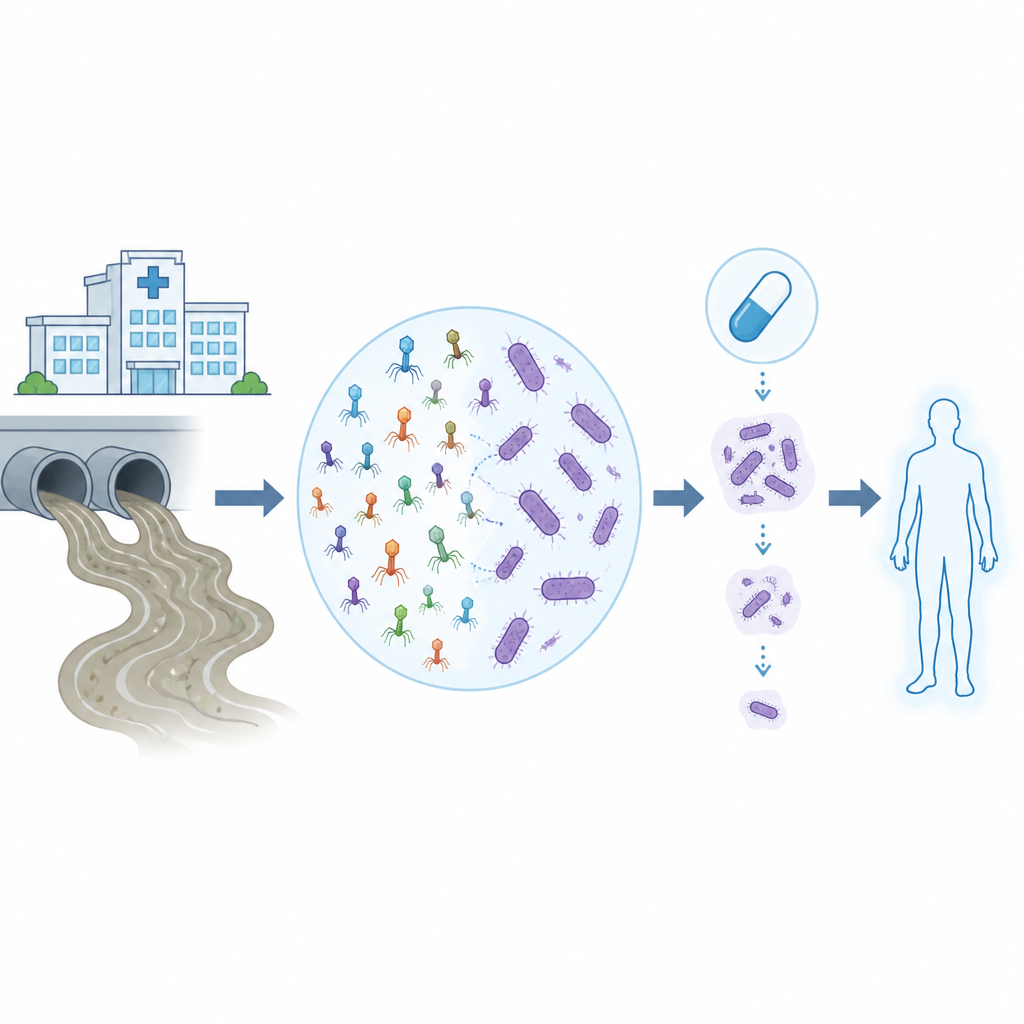
البحث عن الفيروسات المفيدة في مياه الصرف
بدأ الباحثون بتجميع لوحة مكوّنة من عشرين سلالة من A. baumannii المقاومة متعددة الأدوية، جمعت من مستشفيات عبر إيطاليا. باستخدام بصمات جينية، اختاروا سلالتين تمثيليتين كطُعم للفاجات وعرضوهما على مياه صرف غير معالجة، وهي مستودع طبيعي غني بهذه الفيروسات. نجحت سلالة واحدة فقط، المسماة Abau1، في إنتاج فاجات شكلت بقعًا واضحة من البكتيريا الميتة على أطباق المختبر. أظهرت الميكروسكوبات الإلكترونية أربع فاجات مرتبطة، كلها من نفس المجموعة الفيروسية الواسعة، لكن ذات شكلين جسديين مميزين يشيران إلى أنماط حياة وسلوك مختلفة.
فرز القاتلين الفعّالين من الركاب الصامتين
ليست كل الفاجات مفيدة للعلاج، لأن بعضها يميل إلى الاختباء بهدوء داخل الحمض النووي البكتيري بدلًا من تدمير المضيف. قام الفريق بتسلسل جينومات الفاجات ومقارنتها مع المادة الوراثية للبكتيريا المضيفة. تبين أن فاجتين تكاد تكونان متطابقتين مع قطع مُدمجة بالفعل في كروموسوم Abau1، ما يعني أنهما ركاب مشتقون من المضيف ويمكن أن تتحولا إلى نمط هادئ معتدل. أما الفاجتان الأخريان، المسماة ΦAb1-SL1 وΦAb1-SL2، فلم تُظهر أي تداخل مع حمض المضيف الحامل ولم تحمل أي جينات معروفة لإنتاج سموم أو مقاومة مضادات حيوية، مما يصنفهما على أنهما فاجات ليتية بحتة تفجر بخاصية القتل بثبات.
اختبار القوة والنطاق والتعاون مع الأدوية
سأل العلماء بعد ذلك عن مدى متانة وتعدد استخدامات الفاجات الليتية الاثنتين. بقيتا معديتين عبر نطاق واسع من درجات الحرارة والحموضة، بما في ذلك ظروف مشابهة لأجزاء من جسم الإنسان، وتكاثرتا بكفاءة داخل البكتيريا. ومع ذلك، استطاعتا إصابة مجموعة ضيقة فقط من سلالات A. baumannii التي تشترك في نوع غلاف خارجي محدد، ما يؤكد كيف تعمل الفاجات غالبًا كأنظمة قفل ومفتاح. والأبرز أن إحدى الفاجات، ΦAb1-SL1، أظهرت تآزرًا قويًا مع عدة مضادات من فئة السيفالوسبورينات، وخصوصًا مع سيفيدرول. في اختبارات المختبر، أدى الجمع بين هذه الفاجة وجرعات منخفضة من سيفيدرول إلى خفض نمو البكتيريا إلى حد أكبر بكثير من أي من العلاجين بمفرده وخفض جرعة المضاد الحيوي المطلوبة لإخراج السلالة من نطاق المقاومة، بينما لم يُرَ هذا التأثير المساعد مع الكاربابينيم ميروبينيم. 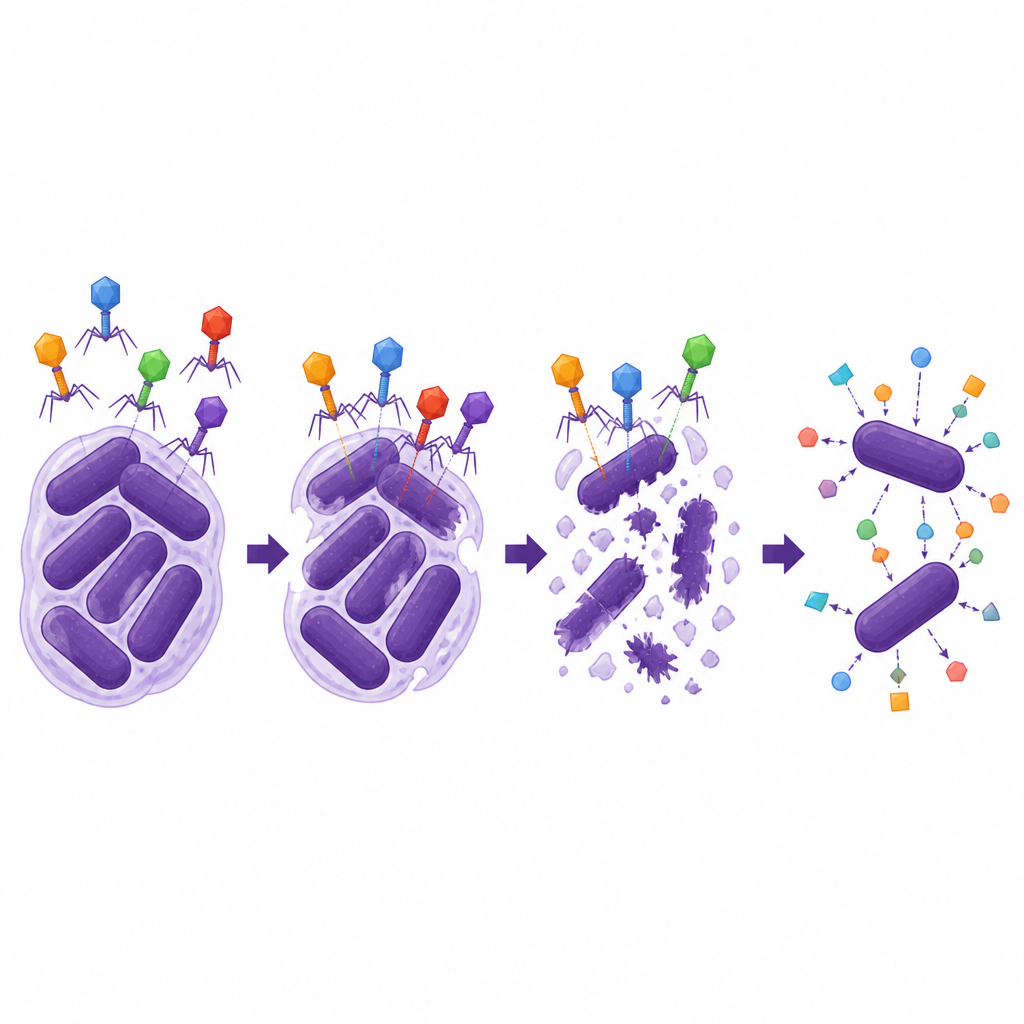
تدريب فيروس ليتعرف على أهداف جديدة
نظرًا لأن نطاق إصابة فاجة واحدة الضيق يقيد فائدتها الطبية، حاول الفريق دفع ΦAb1-SL1 وΦAb1-SL2 لمهاجمة سلالة ثانية كانت مقاومة مبدئيًا مسماة Abau2. عبر نمو الفاجات بشكل متكرر مع هذا المضيف الجديد، حصلوا في النهاية على متغير متكيف، ΦAb2-SL1، استطاع مهاجمة كل من السلالة الأصلية والسلالة الجديدة، رغم أنه تكاثر بكفاءة أقل على Abau2. كشف تسلسل الجينوم عن تعديلات جينية طفيفة فقط، معظمها في بروتينات الذيل التي تتلامس على الأرجح مع سطح البكتيريا، ومع ذلك وسعت هذه التغييرات الدقيقة نطاق مضيف الفاجة مع الحفاظ على خصائص نموها الأساسية واستقرارها.
ماذا يعني هذا للعلاجات المستقبلية
بعبارة بسيطة، تُظهر هذه الدراسة أنه يمكن صيد فاجات مفيدة ضد جرثوم مستشفيات عالية الخطورة من مياه الصرف، وفحصها وتنقيتها باستخدام أدوات جينية حديثة، ثم تدريبها للتعرف على أهداف بكتيرية إضافية. عملت إحدى هذه الفاجات بشكل جيد بشكل خاص عندما اقترنت بالمضاد الحيوي المتقدم سيفيدرول، مما يوحي بأن مثل هذه التركيبات قد تعيد فعالية الأدوية ضد العدوى العنيدة بدلاً من استبدال المضادات الحيوية تمامًا. وعلى الرغم من أن التجارب أُجريت في أنابيب اختبار فقط وأن الفاجات لا تزال تصيب مجموعة محدودة من السلالات، فإن خط الأنابيب خطوة بخطوة الموضح هنا يشير إلى إمكانية بناء بنوك إقليمية من الفاجات يمكن للأطباء الاستعانة بها عند علاج A. baumannii المقاومة متعددة الأدوية، وفي نهاية المطاف، ضد أعداء بكتيرية عنيدة أخرى.
الاستشهاد: Nicolosi, A., Bonanno Ferraro, G., Brandtner, D. et al. Integrated wet lab and in silico discovery and characterization of bacteriophages with antibiotic synergy against multidrug resistant Acinetobacter baumannii. Sci Rep 16, 15091 (2026). https://doi.org/10.1038/s41598-026-44506-4
الكلمات المفتاحية: علاج بالفاجات البكتيرية, Acinetobacter baumannii, تآزر المضادات الحيوية, سيفيدرول, المقاومة متعددة الأدوية