Clear Sky Science · de
Integrierte Nassenlabor- und In-silico-Entdeckung und Charakterisierung von Bakteriophagen mit antibiotischer Synergie gegen multiresistente Acinetobacter baumannii
Alte Keimfeinde gewinnen neue Verbündete
Arzneimittelresistente Infektionen machen einst routinemäßige Krankenhausbehandlungen deutlich riskanter, insbesondere wenn der Erreger Acinetobacter baumannii ist – ein schwer zu beseitigendes Bakterium, das vielen Antibiotika trotzt. Diese Studie untersucht, wie Viren, die Bakterien befallen – sogenannte Bakteriophagen oder Phagen – im alltäglichen Abwasser zu finden sind und dann im Labor sowie mithilfe von Computeranalysen trainiert und getestet werden können, um zusammen mit modernen Antibiotika gegen diese hartnäckigen Krankenhauskeime zu wirken. 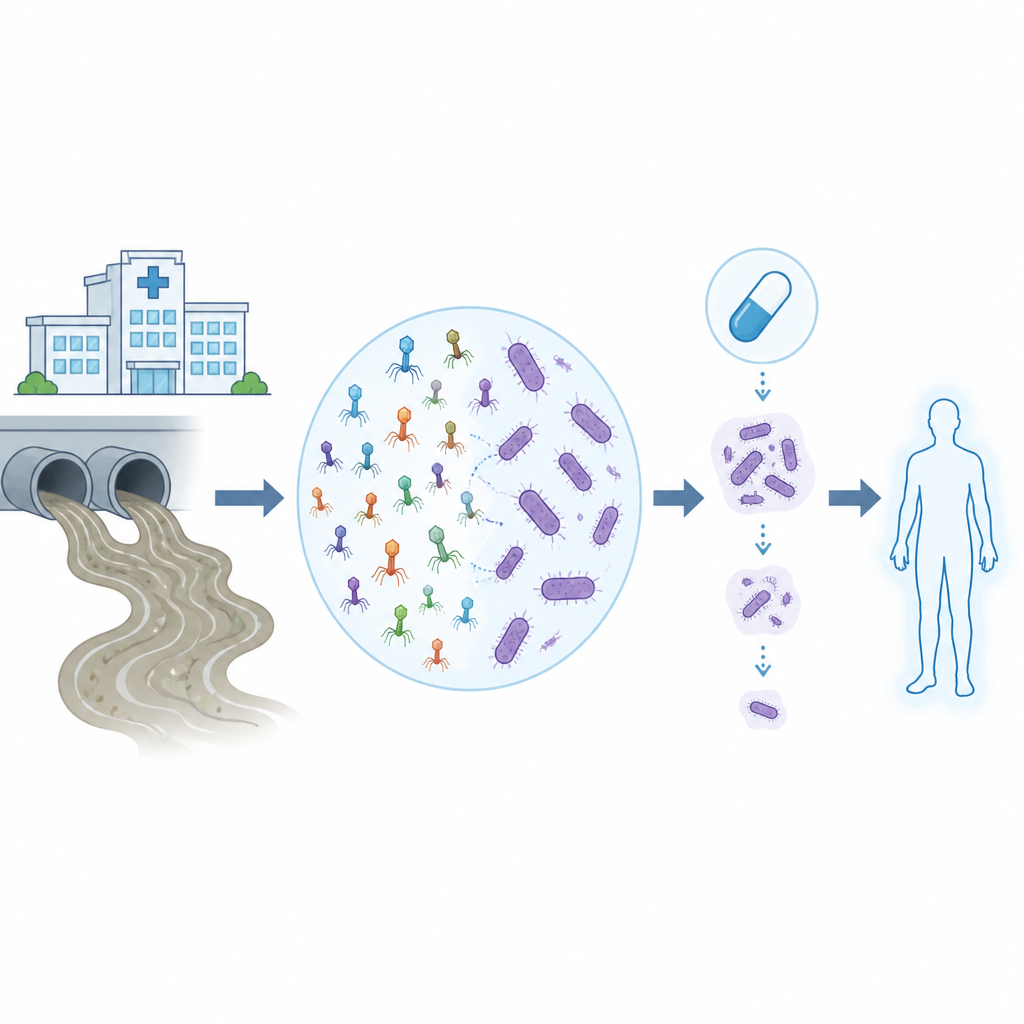
Auf der Suche nach nützlichen Viren im Abwasser
Die Forschenden begannen damit, ein Panel von zwanzig multiresistenten A. baumannii-Stämmen zusammenzustellen, die aus Krankenhäusern in ganz Italien stammten. Mithilfe genetischer Fingerabdrücke wählten sie zwei repräsentative Stämme als Köder für Phagen aus und setzten diese unbehandeltem Abwasser aus, einem reichen natürlichen Reservoir dieser Viren. Nur ein Stamm, genannt Abau1, ergab Phagen, die auf Agarplatten klare Flecken toter Bakterien hinterließen. Elektronenmikroskopie zeigte vier verwandte Phagen, alle aus derselben großen Virengruppe, jedoch mit zwei unterschiedlichen Körperformen, die auf verschiedene Lebensweisen und Verhaltensweisen hindeuten.
Ermittlung guter Killer versus stiller Mitbewohner
Nicht jeder Phage ist für eine Therapie geeignet, weil einige dazu neigen, sich still im bakteriellen Genom einzunisten, anstatt ihren Wirt zu zerstören. Das Team sequenzierte die Phagen-Genome und verglich sie mit dem genetischen Material des Wirtsbakteriums. Zwei Phagen waren nahezu identisch mit Sequenzen, die bereits im Chromosom von Abau1 eingebettet waren, was darauf hinweist, dass es sich um wirtseigene Mitbewohner handelt, die in einen ruhigen, temperaten Lebenszyklus übergehen können. Die anderen beiden, bezeichnet als ΦAb1-SL1 und ΦAb1-SL2, zeigten keine Überschneidung mit der Wirts-DNA und trugen keine bekannten Gene für Toxinproduktion oder Antibiotikaresistenz—ein Hinweis darauf, dass es sich um strikt lytische Phagen handelt, die zuverlässig aufplatzen und ihre Ziele töten.
Prüfung von Stärke, Reichweite und Zusammenarbeit mit Medikamenten
Die Forschenden fragten dann, wie robust und vielseitig die beiden lytischen Phagen sind. Beide blieben über einen weiten Bereich von Temperaturen und pH-Werten infektiös, einschließlich Bedingungen, die in Teilen des menschlichen Körpers vorkommen, und sie vermehrten sich effizient, sobald sie in Bakterien gelangten. Sie konnten jedoch nur eine enge Gruppe von A. baumannii-Stämmen infizieren, die einen bestimmten äußeren Kapseltyp teilten, was unterstreicht, wie Phagen oft wie Schloss-und-Schlüssel-Systeme funktionieren. Am auffälligsten zeigte ein Phage, ΦAb1-SL1, starke Synergie mit mehreren Cephalosporin-Antibiotika, insbesondere mit Cefiderocol. In Labortests reduzierte die Kombination dieses Phagen mit niedrigen Cefiderocol-Dosen das Bakterienwachstum deutlich stärker als jede Behandlung allein und senkte die benötigte Antibiotikadosis, um den Stamm aus dem Resistenzbereich zu bringen, während eine solche Unterstützung beim Carbapenem-Medikament Meropenem nicht beobachtet wurde. 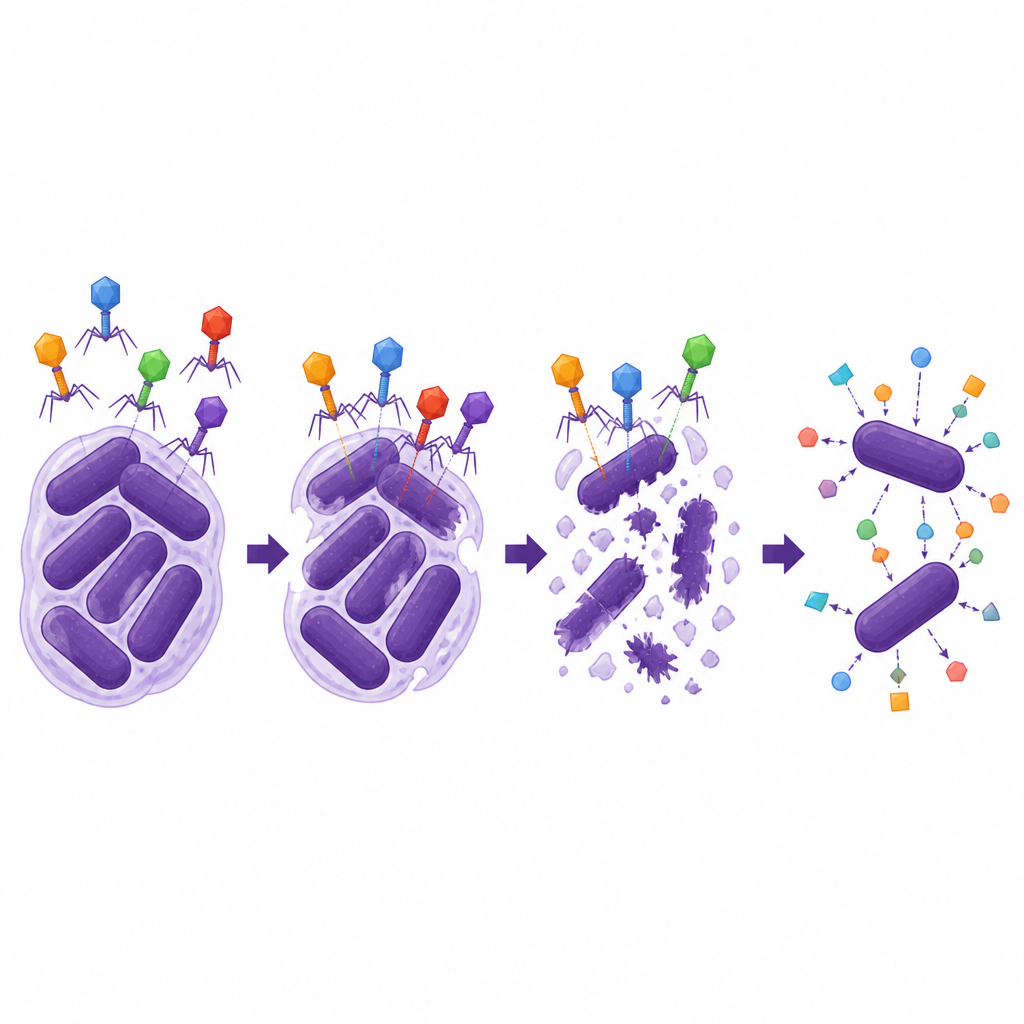
Training eines Virus, neue Ziele zu erkennen
Da die enge Wirtsreichweite eines einzelnen Phagen seine medizinische Nützlichkeit einschränkt, versuchte das Team, ΦAb1-SL1 und ΦAb1-SL2 dazu zu bringen, einen zweiten, zunächst resistenten Stamm namens Abau2 zu infizieren. Durch wiederholtes Passagieren der Phagen mit diesem neuen Wirt erzielten sie schließlich eine adaptierte Variante, ΦAb2-SL1, die sowohl den ursprünglichen als auch den neuen Stamm angreifen konnte, obwohl sie sich auf Abau2 weniger effizient vermehrte. Die Genomsequenzierung zeigte nur kleine genetische Anpassungen, hauptsächlich in Schwanzproteinen, die wahrscheinlich die bakterielle Oberfläche berühren; dennoch erweiterten diese subtilen Veränderungen die Wirtsreichweite des Phagen, während seine grundlegenden Wachstumsmerkmale und seine Stabilität erhalten blieben.
Was das für künftige Behandlungen bedeutet
Vereinfacht gesagt zeigt diese Arbeit, dass nützliche Phagen gegen einen hochriskanten Krankenhauskeim aus Abwasser gefischt, mithilfe moderner genetischer Werkzeuge geprüft und gereinigt und dann darauf trainiert werden können, zusätzliche bakterielle Ziele zu erkennen. Einer dieser Phagen funktionierte besonders gut in Kombination mit dem fortschrittlichen Antibiotikum Cefiderocol, was nahelegt, dass solche Kombinationen die Wirksamkeit von Medikamenten gegen hartnäckige Infektionen wiederbeleben könnten, anstatt Antibiotika vollständig zu ersetzen. Obwohl die Experimente nur in Reagenzgläsern durchgeführt wurden und die Phagen weiterhin nur eine begrenzte Anzahl von Stämmen infizieren, zeigt die hier skizzierte Schritt-für-Schritt-Pipeline den Weg hin zu regionalen Phagenbanken, aus denen Klinikärzte bei der Behandlung multiresistenter A. baumannii-Stämme und schließlich anderer schwerer bakterieller Gegner schöpfen könnten.
Zitation: Nicolosi, A., Bonanno Ferraro, G., Brandtner, D. et al. Integrated wet lab and in silico discovery and characterization of bacteriophages with antibiotic synergy against multidrug resistant Acinetobacter baumannii. Sci Rep 16, 15091 (2026). https://doi.org/10.1038/s41598-026-44506-4
Schlüsselwörter: Bakteriophagen-Therapie, Acinetobacter baumannii, antibiotische Synergie, Cefiderocol, Multiresistenz