Clear Sky Science · it
Scoperta e caratterizzazione integrate in laboratorio e in silico di batteriofagi con sinergia antibiotica contro Acinetobacter baumannii multiresistente
I vecchi nemici germinali guadagnano nuovi alleati
Le infezioni resistenti ai farmaci stanno rendendo trattamenti ospedalieri una volta di routine molto più rischiosi, soprattutto quando il colpevole è Acinetobacter baumannii, un batterio difficile da eliminare che ignora molti antibiotici. Questo studio esplora come i virus che attaccano i batteri, chiamati batteriofagi o fagi, possano essere trovati nelle comuni acque reflue e poi allenati e testati in laboratorio e tramite analisi in silico per collaborare con antibiotici moderni contro questi ostinati germi ospedalieri. 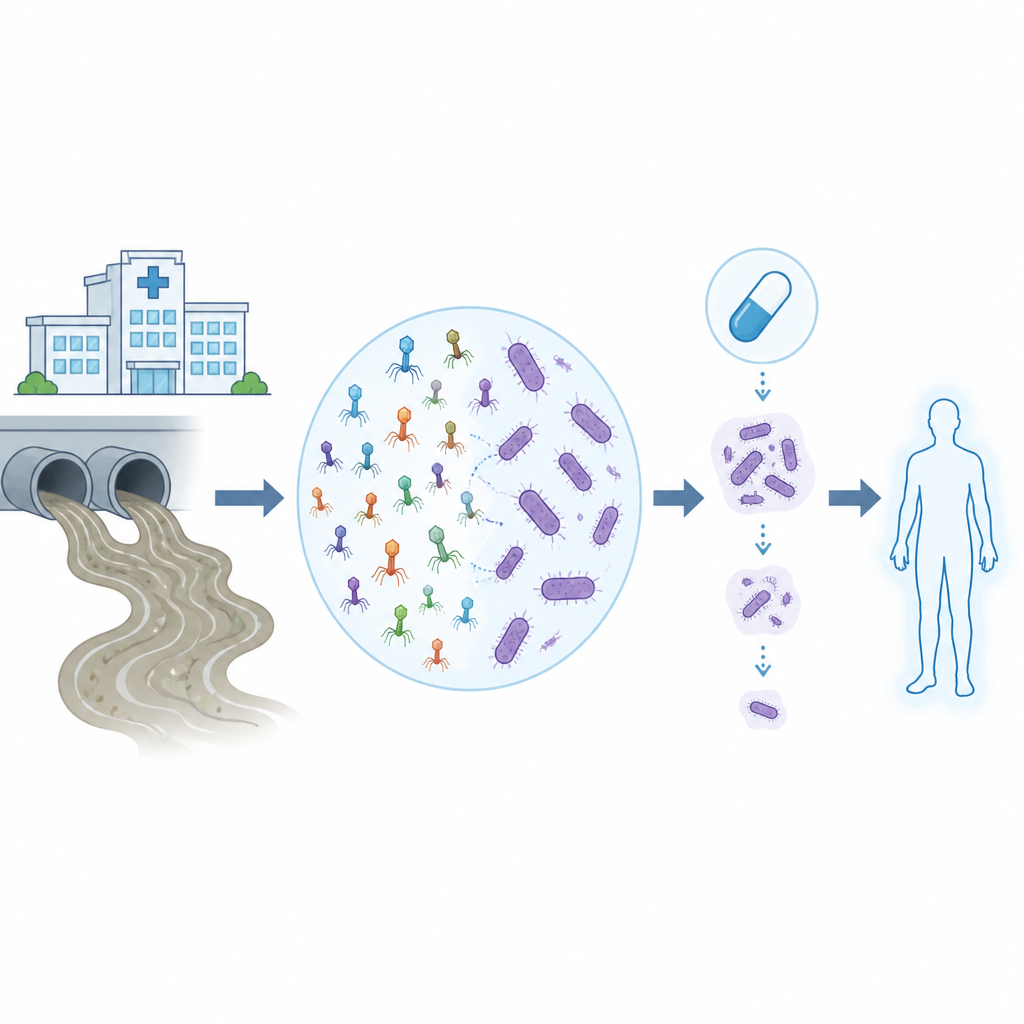
Caccia ai virus utili nelle acque reflue
I ricercatori hanno iniziato assemblando un pannello di venti ceppi di A. baumannii multiresistenti raccolti in ospedali di tutta Italia. Usando impronte genetiche, hanno scelto due ceppi rappresentativi come esca per i fagi ed li hanno esposti ad acque reflue non trattate, un ricco serbatoio naturale di questi virus. Solo un ceppo, chiamato Abau1, ha prodotto fagi che formavano chiare aree di batteri morti sulle piastre di laboratorio. La microscopia elettronica ha mostrato quattro fagi correlati, tutti appartenenti allo stesso ampio gruppo virale, ma con due distinte morfologie corporali che suggerivano diversi stili di vita e comportamenti.
Distinguere i buoni sterminatori dai silenziosi passeggeri
Non tutti i fagi sono utili per la terapia, perché alcuni tendono a nascondersi silenziosamente all’interno del DNA batterico invece di distruggere l’ospite. Il gruppo ha sequenziato i genomi dei fagi e li ha confrontati con il materiale genetico del batterio ospite. Due fagi si sono rivelati quasi identici a frammenti già inseriti nel cromosoma di Abau1, il che significa che derivavano dall’ospite e potevano adottare uno stile di vita temperato e silente. Gli altri due, denominati ΦAb1-SL1 e ΦAb1-SL2, non mostravano sovrapposizioni con il DNA dell’ospite e non portavano geni noti per la produzione di tossine o per la resistenza agli antibiotici, caratterizzandoli come fagi puramente litici che esplodono e uccidono in modo affidabile i loro bersagli.
Valutare forza, portata e collaborazione con i farmaci
Gli scienziati si sono poi chiesti quanto fossero robusti e versatili i due fagi litici. Entrambi sono rimasti infettivi in un’ampia gamma di temperature e valori di pH, incluse condizioni simili a quelle presenti in parti del corpo umano, e si sono moltiplicati in modo efficiente una volta all’interno dei batteri. Tuttavia, potevano infettare solo un ristretto insieme di ceppi di A. baumannii che condividevano un specifico tipo di capsula esterna, sottolineando come i fagi spesso funzionino come sistemi a chiave e serratura. Più sorprendentemente, un fago, ΦAb1-SL1, ha mostrato una forte sinergia con diversi antibiotici cefalosporinici, specialmente il cefiderocol. Nei test di laboratorio, la combinazione di questo fago con basse dosi di cefiderocol riduceva la crescita batterica molto più di ciascun trattamento da solo e abbassava la dose di antibiotico necessaria a spostare il ceppo fuori dall’intervallo di resistenza, mentre un aiuto simile non è stato osservato con il carbapenemico meropenem. 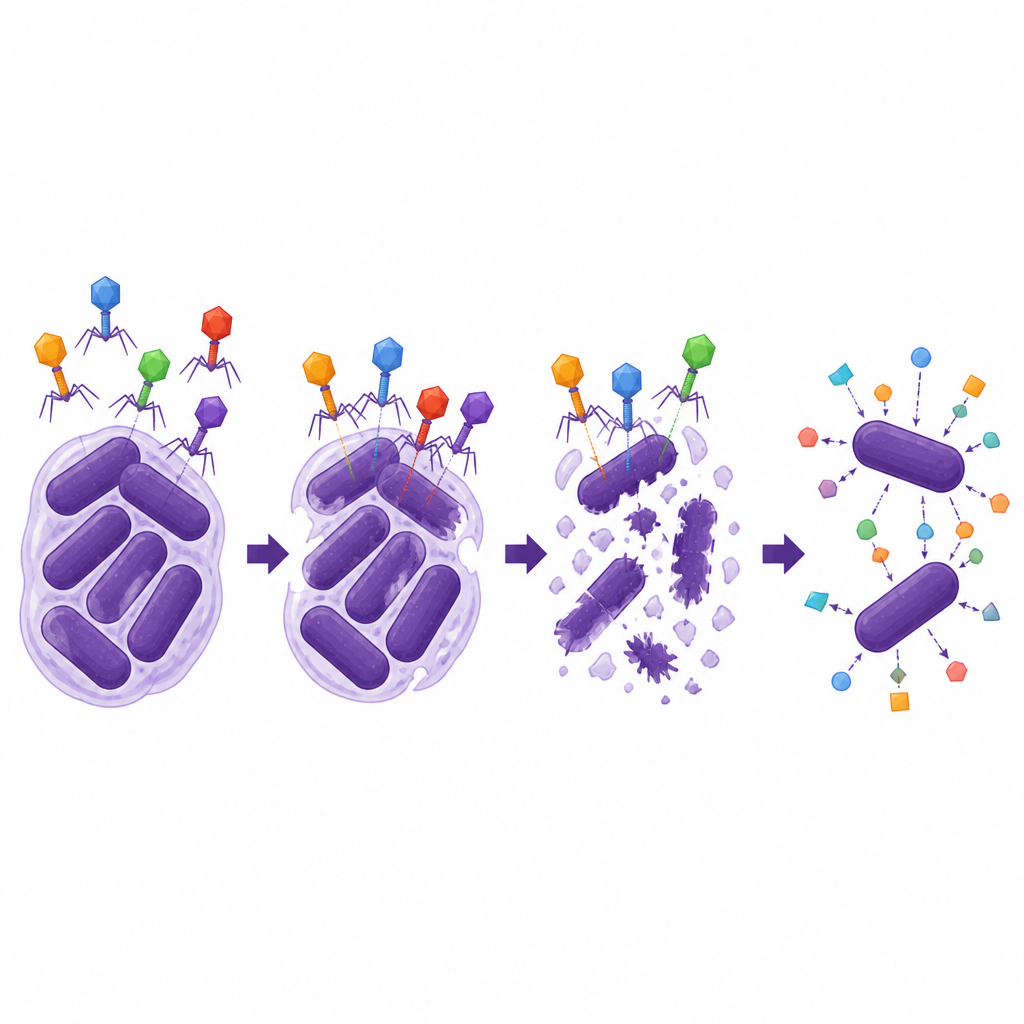
Addestrare un virus a riconoscere nuovi bersagli
Poiché la portata ristretta di un singolo fago limita la sua utilità medica, il team ha provato a spingere ΦAb1-SL1 e ΦAb1-SL2 a infettare un secondo ceppo inizialmente resistente, chiamato Abau2. Facendo crescere ripetutamente i fagi con questo nuovo ospite, hanno infine ottenuto una variante adattata, ΦAb2-SL1, in grado di attaccare sia il ceppo originale sia il nuovo, sebbene si moltiplicasse meno efficacemente su Abau2. Il sequenziamento del genoma ha rivelato solo piccole modifiche genetiche, principalmente nelle proteine della coda che probabilmente entrano in contatto con la superficie batterica; queste sottili alterazioni hanno ampliato il range di ospiti del fago preservandone le caratteristiche fondamentali di crescita e stabilità.
Cosa significa per i trattamenti futuri
In termini semplici, questo lavoro dimostra che fagi utili contro un patogeno ospedaliero ad alto rischio possono essere pescati dalle acque reflue, selezionati e depurati con strumenti genetici moderni e poi allenati per riconoscere bersagli batterici aggiuntivi. Uno di questi fagi ha funzionato particolarmente bene se associato all’antibiotico avanzato cefiderocol, suggerendo che tali combinazioni potrebbero far rivivere l’efficacia dei farmaci contro infezioni ostinate invece di sostituire del tutto gli antibiotici. Sebbene gli esperimenti siano stati condotti solo in provetta e i fagi infettino ancora un numero limitato di ceppi, la pipeline passo dopo passo delineata qui indica la possibilità di costruire banche regionali di fagi da cui i clinici potrebbero attingere quando trattano A. baumannii multiresistente e, in futuro, altri batteri difficili da combattere.
Citazione: Nicolosi, A., Bonanno Ferraro, G., Brandtner, D. et al. Integrated wet lab and in silico discovery and characterization of bacteriophages with antibiotic synergy against multidrug resistant Acinetobacter baumannii. Sci Rep 16, 15091 (2026). https://doi.org/10.1038/s41598-026-44506-4
Parole chiave: terapia con batteriofagi, Acinetobacter baumannii, sinergia antibiotica, cefiderocol, resistenza multidrogica