Clear Sky Science · ja
多剤耐性Acinetobacter baumanniiに対して抗生物質と相乗するバクテリオファージの統合的ウェットラボおよびインシリコによる探索と特性解析
古くからの敵に新たな味方が加わる
薬剤耐性感染症は、かつては日常的だった病院治療をはるかに危険にしており、とりわけ多くの抗生物質をはねつける困難な細菌、Acinetobacter baumanniiが問題となっています。本研究は、細菌を捕食するウイルスであるバクテリオファージ(ファージ)を日常の下水から見つけ、実験室とコンピュータ上で訓練・検査して、こうした頑強な院内病原体に対して現代の抗生物質と協働して働く可能性を探ります。 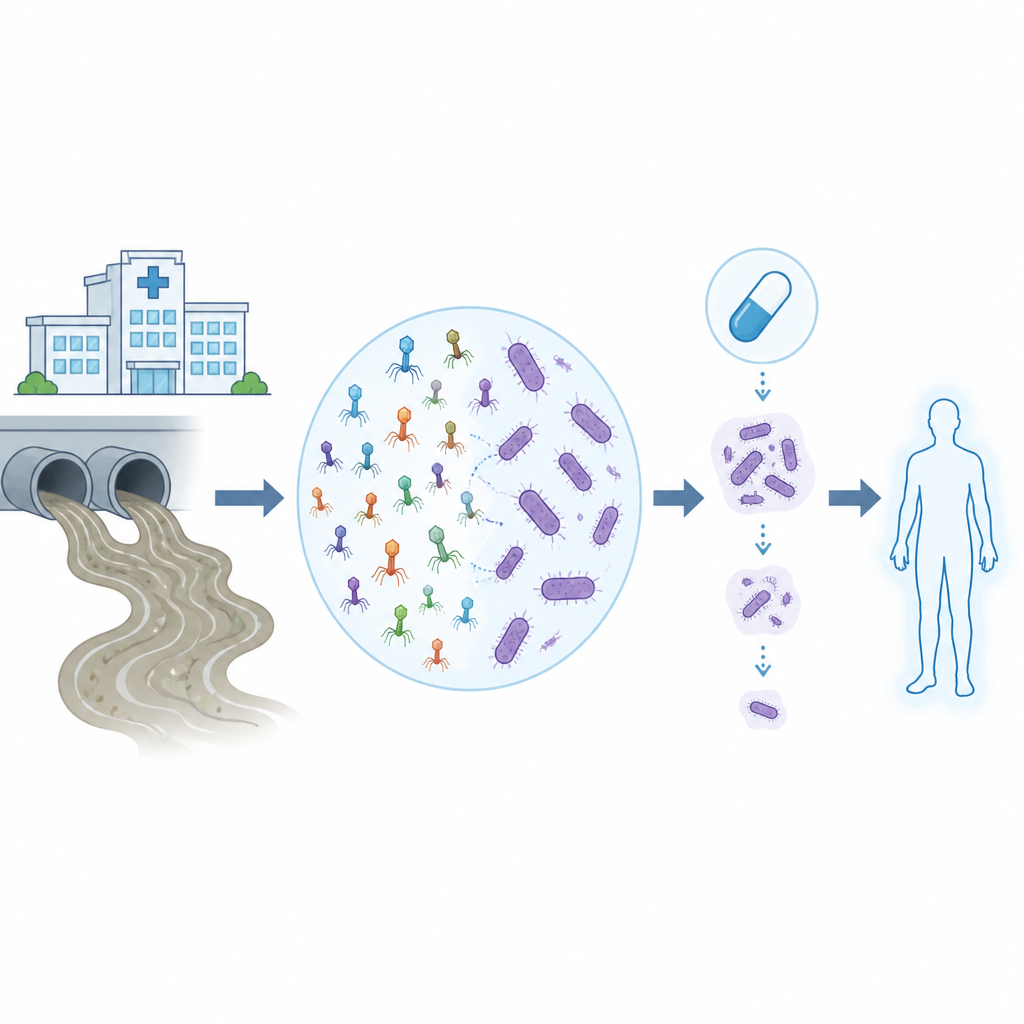
下水中で有用なウイルスを探索する
研究者らはまず、イタリア各地の病院から集めた20株の多剤耐性A. baumanniiパネルを組みました。遺伝的指紋を用いて代表的な2株をファージの「餌」として選び、未処理の下水にさらしました。下水はこうしたウイルスの豊かな自然の貯留層です。培養板上で明確な死滅スポットを形成したのは1株(Abau1)のみでした。電子顕微鏡観察により、同じ広義のウイルス群に属する4つの関連ファージが確認されましたが、形態は2種類に分かれており、それが異なる生活様式や挙動を示唆していました。
有力な殺菌者と静かに寄生するものを見分ける
すべてのファージが治療に有用というわけではありません。中には宿主のDNAに静かに組み込まれて潜伏するものがあり、そうしたファージは宿主を破壊しません。チームはファージゲノムを解読し、宿主細菌のゲノムと比較しました。2つのファージはAbau1染色体に既に埋め込まれている断片とほぼ同一であることが分かり、それらは宿主由来の寄生的なもの(温和型)であり静穏な生活様式に移行し得るものでした。他の2つ、ΦAb1-SL1とΦAb1-SL2は宿主DNAとの重複がなく、毒素産生や抗生物質耐性に関わる既知の遺伝子を持たなかったため、標的を確実に破裂させ殺す純粋な溶菌性ファージと判断されました。
強さ、攻撃範囲、薬剤との協働を評価する
次に、研究者らは2つの溶菌性ファージがどれだけ頑健で多用途かを調べました。両ファージは幅広い温度と酸性度の範囲で感染力を維持し、人体の一部に類似した条件下でも増殖が効率的でした。しかし、感染できるA. baumannii株の範囲は狭く、特定の外膜被包(カプセル)型を共有する株に限られ、ファージがしばしば鍵と錠のように振る舞うことを強調しました。最も注目すべきは、ΦAb1-SL1がいくつかのセフェム系抗生物質、特にセフィデロコルと強い相乗効果を示した点です。試験管内の検査で、このファージと低用量のセフィデロコルを併用すると、いずれか単独の治療よりも細菌増殖がはるかに抑えられ、耐性範囲から株を移し出すために必要な抗生物質量が低下しました。一方、カルバペネム系のメロペネムでは同様の助けは見られませんでした。 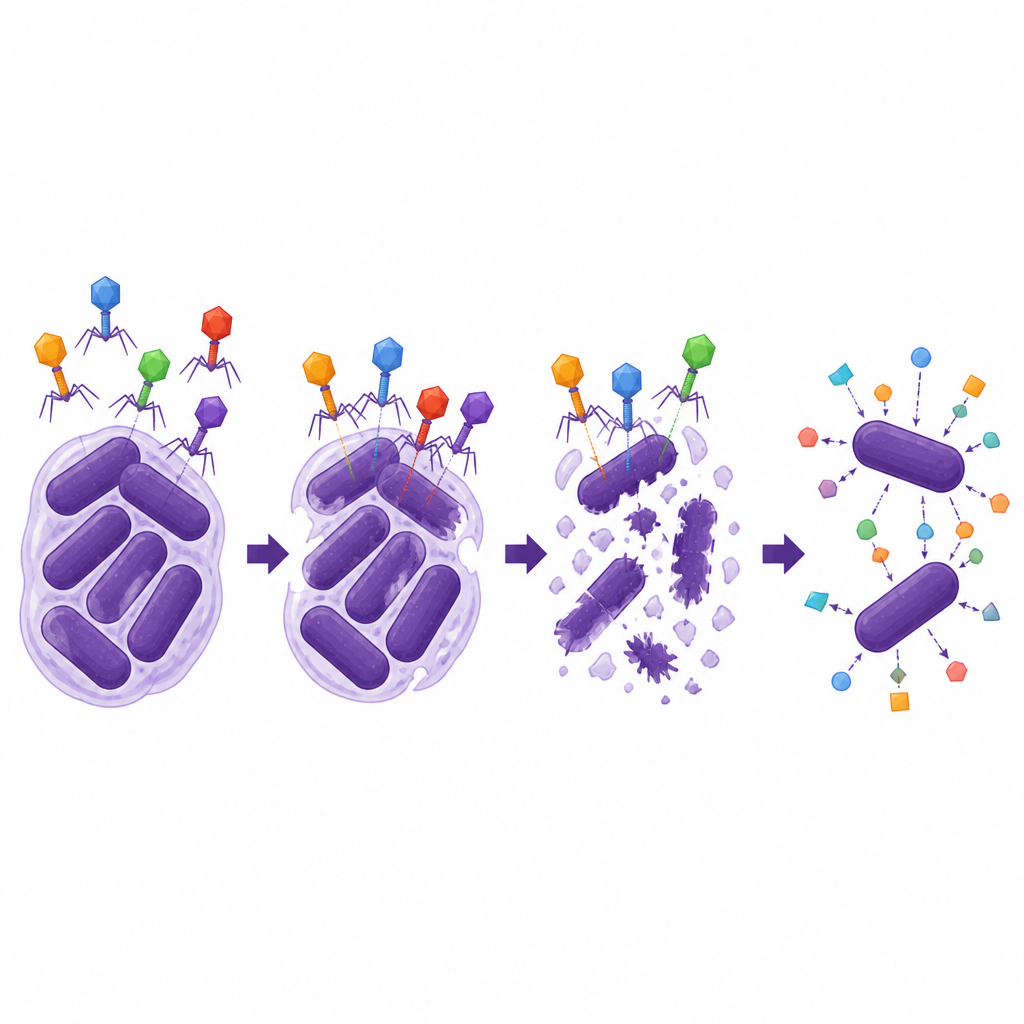
新しい標的を認識するようウイルスを訓練する
単一ファージの狭い攻撃範囲は医療応用を制限するため、チームはΦAb1-SL1とΦAb1-SL2を用いて、当初は抵抗性であった別の株Abau2に感染させるよう適応を試みました。新しい宿主と繰り返し共培養することで、最終的に元の株と新規株の両方を攻撃できる適応変異体ΦAb2-SL1を得ましたが、Abau2上では増殖効率は低下しました。ゲノム解析により、主に細菌表面に触れる尾部タンパク質にわずかな遺伝的修正が見られ、こうした微細な変化が宿主範囲を広げつつも基本的な増殖特性と安定性を維持していることが示されました。
将来の治療への示唆
簡潔に言えば、本研究は高リスクな院内病原体に対する有用なファージが下水から採取でき、現代の遺伝学的手法でスクリーニング・精製され、さらに追加の細菌標的を認識するよう訓練できることを示しています。これらのうちの一つは、高度な抗生物質であるセフィデロコルとの併用で特に有効であり、そのような組み合わせが抗生物質を完全に置き換えるのではなく、難治性感染症に対する薬剤効果を回復させる可能性を示唆します。実験はいずれも試験管内で行われ、ファージの感染対象は依然として限られているものの、ここで示した段階的なパイプラインは、臨床医が多剤耐性A. baumanniiや将来的には他の手強い細菌に対処する際に利用できる地域的なファージバンクの構築に向けた道筋を示しています。
引用: Nicolosi, A., Bonanno Ferraro, G., Brandtner, D. et al. Integrated wet lab and in silico discovery and characterization of bacteriophages with antibiotic synergy against multidrug resistant Acinetobacter baumannii. Sci Rep 16, 15091 (2026). https://doi.org/10.1038/s41598-026-44506-4
キーワード: バクテリオファージ療法, Acinetobacter baumannii, 抗生物質の相乗効果, セフィデロコル, 多剤耐性