Clear Sky Science · tr
Çok ilaca dirençli Acinetobacter baumannii'ye karşı antibiyotikle sinerji gösteren bakteriyofajların entegre ıslak laboratuvar ve in silico keşfi ve karakterizasyonu
Eski Mikrop Düşmanları Yeni Müttefikler Kazanıyor
İlaçlara dirençli enfeksiyonlar, özellikle birçok antibiyotiğe direnç gösteren ve öldürülmesi zor olan Acinetobacter baumannii söz konusu olduğunda, bir zamanlar rutinde yapılan hastane müdahalelerini çok daha riskli hale getiriyor. Bu çalışma, bakterileri hedef alan virüsler olan bakteriyofajların (fajların) günlük atık sularda nasıl bulunabildiğini ve laboratuvarda ile bilgisayarda eğitilip test edilerek bu inatçı hastane mikroplarına karşı modern antibiyotiklerle nasıl birlikte çalıştırılabileceğini inceliyor. 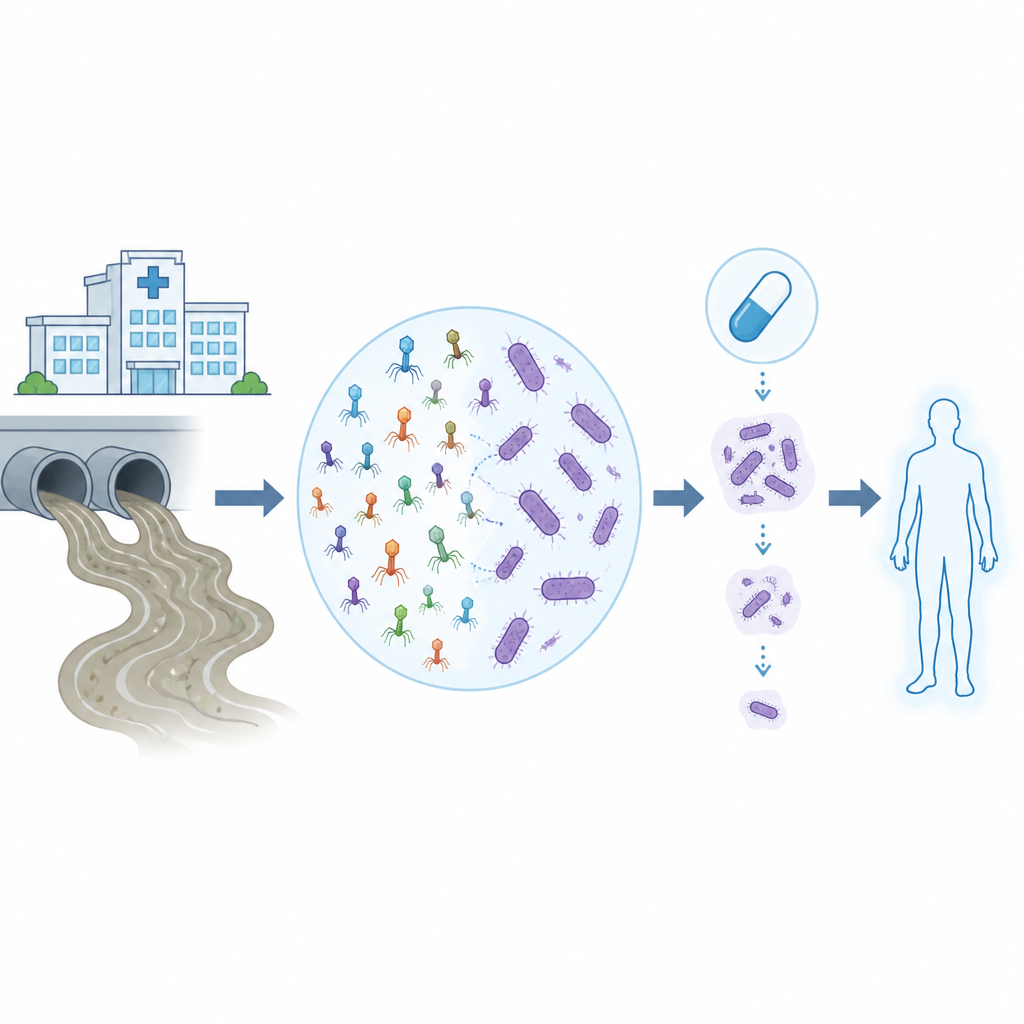
Atık Suda Yararlı Virüsleri Avlamak
Araştırmacılar, İtalya genelindeki hastanelerden toplanan yirmi çok ilaca dirençli A. baumannii suşundan oluşan bir panel kurmakla başladı. Genetik parmak izlerine dayanarak iki temsilci suşu faj için yem olarak seçtiler ve bunları bu virüslerin zengin doğal rezervuarı olan arıtılmamış atık suya maruz bıraktılar. Sadece Abau1 adlı suş, laboratuvar plakalarında bakterilerin öldüğünü gösteren net bölgeler oluşturan fajlar verdi. Elektron mikroskobunda, aynı geniş viral gruba ait dört ilişkili faj görüldü; ancak iki farklı gövde şekli, farklı yaşam biçimlerine ve davranışlara işaret ediyordu.
İyi Katilleri Sessiz Gezginlerden Ayırmak
Her faj terapötik amaç için uygun değildir; çünkü bazıları konaklarını yok etmek yerine bakteriyel DNA içinde sessizce gizlenmeye meyillidir. Ekip, faj genomlarını diziledi ve bunları konak bakterinin kendi genetik materyaliyle karşılaştırdı. İki faj, Abau1 kromozomuna zaten gömülü olan parçalara neredeyse tamamen denk çıktı; bu da bunların konak kaynaklı, sessizleşebilen (temperat) gezginler olduğunu gösteriyordu. Diğer iki faj ise, ΦAb1-SL1 ve ΦAb1-SL2 adlarını taşıyanlar, konak DNA ile örtüşme göstermedi ve bilinen toksin üretimi ya da antibiyotik direnci genleri taşımıyordu; bu da onları hedeflerini güvenilir şekilde parçalayıp öldüren saf litik fajlar olarak işaretliyordu.
Güç, Kapsam ve İlaçla İş Birliğini Test Etmek
Bilim insanları daha sonra bu iki litik fajın ne kadar dayanıklı ve çok yönlü olduğunu sorguladılar. Her ikisi de insan vücudunun bazı bölgelerine benzer koşulları da içeren geniş bir sıcaklık ve asidite aralığında enfektif kaldı ve bakterilerin içinde verimli şekilde çoğaldı. Ancak yalnızca belirli bir dış kapsül tipini paylaşan dar bir A. baumannii suş setini enfekte edebildiler; bu da fajların sık sık kilit ve anahtar sistemi gibi davrandığını vurguluyor. En çarpıcı olanı, ΦAb1-SL1 adlı fajın birkaç sefalosporin antibiyotiği, özellikle de cefiderocol ile güçlü bir sinerji göstermesiydi. Laboratuvar testlerinde bu faj ile düşük doz cefiderocol kombinasyonu, ya tek başına uygulanan tedavilerden çok daha fazla bakteri büyümesini azalttı ve suşu dirençli aralıktan çıkarmak için gereken antibiyotik dozunu düşürdü; benzer bir yardım karbapenem sınıfından meropenem ile görülmedi. 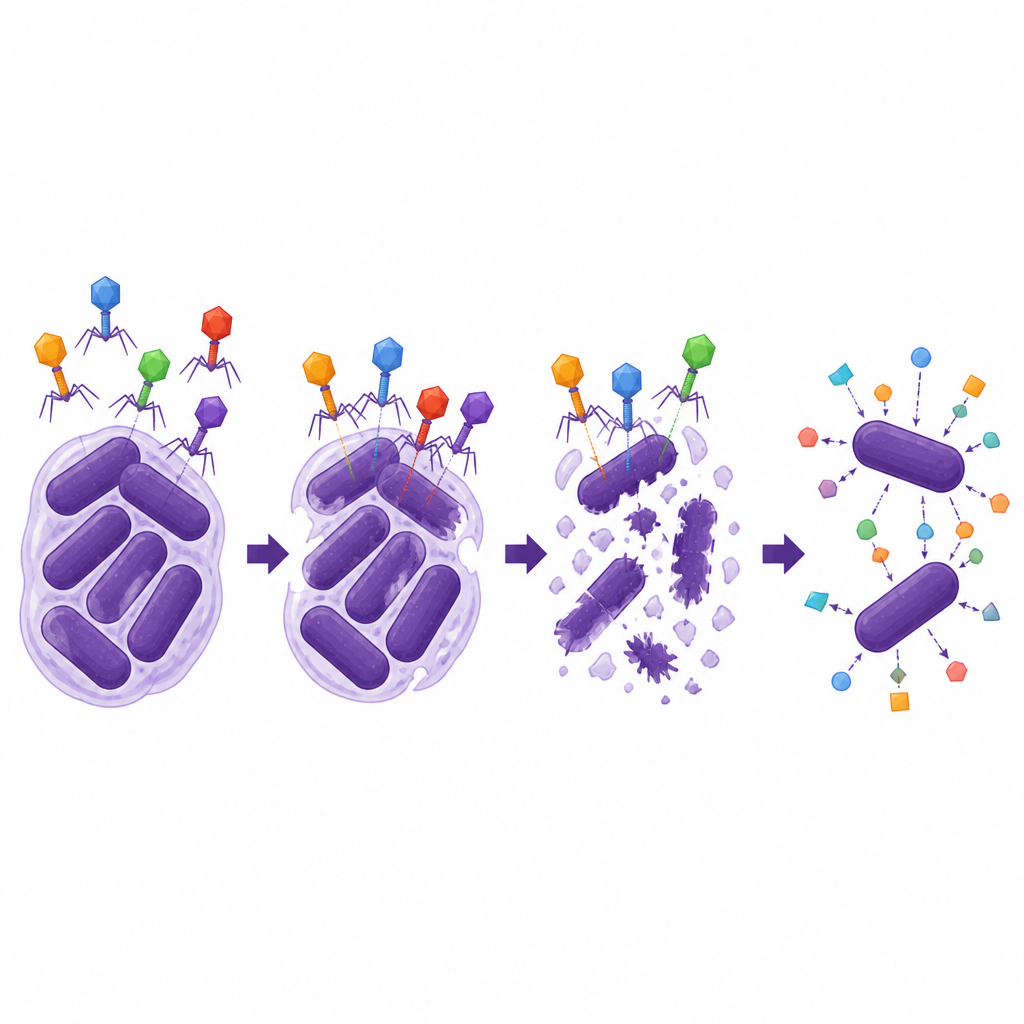
Yeni Hedefleri Tanıması İçin Bir Virüsü Eğitmek
Tek bir fajın dar etki spektrumu tıbbi faydasını sınırladığından, ekip ΦAb1-SL1 ve ΦAb1-SL2’yi başlangıçta dirençli olan Abau2 adlı ikinci bir suşu enfekte etmeleri için zorlamaya çalıştı. Fajları bu yeni konakla tekrarlı olarak büyüterek sonunda hem orijinal hem de yeni suşa saldırabilen, uyarlanmış bir varyant olan ΦAb2-SL1’i elde ettiler; ancak bu varyant Abau2 üzerinde daha az verimli çoğalıyordu. Genom dizilemesi, başlıca bakteriyel yüzeye temas eden kuyruk proteinlerinde olmak üzere yalnızca küçük genetik düzenlemeler ortaya koydu; buna rağmen bu ince değişiklikler fajın konak aralığını genişletirken temel büyüme özelliklerini ve stabilitesini korudu.
Gelecekteki Tedaviler İçin Anlamı
Basitçe ifade etmek gerekirse, bu çalışma yüksek riskli bir hastane mikrobu için yararlı fajların atık sudan elde edilebileceğini, modern genetik araçlarla taranıp temizlenebileceğini ve ardından ek bakteri hedeflerini tanımaya eğitilebileceğini gösteriyor. Bu fajlardan biri gelişmiş antibiyotik cefiderocol ile özellikle iyi çalıştı; bu da böyle kombinasyonların antibiyotikleri tamamen değiştirmek yerine inatçı enfeksiyonlara karşı ilaç etkinliğini yeniden canlandırabileceğine işaret ediyor. Deneyler yalnızca test tüplerinde yapıldı ve fajlar hâlâ sınırlı bir suş setini enfekte ediyor olsa da, burada adım adım sunulan yöntem bölgesel faj bankaları kurmaya ve klinisyenlerin çok ilaca dirençli A. baumannii ve nihayetinde diğer zorlu bakteri düşmanlarını tedavi ederken bunlardan yararlanmasına yönelik bir yol gösteriyor.
Atıf: Nicolosi, A., Bonanno Ferraro, G., Brandtner, D. et al. Integrated wet lab and in silico discovery and characterization of bacteriophages with antibiotic synergy against multidrug resistant Acinetobacter baumannii. Sci Rep 16, 15091 (2026). https://doi.org/10.1038/s41598-026-44506-4
Anahtar kelimeler: bakteriyofaj tedavisi, Acinetobacter baumannii, antibiyotik sinerjisi, cefiderocol, çoklu ilaç direnci