Clear Sky Science · fr
Découverte et caractérisation intégrées, en laboratoire humide et in silico, de bactériophages en synergie avec des antibiotiques contre Acinetobacter baumannii multirésistant
De vieux ennemis microbiens gagnent de nouveaux alliés
Les infections résistantes aux médicaments rendent autrefois banales les interventions hospitalières beaucoup plus risquées, en particulier lorsque l’agent en cause est Acinetobacter baumannii, une bactérie difficile à éliminer qui résiste à de nombreux antibiotiques. Cette étude examine comment des virus prédateurs de bactéries, appelés bactériophages ou phages, peuvent être trouvés dans les eaux usées quotidiennes puis entraînés et testés en laboratoire et par analyses informatiques pour agir de concert avec des antibiotiques modernes contre ces germes hospitaliers persistants. 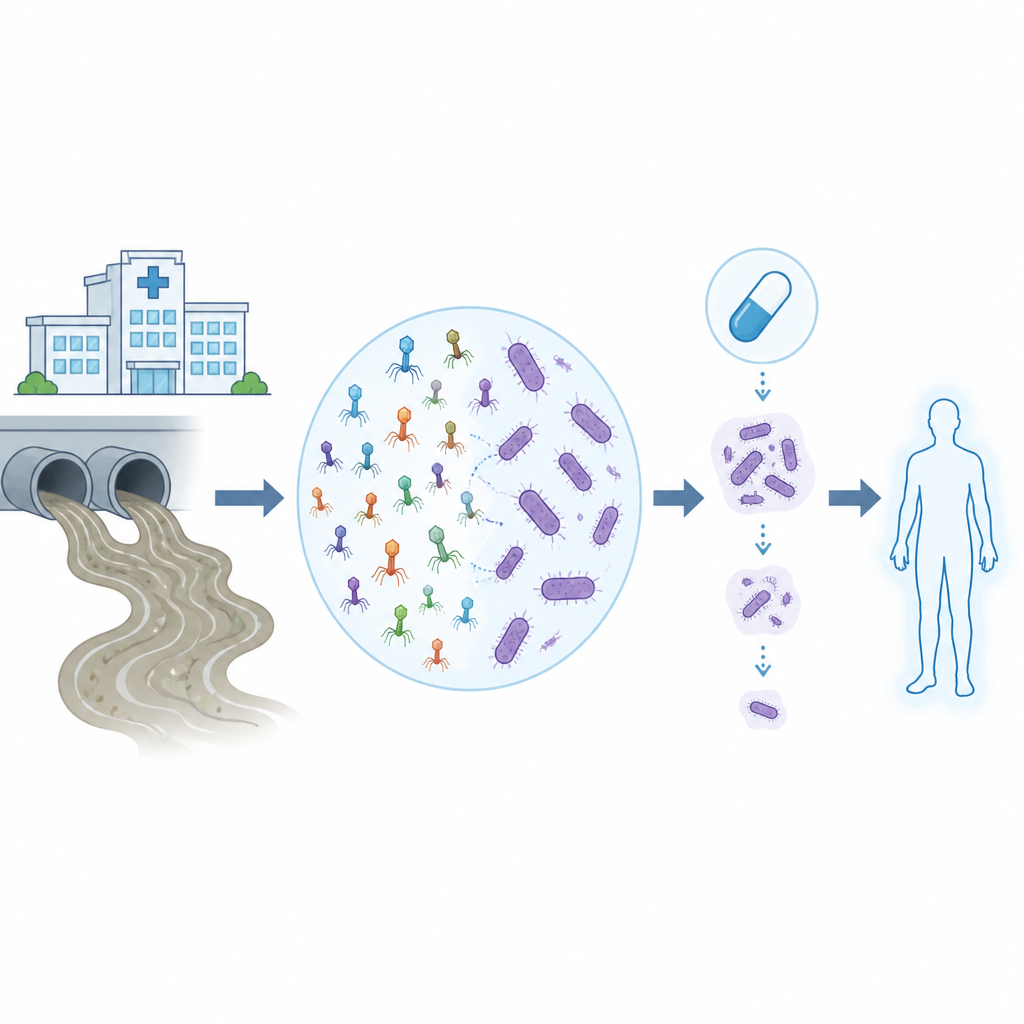
À la recherche de virus utiles dans les eaux usées
Les chercheurs ont commencé par constituer un panel de vingt souches d’A. baumannii multirésistantes prélevées dans des hôpitaux italiens. À l’aide de profils génétiques, ils ont choisi deux souches représentatives comme « appâts » pour les phages et les ont exposées à des eaux usées non traitées, un réservoir naturel riche en ces virus. Une seule souche, appelée Abau1, a permis d’isoler des phages formant des zones claires de bactéries mortes sur des plaques de laboratoire. La microscopie électronique a révélé quatre phages apparentés, tous issus du même grand groupe viral, mais présentant deux morphologies corporelles distinctes suggérant des modes de vie et des comportements différents.
Distinguer les bons tueurs des passagers silencieux
Tous les phages ne sont pas utiles en thérapie, car certains tendent à s’intégrer discrètement dans l’ADN bactérien au lieu de détruire leur hôte. L’équipe a séquencé les génomes des phages et les a comparés au matériel génétique de la bactérie hôte. Deux phages se sont révélés presque identiques à des séquences déjà intégrées dans le chromosome d’Abau1, ce qui signifie qu’il s’agissait de passagers d’origine hôte susceptibles d’adopter un mode de vie tempéré et silencieux. Les deux autres, nommés ΦAb1-SL1 et ΦAb1-SL2, ne présentaient aucun recoupement avec l’ADN de l’hôte et ne portaient aucun gène connu de production de toxines ou de résistance aux antibiotiques, les qualifiant de phages strictement lytiques qui font éclater et tuer leurs cibles de façon fiable.
Évaluer la robustesse, l’étendue et la coopération avec les médicaments
Les scientifiques ont ensuite évalué la résistance et la polyvalence des deux phages lytiques. Les deux restaient infectieux sur une large gamme de températures et d’acidité, y compris des conditions similaires à celles rencontrées dans certaines parties du corps humain, et se multipliaient efficacement une fois à l’intérieur des bactéries. Cependant, ils n’infectaient qu’un ensemble restreint de souches d’A. baumannii partageant un type de capsule externe spécifique, soulignant combien les phages fonctionnent souvent comme des systèmes serrure/clé. Plus remarquable, un phage, ΦAb1-SL1, a montré une forte synergie avec plusieurs antibiotiques céphalosporines, en particulier le cefiderocol. Dans des essais en laboratoire, la combinaison de ce phage avec de faibles doses de cefiderocol réduisait la croissance bactérienne bien plus que chaque traitement pris séparément et abaissait la dose d’antibiotique nécessaire pour sortir la souche de la plage de résistance, tandis qu’un tel effet n’était pas observé avec le carbapénème méropénem. 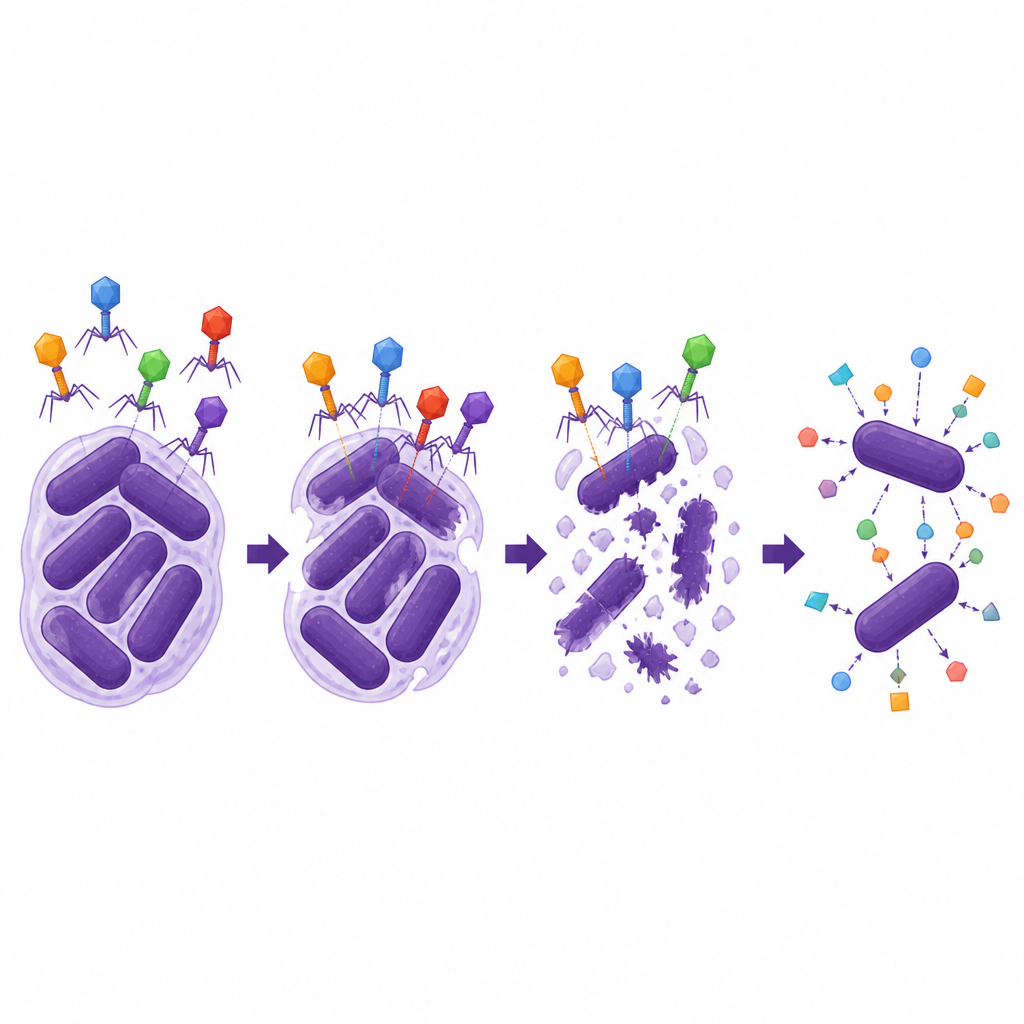
Apprendre à un virus à reconnaître de nouvelles cibles
Étant donné que la portée étroite d’un phage limite son utilité médicale, l’équipe a tenté d’amener ΦAb1-SL1 et ΦAb1-SL2 à infecter une seconde souche initialement résistante nommée Abau2. En cultivant les phages de manière itérative avec ce nouvel hôte, ils ont finalement obtenu un variant adapté, ΦAb2-SL1, capable d’attaquer à la fois la souche d’origine et la nouvelle souche, bien qu’il se multiplie moins efficacement sur Abau2. Le séquençage du génome a révélé seulement de petites modifications génétiques, principalement dans des protéines de la queue qui touchent probablement la surface bactérienne ; ces changements subtils ont néanmoins élargi l’éventail d’hôtes du phage tout en préservant ses caractéristiques de croissance et sa stabilité de base.
Ce que cela implique pour les traitements futurs
En termes simples, ce travail montre que des phages utiles contre une bactérie hospitalière à haut risque peuvent être pêchés dans les eaux usées, sélectionnés et purifiés à l’aide d’outils génétiques modernes, puis entraînés à reconnaître d’autres cibles bactériennes. L’un de ces phages a particulièrement bien fonctionné en association avec l’antibiotique de pointe cefiderocol, suggérant que de telles combinaisons pourraient restaurer l’efficacité des médicaments contre des infections tenaces plutôt que de remplacer complètement les antibiotiques. Bien que les expériences aient été réalisées uniquement en éprouvettes et que les phages infectent encore un nombre limité de souches, la démarche pas à pas décrite ici oriente la création de banques régionales de phages auxquelles les cliniciens pourraient recourir pour traiter Acinetobacter baumannii multirésistant et, à terme, d’autres redoutables adversaires bactériens.
Citation: Nicolosi, A., Bonanno Ferraro, G., Brandtner, D. et al. Integrated wet lab and in silico discovery and characterization of bacteriophages with antibiotic synergy against multidrug resistant Acinetobacter baumannii. Sci Rep 16, 15091 (2026). https://doi.org/10.1038/s41598-026-44506-4
Mots-clés: thérapie par bactériophages, Acinetobacter baumannii, synergie antibiotique, cefiderocol, multirésistance