Clear Sky Science · zh
导管原位癌的空间蛋白质组学揭示明显的区域差异
为何早期乳腺变化重要
导管原位癌(DCIS)是一种常在常规乳腺X光检查中发现的早期乳腺病变。此时病变尚未突破乳管进入周围组织,但在部分女性中最终可能发展为侵袭性乳腺癌。目前,医生无法可靠地区分哪些DCIS是无害的、不会进展的“过客”,哪些则会成为未来的威胁,因此许多患者接受了可能并非必需的手术和放疗。本研究以一种新的高分辨率方式审视DCIS,探究乳管内及其周围蛋白质的分布如何帮助预测哪些病变更可能变得危险。
把乳腺组织当作地图来观察
研究者没有将组织研磨成单一混合样本,而是使用一种称为空间蛋白质组学的技术,在切片上精确选择的点位测量数十种蛋白质,近似于在地图上打点。他们检查了103名接受DCIS治疗的女性的存档组织,其中一些人之后没有出现进一步的乳腺问题,一些人在同侧乳房再次出现DCIS,另一些则最终出现了侵袭性癌症。对每个病例,病理学家标记了DCIS导管内的区域、附近的支持组织(间质)、外观正常的导管和活检部位。从超过1200个此类微小区域中,研究团队量化了53种与激素、促生长、结构和免疫活性相关的蛋白,绘制出每个病变的详细空间画像。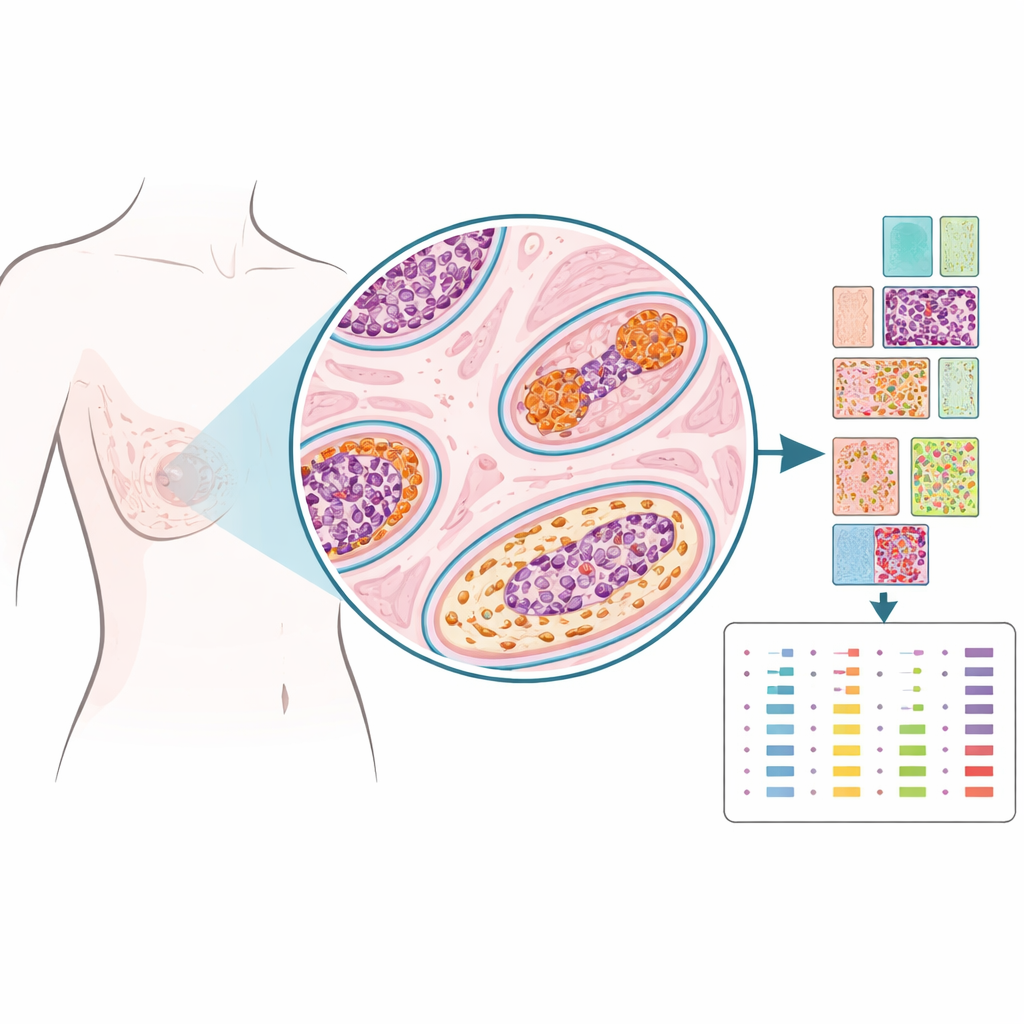
两类主要的早期病变
当团队在不告知计算机任何临床信息的情况下对数据进行分组时,出现了一个显著模式。大多数DCIS样本可归为两类:一类为雌激素受体(ER)水平高且生长因子受体HER2水平低,另一类则相反,ER水平低而HER2水平高。这一划分与侵袭性乳腺癌的分类相似但并不完全相同。外观正常的导管没有表现出同样明显的聚类,而DCIS周围的支持组织则显示出其自身独特的蛋白模式。在周围间质中,靠近ER阴性DCIS的区域往往富含免疫细胞标志物,提示与靠近ER阳性DCIS的区域相比,免疫小环境更为活跃。
每个导管内部的隐性差异
由于该技术可以区分单个导管内的不同区域,研究者还比较了导管边缘与中心的蛋白水平。与导管壁相关的收缩外层和细胞分裂相关的蛋白在边缘更为丰富,这暗示贴近导管壁的细胞代谢更活跃。相反,与能量供应相关的糖转运蛋白在导管中心更高,提示拥挤的内层细胞具有不同的代谢需求。值得注意的是,总体的激素受体水平在中心与边缘之间变化不大,但结构和生长相关蛋白的细微平衡发生了改变,揭示出整体样本检测无法发现的内部组织结构。
提示哪些DCIS可能会进展
关键问题是这些空间蛋白模式中是否有能预示未来侵袭性癌症的信号。将后来发生侵袭性疾病的女性与未发生者比较时,单看DCIS自身时在生长和结构蛋白上发现了一些有提示性的但统计显著性较弱的差异。当他们将DCIS中蛋白水平与同一患者附近外观正常导管进行比较时,信号更强。在后来变为侵袭性的病变中,导管内某些免疫相关蛋白的比值发生了变化:杀伤性T细胞及其相关受体的标志物往往较低,而一种可能抑制免疫反应的蛋白相对较高。这提示导管内部的局部免疫环境可能较难抑制新生的癌细胞。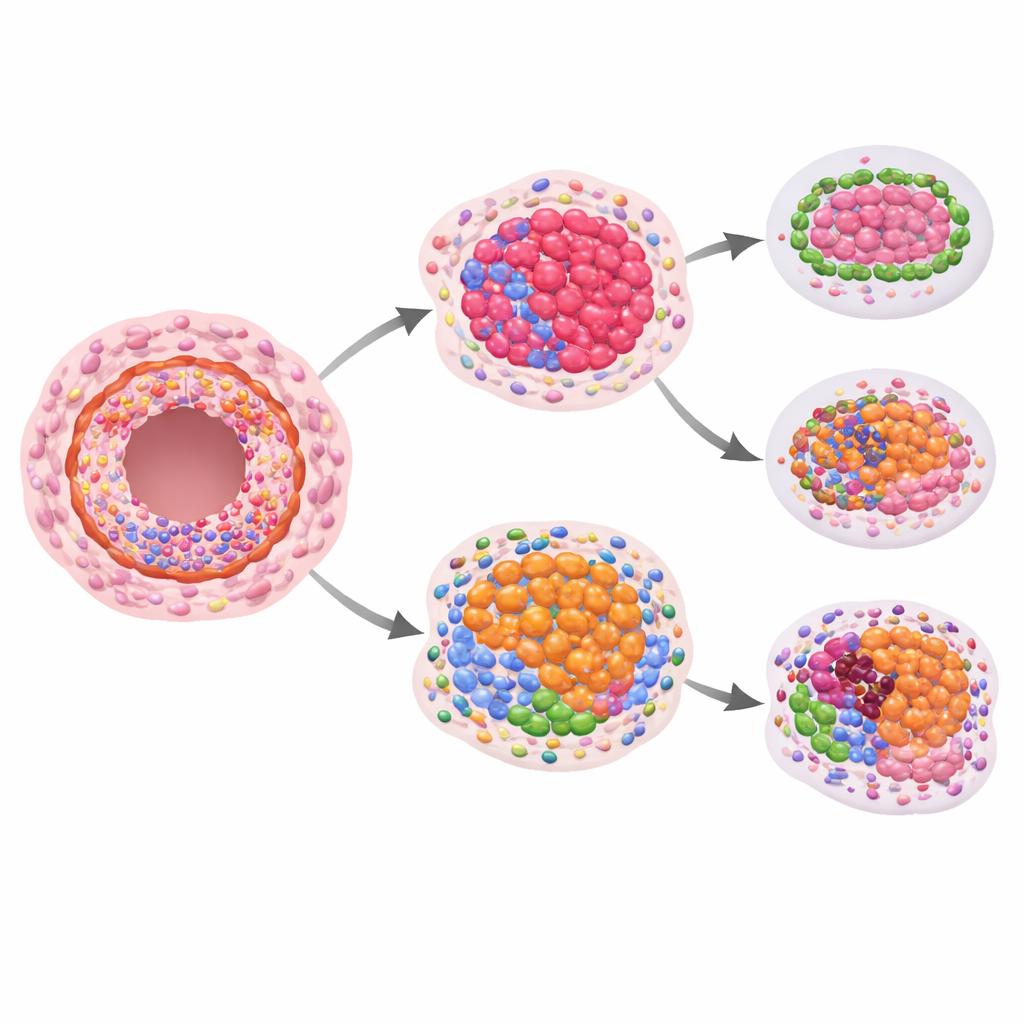
治疗与时间如何重塑肿瘤
对于一部分患者,研究者还研究了同侧乳房后来发生事件的组织——要么是另一处DCIS病变,要么是侵袭性肿瘤——并将其与原始DCIS进行比较。在许多配对样本中,激素与HER2模式相似,但也有出现重大转变的情况,包括某些原为ER高、HER2低的DCIS随后出现ER低、HER2高的复发,或原为HER2高的DCIS随后出现HER2明显降低的侵袭性癌症。其中一些变化很可能反映的是完全独立新肿瘤的出现,而非原有病变的线性演化。在接受激素治疗的女性中,后续出现的癌症常表现出受雌激素驱动的蛋白水平降低,表明治疗可以改变随后的疾病的分子特征。
这对患者意味着什么
这项研究表明DCIS并非一种单一均质的状态,而是由在激素信号、免疫存在和细胞行为上存在差异的区域构成的拼图,而这些差异可能影响未来的风险。虽然没有单一蛋白成为完美的预测工具,这项工作突出了导管内部的特定免疫标志物以及DCIS与邻近正常组织之间的对比,作为未来风险评分的有希望成分。将这种空间信息与现有的遗传和临床资料结合,研究者希望推动朝着这样的未来发展:能够更有把握地向DCIS患者说明,她们是可以安全选择密切监测,还是确实需要积极治疗。
引用: Marks, J.R., Dai, Y., King, L.M. et al. Spatial proteomics of breast ductal carcinoma in situ reveal distinct regional differences. Sci Rep 16, 13350 (2026). https://doi.org/10.1038/s41598-026-43486-9
关键词: 导管原位癌, 空间蛋白质组学, 乳腺癌风险, 肿瘤微环境, 免疫标志物