Clear Sky Science · de
Räumliche Proteomik von duktalem Carcinoma in situ der Brust zeigt ausgeprägte regionale Unterschiede
Warum frühe Veränderungen in der Brust wichtig sind
Duktales Carcinoma in situ (DCIS) ist eine frühe Form von Brustveränderung, die häufig bei routinemäßigen Mammographien entdeckt wird. Es hat die Milchgänge noch nicht in das umliegende Gewebe durchbrochen, kann aber bei einigen Frauen später zu invasivem Brustkrebs führen. Derzeit können Ärztinnen und Ärzte nicht zuverlässig unterscheiden, welche DCIS-Läsionen harmlos sind und welche zu einer späteren Gefahr werden, deshalb erhalten viele Patientinnen Operationen und Bestrahlungen, die sie möglicherweise nicht benötigen. Diese Studie wirft einen neuen, hochauflösenden Blick auf DCIS, um zu prüfen, wie die Anordnung von Proteinen in und um diese Gänge dazu beitragen könnte, vorherzusagen, welche Fälle eher gefährlich werden.
Brustgewebe wie eine Landkarte betrachten
Statt Gewebe zu einem einzelnen, vermischten Probenmaterial zu vermahlen, nutzten die Forschenden eine Technik namens räumliche Proteomik, um Dutzende Proteine an gezielt ausgewählten Punkten auf dem Objektträger zu messen – fast wie das Setzen von Pins auf einer Karte. Sie untersuchten archiviertes Gewebe von 103 Frauen, die wegen DCIS behandelt worden waren: einige hatten später keine weiteren Brustprobleme, einige entwickelten erneut DCIS in derselben Brust, und einige bekamen schließlich einen invasiven Tumor in dieser Brust. Für jeden Fall markierten Pathologinnen Regionen innerhalb der DCIS-Gänge, das nahegelegene Stroma, normal aussehende Gänge und Biopsiestellen. Aus mehr als 1.200 dieser winzigen Regionen quantifizierte das Team 53 Proteine, die mit Hormonen, Wachstum, Struktur und Immunaktivität verbunden sind, und erstellte so ein detailliertes räumliches Porträt jeder Läsion. 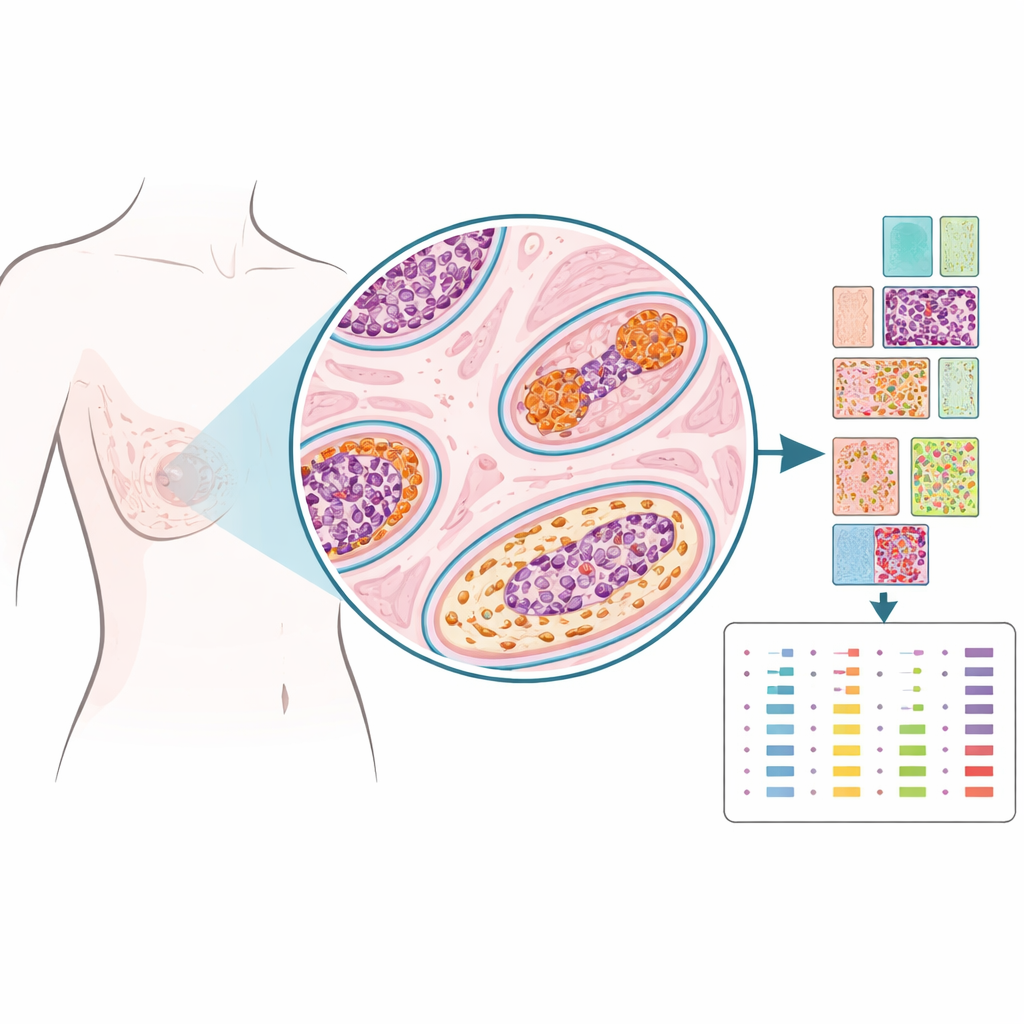
Zwei Haupttypen früher Läsionen
Als das Team die Daten gruppierte, ohne dem Computer klinische Details zu verraten, zeigte sich ein auffälliges Muster. Die meisten DCIS-Proben fielen in eine von zwei Gruppen: solche mit hohen Spiegeln des Östrogenrezeptors (ER) und niedrigen Spiegeln des Wachstumsfaktor-Rezeptors HER2, und solche mit dem umgekehrten Muster – niedriger ER- und hoher HER2-Expression. Diese Aufteilung ähnelte, war aber nicht identisch mit der Kategorisierung invasiver Brustkrebse. Normal aussehende Gänge zeigten nicht dieselbe starke Clusterbildung, und das stützende Gewebe um DCIS wies eigene, unterscheidbare Proteinmuster auf. Im umgebenden Stroma waren Bereiche neben ER-negativem DCIS tendenziell reich an Immunzellmarkern, was auf eine aktivere Immunumgebung im Vergleich zu Regionen um ER-positives DCIS hindeutet.
Verborgene Unterschiede innerhalb eines Gangs
Da die Technik Regionen innerhalb eines einzelnen Gangs trennen konnte, verglichen die Forschenden auch Proteinspiegel am Rand des Gangs mit denen im Zentrum. Proteine, die mit der kontraktilen äußeren Schicht des Gangs und mit Zellteilung assoziiert sind, waren am Rand häufiger vorhanden, was darauf hindeutet, dass Zellen, die an der Gangwand anliegen, besonders aktiv sind. Im Gegensatz dazu war ein Zuckertransporter, der mit der Energieversorgung verknüpft ist, im Gangzentrum höher ausgeprägt, was auf unterschiedliche Stoffwechselanforderungen in den engen inneren Zellen hinweist. Bemerkenswert war, dass die allgemeinen Hormonrezeptorspiegel zwischen Zentrum und Rand nicht stark variierten, wohl aber das feine Gleichgewicht strukturbezogener und wachstumsbezogener Proteine, sodass eine innere Organisation sichtbar wird, die bei Bulk-Tests verborgen bliebe.
Hinweise darauf, welches DCIS fortschreiten könnte
Die entscheidende Frage war, ob diese räumlichen Proteinmuster zukünftigen invasiven Krebs vorhersagen können. Beim Vergleich von Frauen, die später eine invasive Erkrankung entwickelten, mit denen, die dies nicht taten, zeigten sich bei Betrachtung von DCIS allein vorsichtige, aber statistisch eher moderate Unterschiede in Wachstums- und Strukturproteinen. Deutlichere Signale traten auf, wenn sie betrachteten, wie sich Proteinspiegel im DCIS im Vergleich zu nahegelegenen, normal aussehenden Gängen derselben Patientin verhielten. In Läsionen, die später invasiv wurden, verschob sich das Verhältnis bestimmter immunbezogener Proteine innerhalb der Gänge: Marker hilfreicher Killer-T-Zellen und zugehöriger Rezeptoren waren tendenziell niedriger, während ein Protein, das Immunreaktionen dämpfen kann, relativ höher war. Das deutet auf eine lokale Immunumgebung innerhalb der Gänge hin, die weniger gut in der Lage sein könnte, entstehende Krebszellen in Schach zu halten. 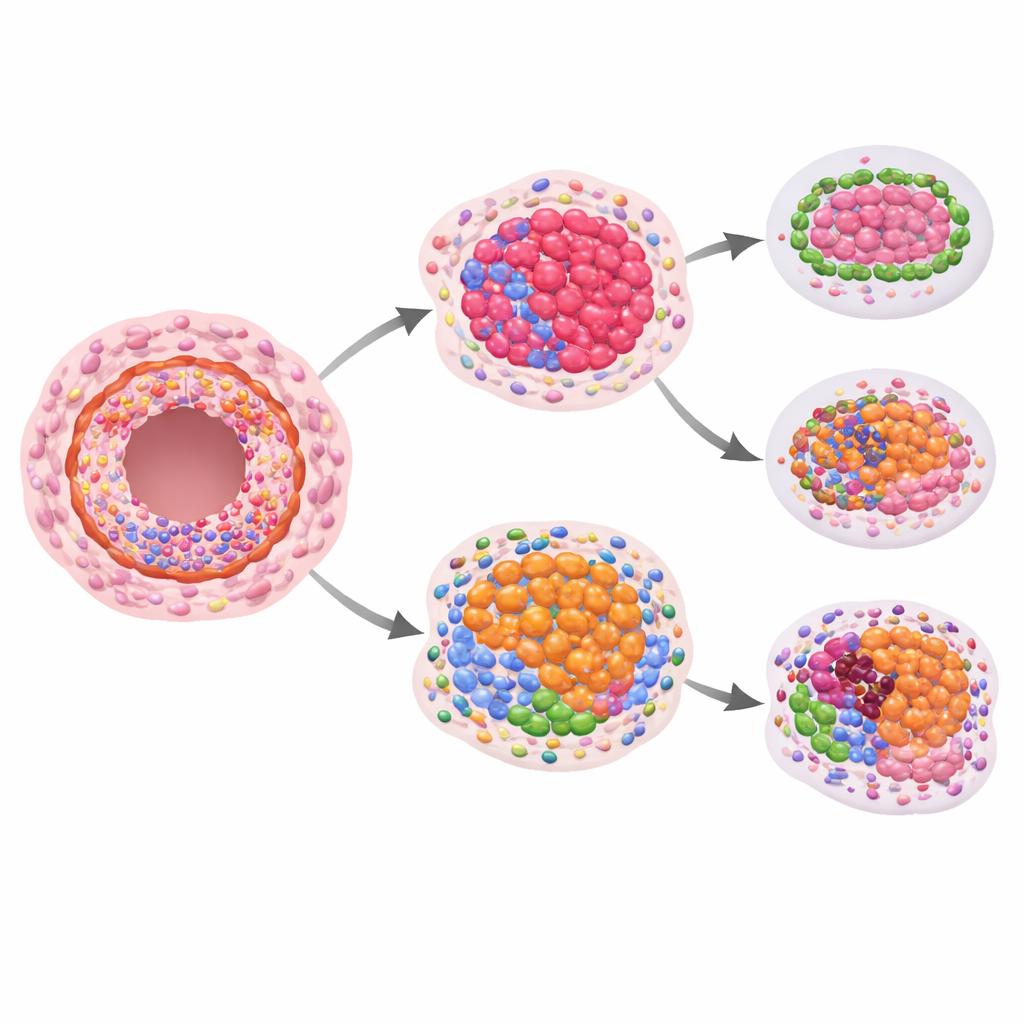
Wie Behandlung und Zeit Tumoren umgestalten
Für eine Teilgruppe von Patientinnen untersuchten die Forschenden außerdem Gewebe von späteren Ereignissen in derselben Brust – entweder eine weitere DCIS-Läsion oder ein invasiver Tumor – und verglichen diese mit dem ursprünglichen DCIS. In vielen Paaren waren Hormon- und HER2-Muster ähnlich, doch einige zeigten große Verschiebungen, darunter Fälle, in denen ein ER-hohes, HER2-niedriges DCIS von einem HER2-hohen, ER-niedrigen Rezidiv gefolgt wurde, oder in denen ein HER2-hohes DCIS von einem invasiven Krebs mit deutlich weniger HER2 gefolgt war. Einige dieser Veränderungen spiegeln wahrscheinlich völlig neue, unabhängig entstandene Tumoren wider und nicht eine lineare Evolution der ursprünglichen Läsion. Bei Frauen, die eine Hormontherapie erhielten, wiesen spätere Tumore häufig verringerte Spiegel von durch Östrogen getriebenen Proteinen auf, was darauf hindeutet, dass die Behandlung das molekulare Profil nachfolgender Erkrankungen verändern kann.
Was das für Patientinnen bedeutet
Die Studie zeigt, dass DCIS keine einheitliche Erkrankung ist, sondern ein Flickenteppich von Regionen mit Unterschieden in Hormonsignalgebung, Immunpräsenz und Zellverhalten, und dass diese Unterschiede für das zukünftige Risiko relevant sein können. Zwar trat kein einzelnes Protein als perfekte Vorhersage auf, doch hebt die Arbeit bestimmte Immunmarker innerhalb der Gänge sowie den Kontrast zwischen DCIS und benachbartem Normalgewebe als vielversprechende Bestandteile zukünftiger Risikobewertungen hervor. Durch das Hinzufügen dieser räumlichen Ebene zu bestehenden genetischen und klinischen Informationen hoffen Forschende, einer Zukunft näherzukommen, in der Frauen mit DCIS mit größerer Sicherheit mitgeteilt werden kann, ob sie eine sorgfältige Überwachung wählen können oder tatsächlich eine aggressive Behandlung benötigen.
Zitation: Marks, J.R., Dai, Y., King, L.M. et al. Spatial proteomics of breast ductal carcinoma in situ reveal distinct regional differences. Sci Rep 16, 13350 (2026). https://doi.org/10.1038/s41598-026-43486-9
Schlüsselwörter: duktales Carcinoma in situ, räumliche Proteomik, Brustkrebsrisiko, Tumormikroumgebung, Immunmarker