Clear Sky Science · tr
Meme kanallarında in situ duktal karsinomun mekânsal proteomikleri belirgin bölgesel farklılıkları ortaya koyuyor
Neden erken meme değişiklikleri önemli?
Duktal karsinom in situ (DKIS), rutin mamografilerde sıklıkla tespit edilen erken bir meme hastalığı biçimidir. Henüz süt kanallarından çevre dokuya sıçramamıştır, ancak bazı kadınlarda zamanla invaziv meme kanserine dönüşebilir. Şu anda doktorlar hangi DKIS lezyonlarının zararsız yolcular, hangilerinin gelecekte tehdit oluşturacağını güvenilir şekilde ayırt edemiyor; bu yüzden birçok hasta, gerekmeyebilecek ameliyat ve radyoterapi alıyor. Bu çalışma, DKIS içindeki ve çevresindeki protein dizilimlerinin hangi vakaların tehlikeli hâle gelme olasılığının daha yüksek olduğunu öngörmede yardımcı olabileceğini görmek için yeni, yüksek çözünürlüklü bir yaklaşım sunuyor.
Meme dokusunu bir harita gibi incelemek
Doku örneğini tek bir karışık örnek hâline getirmek yerine araştırmacılar, kaydırılmış slayt üzerinde özenle seçilmiş noktalarda onlarca proteini ölçen mekânsal proteomik adlı bir teknoloji kullandılar; neredeyse bir haritaya çivi çakmak gibi. DKIS için tedavi edilmiş 103 kadından arşivlenmiş dokuları incelediler; bazıları sonrasında daha fazla meme sorunu yaşamamış, bazıları aynı memede DKIS tekrarı geliştirmiş ve bazıları nihayetinde o memede invaziv kanser yaşamıştı. Her olguda patologlar DKIS kanallarının içindeki bölgeleri, yakın destekleyici dokuyu (stroma), normal görünümlü kanalları ve biyopsi bölgelerini işaretlediler. 1.200’den fazla böyle küçük bölgeden ekip hormon, büyüme, yapı ve immün aktivite ile ilişkili 53 proteini nicelendirerek her lezyon için ayrıntılı bir mekânsal portre oluşturdu. 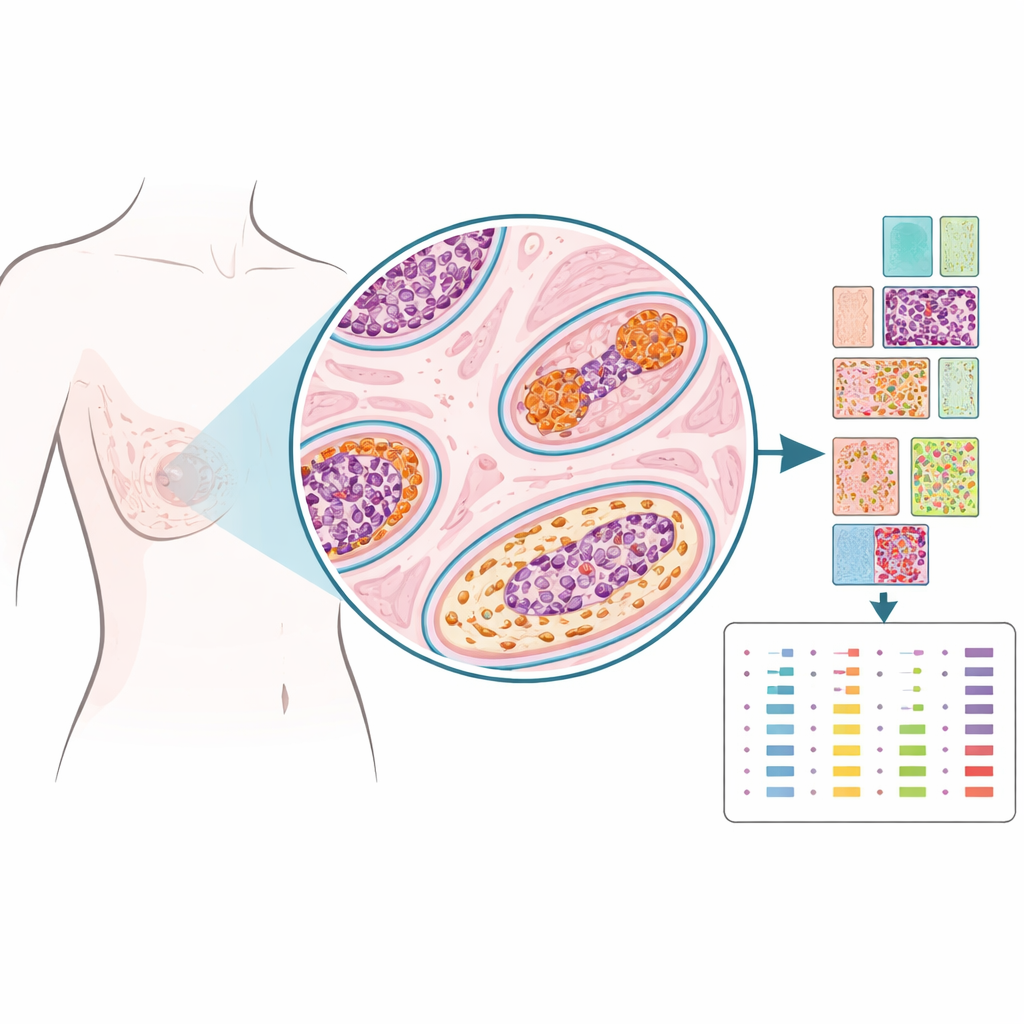
Erken lezyonların iki ana türü
Veriler, bilgisayara klinik ayrıntı hakkında bilgi vermeden gruplanınca çarpıcı bir desen ortaya çıktı. Çoğu DKIS örneği iki gruptan birine düştü: östrojen reseptörü (ER) yüksek ve büyüme faktörü reseptörü HER2 düşük olanlar; ve tersine düşük ER ve yüksek HER2 gösterenler. Bu ayrım, invaziv meme kanserlerinin sınıflandırılmasına benziyordu ama tamamen örtüşmüyordu. Normal görünümlü kanallar aynı keskin kümelenmeyi göstermedi ve DKIS etrafındaki destekleyici doku kendi özgün protein desenlerine sahipti. Çevreleyen stromada, ER-negatif DKIS’e bitişik alanlar genelde immün hücre belirteçleri bakımından zengindi; bu da ER-pozitif DKIS çevresindeki bölgelere kıyasla daha aktif bir immün mahalleye işaret ediyor olabilir.
Her kanal içinde gizli farklılıklar
Teknik tek bir kanal içindeki bölgeleri ayırabildiği için araştırmacılar ayrıca kanal kenarı ile merkezdeki protein düzeylerini karşılaştırdılar. Kanalın kasılabilen dış katmanı ve hücre bölünmesi ile ilişkili proteinler kenarda daha boldu; bu, kanal duvarına yakın hücrelerin özellikle aktif olduğunu gösteriyor. Buna karşılık enerji teminiyle ilişkili bir şeker taşıyıcısı kanal merkezinde daha yüksekti; bu, sıkışık iç hücrelerin farklı metabolik talepleri olduğunu düşündürüyor. Önemli olarak, genel hormon reseptörü düzeyleri merkez ile kenar arasında fazla değişmedi, ancak yapı ve büyümeyle ilişkili proteinlerin ince ölçekli dengesi değişti ve toplu testlerin kaçıracağı bir iç organizasyonu açığa çıkardı.
Hangi DKIS’in ilerleyebileceğine dair ipuçları
Ana soru, bu mekânsal protein desenlerinden herhangi birinin gelecekteki invaziv kanseri öngörüp öngörmediğiydi. İnvaziv hastalığa ilerleyenlerle ilerlemeyenleri karşılaştırdıklarında, ekip DKIS tek başına incelendiğinde büyüme ve yapı proteinlerinde işaretleyici ama istatistiksel olarak ılımlı farklılıklar gördü. Daha güçlü sinyaller, DKIS içindeki protein düzeylerinin aynı hastadaki yakın normal görünümlü kanallarla karşılaştırılmasında ortaya çıktı. Sonradan invaziv hâle gelen lezyonlarda, kanallar içindeki bazı immün ilişkili proteinlerin oranı değişti: yardımcı olduğu düşünülen öldürücü T hücre belirteçleri ve ilgili reseptörler genelde daha düşükken, immün yanıtları baskılayabilen bir protein göreli olarak daha yüksekti. Bu, kanallar içindeki yerel immün ortamın yeni ortaya çıkan kanser hücrelerini kontrol altında tutma yeteneğinin daha zayıf olabileceğine işaret ediyor. 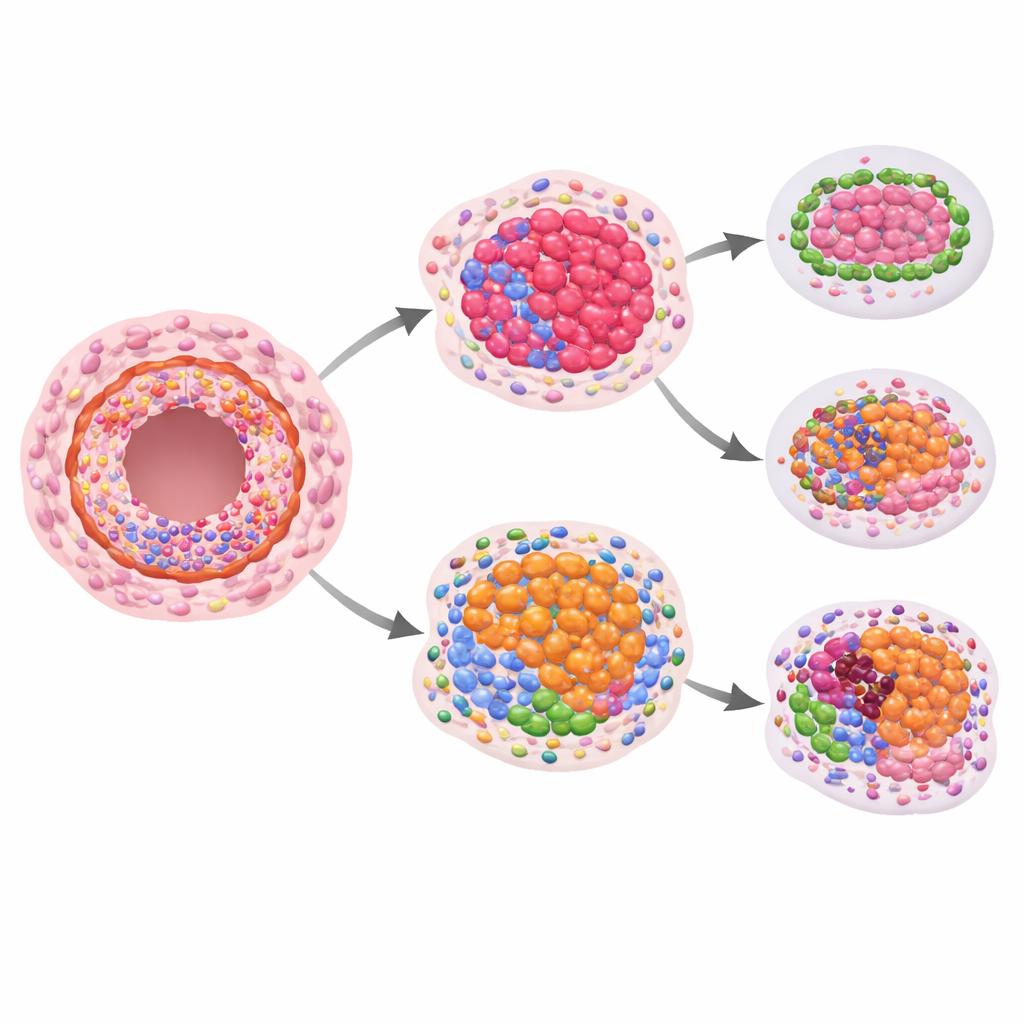
Tedavi ve zamanın tümörleri nasıl yeniden şekillendirdiği
Araştırmacılar, bazı hastalar için aynı memedeki daha sonraki olaylardan —ya başka bir DKIS lezyonu ya da invaziv tümör— alınan dokuları da inceleyip bunları orijinal DKIS ile karşılaştırdılar. Birçok çiftte hormon ve HER2 desenleri benzerdiyken, bazılarında büyük değişimler görüldü; örneğin ER-yüksek, HER2-düşük bir DKIS’i takiben HER2-yüksek, ER-düşük bir nüks veya HER2-yüksek DKIS’in ardından çok daha az HER2 içeren bir invaziv kanser gibi. Bu değişimlerin bir kısmı, orijinal lezyonun doğrusal evrimi yerine tamamen bağımsız yeni tümörlerin ortaya çıkmasını yansıtıyor olabilir. Hormon terapisi alan kadınlarda ise sonraki kanserler sıklıkla östrojen tarafından yönlendirilen proteinlerin azaldığını gösteriyordu; bu da tedavinin sonraki hastalığın moleküler profilini yeniden şekillendirebileceğini düşündürüyor.
Bu hastalar için ne anlama geliyor?
Çalışma, DKIS’in tek tip bir durum olmadığını; hormon sinyalleşmesi, immün varlık ve hücre davranışı bakımından farklılık gösteren bir bölge yaması olduğunu ve bu farklılıkların gelecekteki risk açısından önemli olabileceğini gösteriyor. Hiçbir tek proteinin mükemmel bir kehanet aracı olarak ortaya çıkmamasıyla birlikte, çalışma kanallar içindeki belirli immün belirteçleri ve DKIS ile bitişik normal doku arasındaki kontrastı gelecekteki risk skorları için umut verici bileşenler olarak öne çıkarıyor. Bu mekânsal katmanı mevcut genetik ve klinik bilgilerle birleştirerek araştırmacılar, DKIS’li kadınlara dikkatli takip ile güvenle izlenebilecekleri ya da gerçekten agresif tedaviye ihtiyaç duydukları konusunda daha fazla güvenle yol gösterilebilecek bir geleceğe doğru ilerlemeyi umuyorlar.
Atıf: Marks, J.R., Dai, Y., King, L.M. et al. Spatial proteomics of breast ductal carcinoma in situ reveal distinct regional differences. Sci Rep 16, 13350 (2026). https://doi.org/10.1038/s41598-026-43486-9
Anahtar kelimeler: in situ duktal karsinom, mekânsal proteomik, meme kanseri riski, tümör mikroçevresi, immün belirteçler