Clear Sky Science · fr
Protéomique spatiale du carcinome canalinaire in situ du sein révèle des différences régionales distinctes
Pourquoi les premiers changements mammaires comptent
Le carcinome canalulaire in situ (CCIS) est une forme précoce de maladie du sein souvent détectée lors de mammographies de routine. Il n’a pas encore franchi la paroi des canaux galactophores pour envahir les tissus environnants, mais chez certaines femmes il évolue finalement vers un cancer invasif du sein. Aujourd’hui, les médecins ne peuvent pas dire de façon fiable quels foyers de CCIS sont des anomalies bénignes et lesquels deviendront dangereux, si bien que de nombreuses patientes subissent des chirurgies et des radiothérapies peut‑être non nécessaires. Cette étude propose un regard nouveau et à haute résolution sur le CCIS pour examiner comment la répartition des protéines dans et autour de ces canaux pourrait aider à prédire quels cas sont les plus susceptibles de devenir dangereux.
Observer le tissu mammaire comme une carte
Plutôt que d’écraser le tissu pour obtenir un échantillon homogène, les chercheurs ont utilisé une technologie appelée protéomique spatiale pour mesurer des dizaines de protéines à des points précisément choisis sur la lame, presque comme poser des épingles sur une carte. Ils ont examiné des tissus archivés de 103 femmes traitées pour CCIS, dont certaines n’ont pas eu de problèmes mammaires ultérieurs, d’autres ont présenté un nouveau CCIS dans le même sein, et d’autres encore ont développé par la suite un cancer invasif dans ce sein. Pour chaque cas, des pathologistes ont délimité des régions à l’intérieur des canaux atteints de CCIS, le tissu de soutien adjacent (stroma), des canaux à l’aspect normal et les zones de biopsie. À partir de plus de 1 200 de ces micro‑régions, l’équipe a quantifié 53 protéines liées aux hormones, à la croissance, à la structure et à l’activité immunitaire, créant un portrait spatial détaillé de chaque lésion. 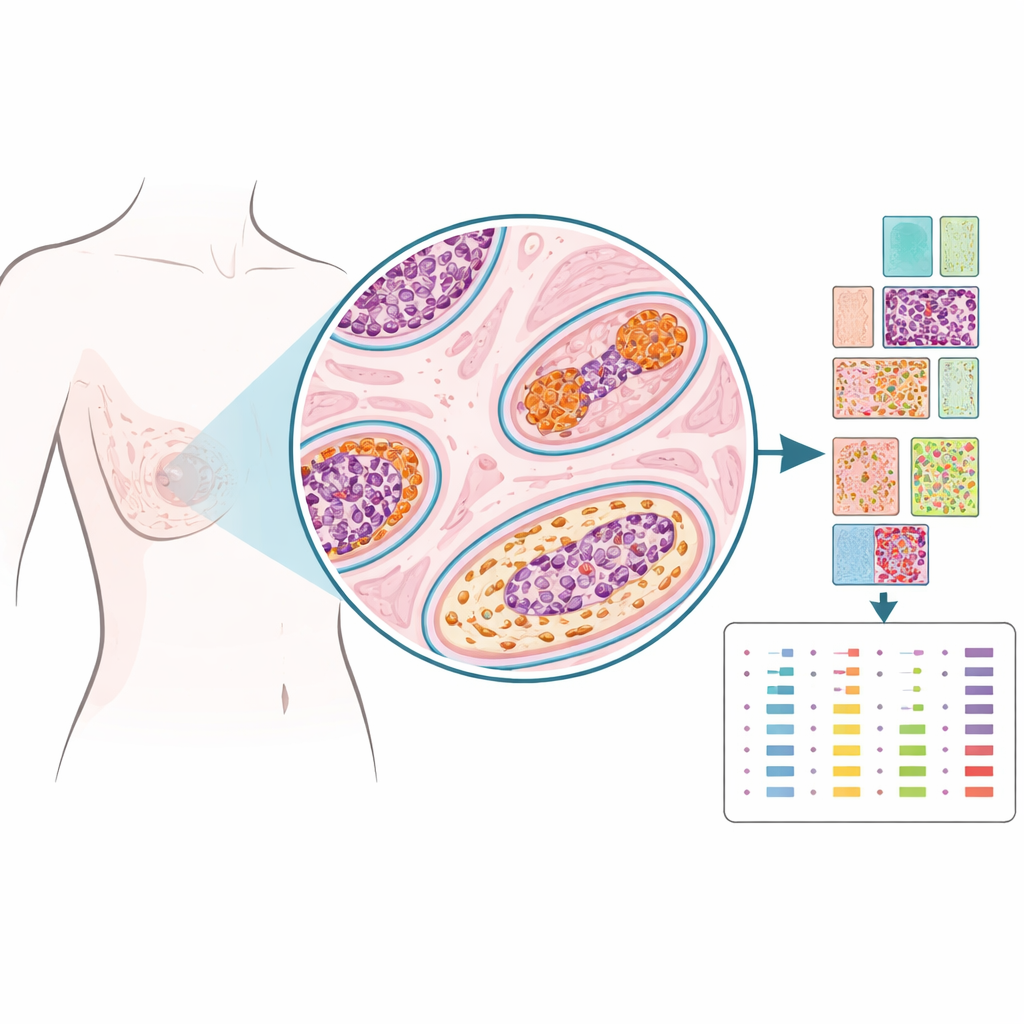
Deux grands types de lésions précoces
Lorsque l’équipe a regroupé les données sans fournir d’informations cliniques au logiciel, un schéma frappant est apparu. La plupart des échantillons de CCIS appartenaient à l’un des deux groupes : ceux avec des taux élevés de récepteur aux œstrogènes (ER) et des niveaux faibles du récepteur du facteur de croissance HER2, et ceux avec le schéma inverse, faibles en ER et riches en HER2. Cette séparation ressemblait, sans être identique, à la classification des cancers du sein invasifs. Les canaux à l’aspect normal ne montraient pas le même regroupement net, et le tissu de soutien autour du CCIS présentait ses propres profils protéiques distincts. Dans le stroma voisin, les zones adjacentes au CCIS ER‑négatif avaient tendance à être riches en marqueurs de cellules immunitaires, suggérant un environnement immunitaire plus actif comparé aux régions entourant un CCIS ER‑positif.
Différences cachées à l’intérieur de chaque canal
Parce que la technique pouvait séparer des régions au sein d’un même canal, les chercheurs ont aussi comparé les niveaux de protéines au bord du canal et au centre. Les protéines associées à la couche externe contractile du canal et à la division cellulaire étaient plus abondantes en périphérie, ce qui suggère que les cellules en contact avec la paroi du canal sont particulièrement actives. En revanche, un transporteur de glucose lié à l’approvisionnement en énergie était plus élevé au centre du canal, évoquant des besoins métaboliques différents pour les cellules intérieures plus compactes. Notamment, les niveaux globaux des récepteurs hormonaux variaient peu entre le centre et la périphérie, mais l’équilibre à fine échelle des protéines structurelles et liées à la croissance changeait, révélant une organisation interne que les tests en vrac ne pourraient pas détecter.
Indices sur les CCIS susceptibles d’évoluer
La question clé était de savoir si certains de ces schémas protéiques spatiaux annonçaient un futur cancer invasif. En comparant les femmes qui ont développé une maladie invasive à celles qui ne l’ont pas fait, les chercheurs ont observé des différences suggestives mais statistiquement modestes dans des protéines de croissance et de structure en examinant le CCIS seul. Des signaux plus forts sont apparus lorsqu’ils ont comparé les niveaux protéiques dans le CCIS avec ceux des canaux à l’aspect normal du même patient. Dans les lésions qui sont devenues invasives, le rapport de certaines protéines liées au système immunitaire à l’intérieur des canaux s’est modifié : des marqueurs des cellules T‑cytotoxiques utiles et de leurs récepteurs avaient tendance à être plus faibles, tandis qu’une protéine capable d’atténuer la réponse immunitaire était relativement plus élevée. Cela suggère un microenvironnement immunitaire local à l’intérieur des canaux peut‑être moins apte à contenir les cellules cancéreuses naissantes. 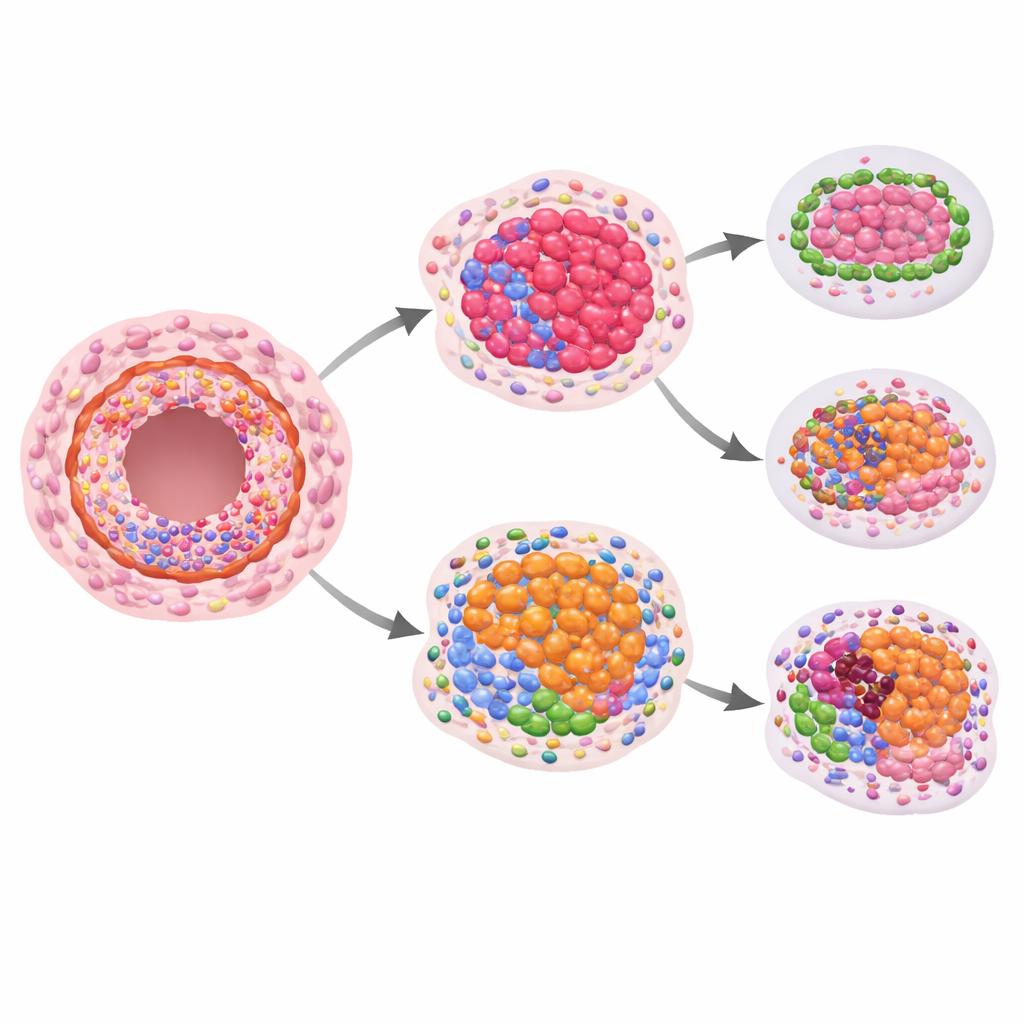
Comment le traitement et le temps remodelent les tumeurs
Pour un sous‑groupe de patientes, les investigateurs ont également étudié des tissus issus d’événements ultérieurs dans le même sein — soit un autre foyer de CCIS soit une tumeur invasive — et les ont comparés au CCIS initial. Dans de nombreuses paires, les profils hormonaux et HER2 étaient similaires, mais certaines ont montré des changements majeurs, y compris des cas où un CCIS ER‑haut, HER2‑faible a été suivi par une récidive HER2‑haute, ER‑faible, ou où un CCIS HER2‑haut a été suivi par un cancer invasif avec beaucoup moins de HER2. Certains de ces changements reflètent probablement l’émergence de tumeurs entièrement nouvelles indépendantes plutôt qu’une évolution linéaire de la lésion d’origine. Chez les femmes ayant reçu un traitement hormonal, les cancers ultérieurs présentaient souvent des niveaux réduits de protéines sous contrôle des œstrogènes, ce qui suggère que le traitement peut remodeler le profil moléculaire des maladies subséquentes.
Ce que cela signifie pour les patientes
L’étude montre que le CCIS n’est pas une condition uniforme, mais une mosaïque de régions qui diffèrent par la signalisation hormonale, la présence immunitaire et le comportement cellulaire, et que ces différences peuvent avoir une importance pour le risque futur. Bien qu’aucune protéine unique ne se soit révélée une boule de cristal parfaite, ce travail met en évidence des marqueurs immunitaires spécifiques à l’intérieur des canaux — ainsi que le contraste entre le CCIS et le tissu normal adjacent — comme ingrédients prometteurs pour de futurs scores de risque. En ajoutant cette couche spatiale aux informations génétiques et cliniques existantes, les chercheurs espèrent avancer vers un avenir où les femmes atteintes de CCIS pourront savoir, avec plus de confiance, si une surveillance attentive suffit ou si un traitement agressif est réellement nécessaire.
Citation: Marks, J.R., Dai, Y., King, L.M. et al. Spatial proteomics of breast ductal carcinoma in situ reveal distinct regional differences. Sci Rep 16, 13350 (2026). https://doi.org/10.1038/s41598-026-43486-9
Mots-clés: carcinome canalinaire in situ, protéomique spatiale, risque de cancer du sein, microenvironnement tumoral, marqueurs immunitaires