Clear Sky Science · ar
البروتيوميات المكانية للسرطان القنوي داخل القناة في الثدي تكشف فروقًا إقليمية مميزة
لماذا تهم التغيرات المبكرة في الثدي
السرطان القنوي داخل القناة (DCIS) هو شكل مبكر من أمراض الثدي يُكتشف غالبًا في صور الماموغرام الروتيني. لم يتجاوز بعد قنوات الحليب إلى الأنسجة المحيطة، لكن لدى بعض النساء يتطور لاحقًا إلى سرطان ثدي غازي. حتى الآن، لا يستطيع الأطباء التمييز بشكل موثوق أي آفات DCIS غير ضارة وأيها يشكل تهديدًا في المستقبل، لذا يتلقى العديد من المريضات جراحات وإشعاعًا قد لا يكن بحاجة حقيقية إليهما. تقدم هذه الدراسة نظرة جديدة عالية الدقة على DCIS لمعرفة كيف يمكن لترتيب البروتينات داخل وحول هذه القنوات أن يساعد في التنبؤ بأي الحالات أكثر احتمالًا لأن تصبح خطيرة.
النظر إلى نسيج الثدي كخريطة
بدلًا من طحن النسيج إلى عينة مدموجة واحدة، استخدم الباحثون تقنية تُدعى البروتيوميات المكانية لقياس العشرات من البروتينات في نقاط مختارة بدقة على الشريحة، كما لو أنهم يضعون دبابيس على خريطة. فحصوا نسيجًا محفوظًا من 103 نساء عولجن من DCIS، بعضهن لم تتعرضن لمشكلات ثدي لاحقة، وبعضهن طُورت لديهن DCIS مرة أخرى في نفس الثدي، وبعضهن تطور لديهن لاحقًا سرطان غازي في ذلك الثدي. في كل حالة، وضع الأطباء الشرعيون علامات على مناطق داخل قنوات DCIS، والنسيج الداعم القريب (الستروما)، والقنوات ذات المظهر الطبيعي، ومواقع الخزعة. من أكثر من 1200 منطقة صغيرة من هذا النوع، قاس الفريق 53 بروتينًا مرتبطة بالهرمونات والنمو والبنية والنشاط المناعي، مكوّنين بورتريهًا مكانيًا مفصّلًا لكل آفة. 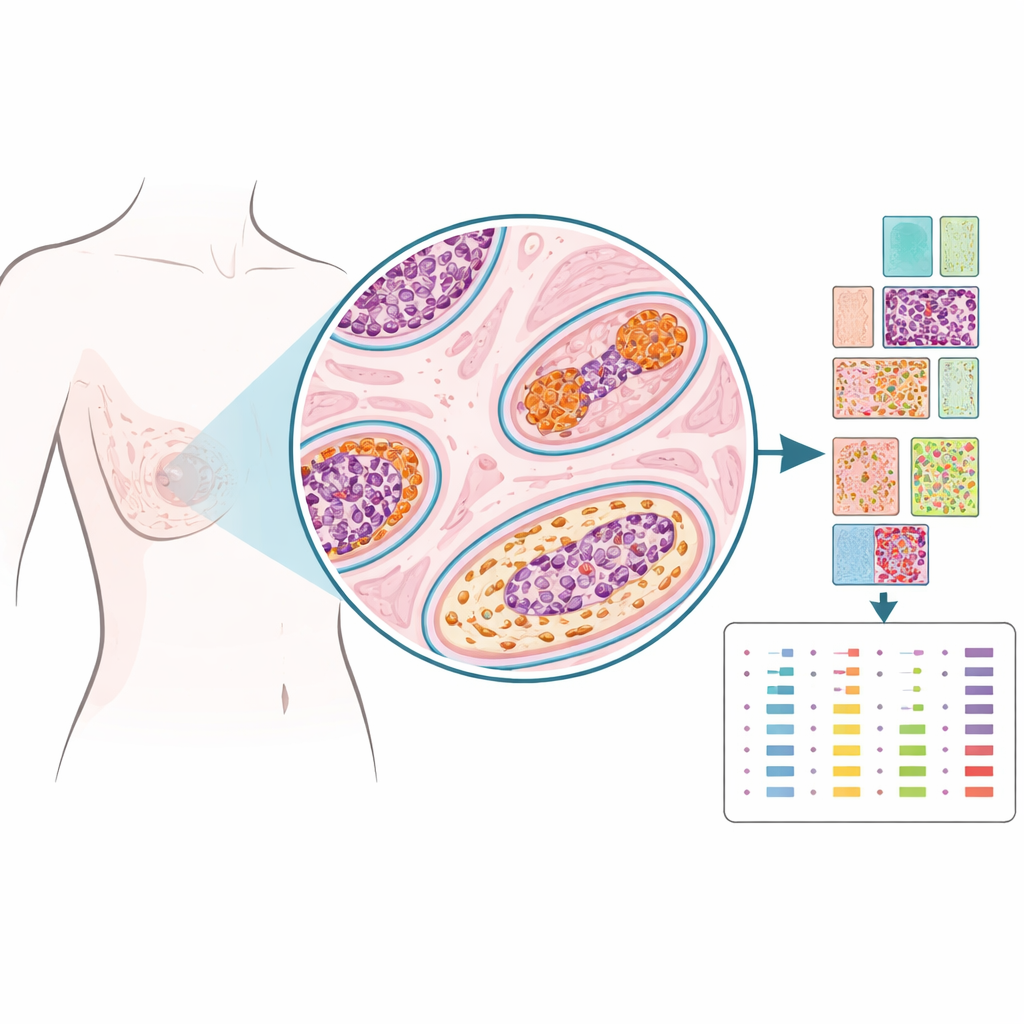
نوعان رئيسيان من الآفات المبكرة
عندما جمع الفريق البيانات دون تزويد الحاسوب بأي تفاصيل سريرية، برز نمط لافت. انقسمت غالبية عينات DCIS إلى إحدى مجموعتين: تلك ذات مستويات مرتفعة لمستقبل الإستروجين (ER) ومستويات منخفضة لمستقبل عامل النمو HER2، وتلك ذات النمط المعاكس — مستويات منخفضة من ER ومرتفعة من HER2. يشبه هذا الانقسام، لكنه ليس متماثلًا تمامًا مع الطريقة التي تُصنَّف بها سرطانات الثدي الغازية. القنوات ذات المظهر الطبيعي لم تُظهر نفس التجمع الحاد، وأظهر النسيج الداعم المحيط بـDCIS أنماط بروتينية مميزة بحد ذاته. في الستروما المحيطة، بدت المناطق بجانب DCIS السلبي لمستقبل الإستروجين غنية بعلامات الخلايا المناعية، مما يشير إلى حيّز مناعي أكثر نشاطًا مقارنة بالمناطق حول DCIS الإيجابي لمستقبل الإستروجين.
فروق خفية داخل كل قناة
لأن التقنية تمكنت من فصل مناطق داخل قناة واحدة، قارن الباحثون أيضًا مستويات البروتين عند حافة القناة بتلك في المركز. كانت البروتينات المرتبطة بطبقة القناة الخارجي الانقباضية وانقسام الخلايا أكثر وفرة عند المحيط، مما يوحي بأن الخلايا الملتصقة بجدار القناة أكثر نشاطًا. في المقابل، كان ناقل سكر مرتبطًا بإمداد الطاقة أعلى في مركز القناة، في إشارة إلى متطلبات أيضية مختلفة في الخلايا الداخلية المزدحمة. وبشكل ملحوظ، لم تتغير مستويات مستقبلات الهرمونات الإجمالية كثيرًا بين المركز والحافة، لكن توازن البروتينات البنيوية والمُحفِّزة للنمو على مقياس دقيق تغير، كاشفًا عن تنظيم داخلي قد تغيب عنه الاختبارات الإجمالية.
دلائل على أي DCIS قد يتقدم
السؤال الرئيسي كان ما إذا كانت أي من هذه الأنماط البروتينية المكانية تتنبأ بسرطان غازي في المستقبل. بمقارنة النساء اللاتي تطور لديهن مرض غازي مع تلك اللاتي لم يتطور لديهن، رصد الباحثون اختلافات مقترحة لكنها متواضعة إحصائيًا في بروتينات النمو والبنية عند النظر إلى DCIS وحده. ظهرت إشارات أقوى عندما نظروا إلى كيفية مقارنة مستويات البروتين في DCIS مع القنوات ذات المظهر الطبيعي المجاورة من نفس المريضة. في الآفات التي أصبحت غازية لاحقًا، تغيّر نسق نسبة بعض البروتينات المرتبطة بالمناعة داخل القنوات: كانت علامات الخلايا القاتلة التائية المفيدة والمستقبلات المرتبطة بها تميل إلى أن تكون أَقل، بينما كان بروتين يمكنه كبح الاستجابات المناعية أعلى نسبيًا. هذا يشير إلى بيئة مناعية محلية داخل القنوات قد تكون أقل قدرة على كبح الخلايا السرطانية الناشئة. 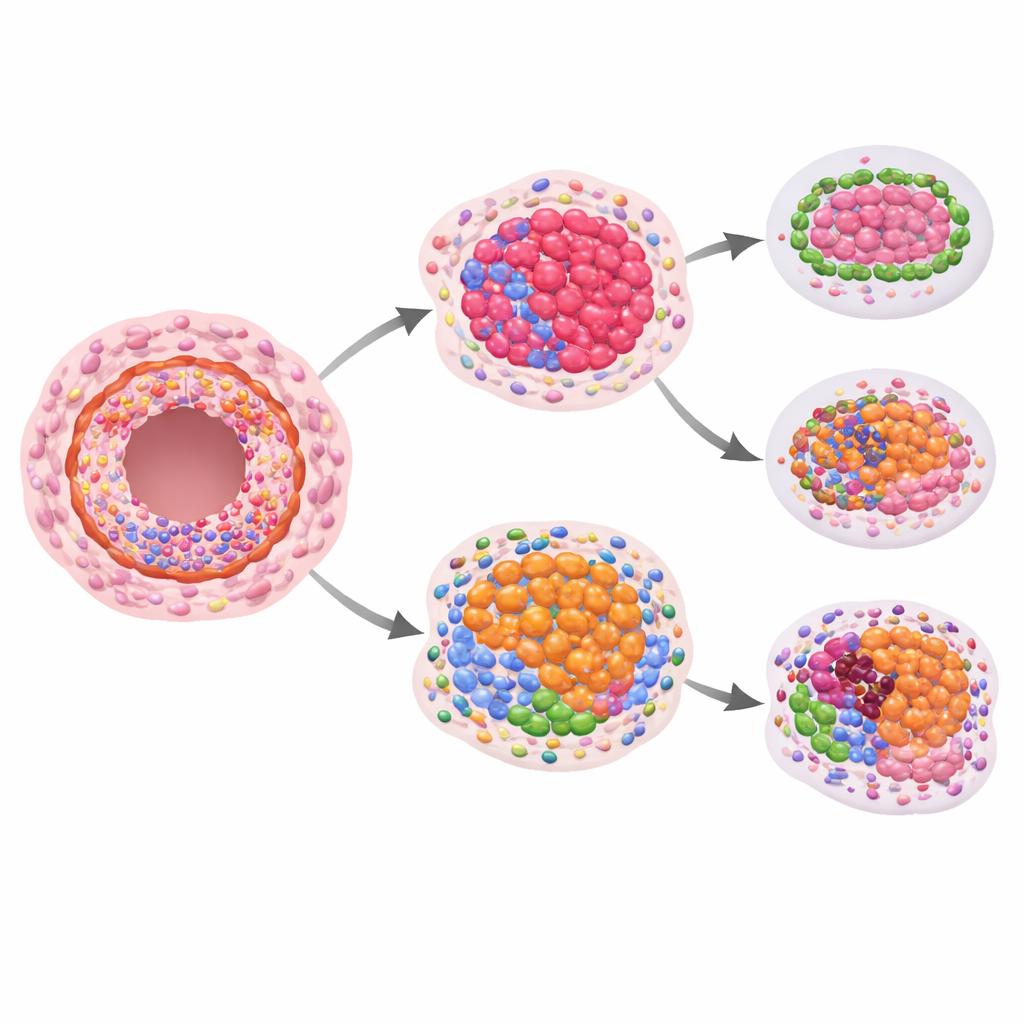
كيف يعيد العلاج والوقت تشكيل الأورام
لفئة فرعية من المريضات، درس الباحثون أيضًا نسيجًا من أحداث لاحقة في نفس الثدي — إما آفة DCIS أخرى أو ورم غازي — وقارنوها مع DCIS الأصلي. في كثير من الأزواج، كانت أنماط الهرمون وHER2 متشابهة، لكن بعض العينات أظهرت تحولات كبيرة، بما في ذلك حالات حيث أعقب DCIS عالي ER ومنخفض HER2 تكرار كان عالي HER2 ومنخفض ER، أو حيث أعقب DCIS عالي HER2 سرطان غازي به مستوى HER2 أقل بكثير. من المرجح أن تعكس بعض هذه التغيرات أورامًا جديدة تنشأ بشكل مستقل بدلاً من تطور خطي للآفة الأصلية. بين النساء اللائي تلقين علاجًا هرمونيًا، كانت الأورام اللاحقة غالبًا ما تُظهر مستويات أقل من البروتينات المدفوعة بالإستروجين، مما يشير إلى أن العلاج يمكن أن يعيد تشكيل الملف الجزيئي للمرض اللاحق.
ماذا يعني هذا للمرضى
تُظهر الدراسة أن DCIS ليست حالة موحدة، بل رقعة من المناطق المختلفة بحسب إشارة الهرمونات، والحضور المناعي، وسلوك الخلايا، وأن هذه الاختلافات قد تكون مهمة للمخاطر المستقبلية. مع أنه لم يظهر بروتين واحد ككرة بلورية مثالية، تسلط النتائج الضوء على علامات مناعية محددة داخل القنوات—إلى جانب التباين بين DCIS والنسيج الطبيعي المجاور—كعناصر واعدة لدرجات المخاطر المستقبلية. بإضافة هذا البُعد المكاني إلى المعلومات الجينية والسريرية الحالية، يأمل الباحثون في التقدم نحو مستقبل يمكن فيه إخبار النساء المصابات بـDCIS، بثقة أكبر، ما إذا كان بإمكانهن اختيار المراقبة الدقيقة بأمان أو أنهن بحاجة فعلًا إلى علاج مكثف.
الاستشهاد: Marks, J.R., Dai, Y., King, L.M. et al. Spatial proteomics of breast ductal carcinoma in situ reveal distinct regional differences. Sci Rep 16, 13350 (2026). https://doi.org/10.1038/s41598-026-43486-9
الكلمات المفتاحية: السرطان القنوي داخل القناة, البروتيوميات المكانية, مخاطر سرطان الثدي, البيئة الدقيقة للورم, علامات مناعية