Clear Sky Science · ru
Пространственный протеомный анализ внутрипротоковой карциномы молочной железы показывает отчетливые региональные различия
Почему важны ранние изменения в молочной железе
Внутрипротоковая карцинома молочной железы (DCIS) — ранняя форма заболевания, которую часто обнаруживают при плановой маммографии. Она пока не проросла за пределы молочных протоков в окружающие ткани, но у некоторых женщин со временем приводит к инвазивному раку молочной железы. В настоящее время врачи не могут с уверенностью отличить доброкачественные, неопасные очаги DCIS от тех, которые представляют угрозу, поэтому многие пациентки получают операции и лучевую терапию, которые им, возможно, не нужны. В этом исследовании применен новый высокоразрешающий подход к DCIS, чтобы выяснить, как расположение белков внутри и вокруг протоков может помочь прогнозировать, какие случаи с большей вероятностью станут опасными.
Рассматривать ткань молочной железы как карту
Вместо того чтобы перемалывать ткань в однородную смесь, исследователи использовали технологию пространственной протеомики для измерения десятков белков в точно выбранных точках на срезе, почти как устанавливая метки на карте. Они изучили архивные образцы от 103 женщин, лечившихся по поводу DCIS: у некоторых больше не возникало проблем с грудью, у некоторых позже появлялся повторный DCIS в той же груди, а у некоторых впоследствии развивался инвазивный рак в этой же груди. Патологи отметили области внутри протоков с DCIS, рядом в поддерживающей ткани (строме), нормальные по виду протоки и места биопсии. Из более чем 1 200 таких крошечных областей команда количественно определила 53 белка, связанных с гормональным статусом, фактором роста, структурой и иммунной активностью, создав детализированный пространственный портрет каждой опухоли. 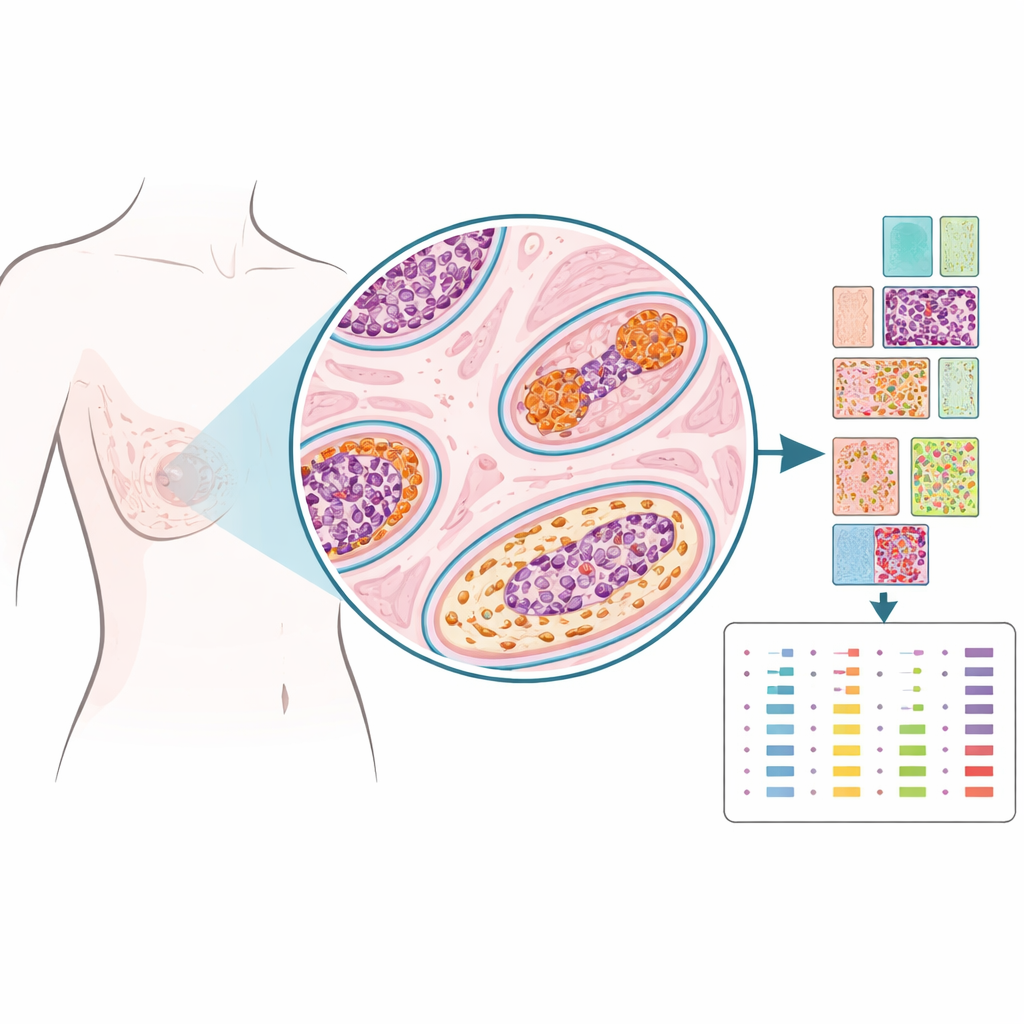
Два основных типа ранних поражений
Когда команда сгруппировала данные без какой‑либо клинической предустановки, выявилась яркая закономерность. Большинство образцов DCIS распределились в одну из двух групп: с высоким уровнем рецептора эстрогена (ER) и низким уровнем рецептора роста HER2, и с противоположным профилем — низким ER и высоким HER2. Это деление напоминало, но не полностью совпадало с классификацией инвазивных раков молочной железы. Нормально выглядящие протоки не демонстрировали такой четкой кластеризации, а поддерживающая ткань вокруг DCIS имела собственные отличительные белковые профили. В окружающей строме области рядом с ER‑негативным DCIS чаще были богаты маркерами иммунных клеток, что указывает на более активное иммунное окружение по сравнению с регионами вокруг ER‑позитивного DCIS.
Скрытые различия внутри каждого протока
Поскольку метод позволял разделять области внутри одного протока, исследователи также сравнили уровни белков на краю протока и в его центре. Белки, связанные с сократительным наружным слоем протока и делением клеток, были более выражены на периферии, что подразумевает повышенную активность клеток, прилегающих к стенке протока. Напротив, транспортер сахара, связанный с энергетическим обеспечением, был выше в центре протока, намекая на различные метаболические потребности у более плотно расположенных внутренних клеток. Примечательно, что общие уровни гормональных рецепторов существенно не менялись между центром и краем, но тонкое соотношение структурных и ростовых белков изменялось, выявляя внутреннюю организацию, которую маскируют анализы цельных образцов.
Подсказки о том, какой DCIS может прогрессировать
Ключевой вопрос заключался в том, предвещают ли какие‑то пространственные белковые паттерны будущую инвазию. Сравнивая женщин, у которых впоследствии развивалось инвазивное заболевание, с теми, у кого этого не было, исследователи обнаружили наводящие, но статистически умеренные различия в белках, связанных с ростом и структурой, при рассмотрении только DCIS. Более сильные сигналы появлялись, когда они сравнивали уровни белков в DCIS с соседними нормально выглядящими протоками у той же пациентки. В поражениях, которые позднее стали инвазивными, соотношение определенных иммунных белков внутри протоков сдвигалось: маркеры цитотоксических T‑клеток и соответствующих рецепторов, как правило, были ниже, тогда как белок, способный подавлять иммунный ответ, был относительно выше. Это указывает на локальную иммунную среду внутри протоков, которая может быть менее способна сдерживать появляющиеся раковые клетки. 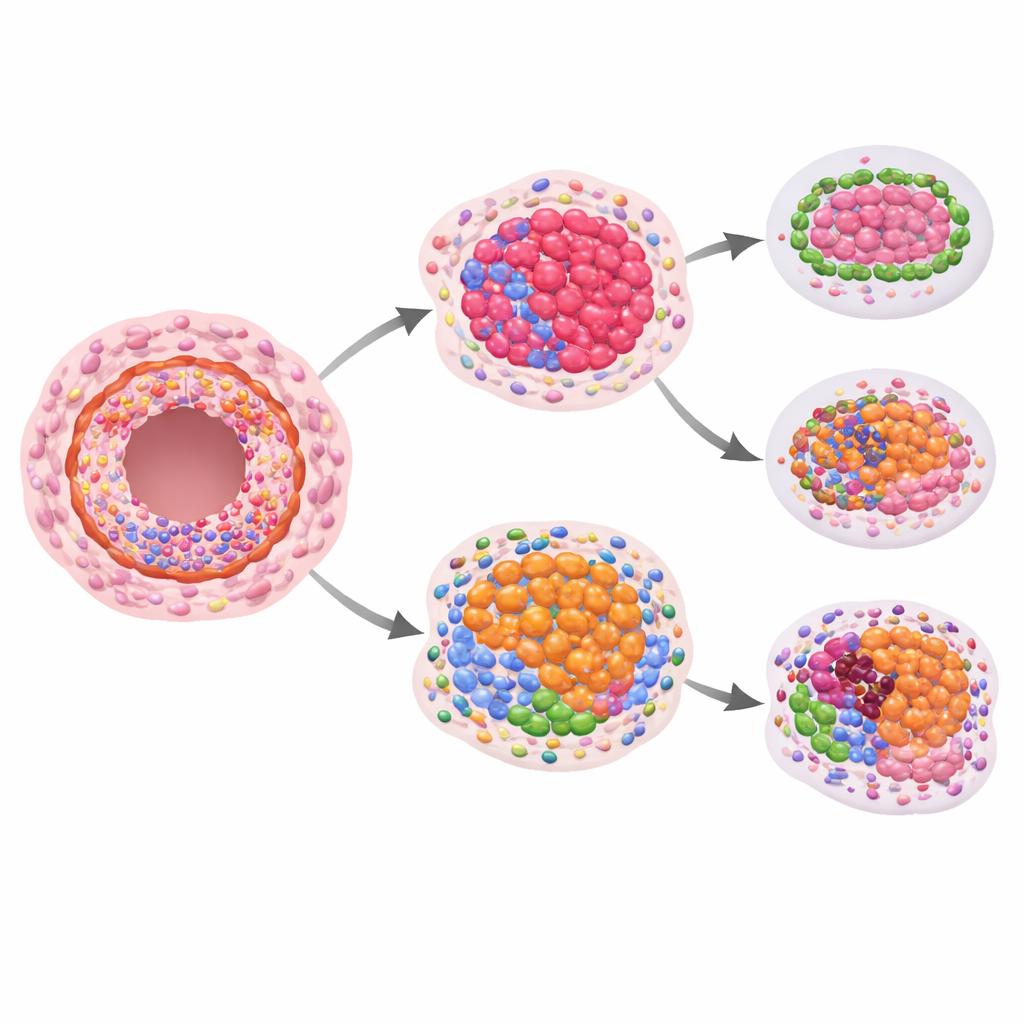
Как лечение и время меняют опухоли
Для подмножества пациенток исследователи также изучали ткань из последующих событий в той же груди — либо повторного DCIS, либо инвазивной опухоли — и сравнивали их с исходным DCIS. Во многих парах гормональные и HER2‑паттерны были схожи, но в некоторых наблюдались значительные сдвиги, включая случаи, когда DCIS с высоким ER и низким HER2 сопровождался рецидивом с высоким HER2 и низким ER, или когда HER2‑высокий DCIS позже сопровождался инвазивной опухолью с гораздо меньшим уровнем HER2. Некоторые из этих изменений, вероятно, отражают появление совершенно новых опухолей, возникающих независимо, а не прямую эволюцию исходного очага. Среди женщин, получавших гормональную терапию, в последующих опухолях часто отмечали снижение уровней белков, управляемых эстрогеном, что говорит о том, что лечение может перестраивать молекулярный профиль последующего заболевания.
Что это означает для пациенток
Исследование показывает, что DCIS не является однородным состоянием, а представляет собой мозаику регионов, различающихся по гормональной сигнализации, присутствию иммунных элементов и поведению клеток, и что эти различия могут иметь значение для будущего риска. Хотя ни один белок не выступил в роли совершенного провидца, работа выделяет конкретные иммунные маркеры внутри протоков — а также контраст между DCIS и соседними нормальными тканями — как перспективные компоненты будущих оценок риска. Добавляя этот пространственный слой к существующим генетическим и клиническим данным, исследователи надеются продвинуться к будущему, в котором женщинам с DCIS можно будет с большей уверенностью сообщать, можно ли безопасно выбрать наблюдение или действительно необходимо агрессивное лечение.
Цитирование: Marks, J.R., Dai, Y., King, L.M. et al. Spatial proteomics of breast ductal carcinoma in situ reveal distinct regional differences. Sci Rep 16, 13350 (2026). https://doi.org/10.1038/s41598-026-43486-9
Ключевые слова: внутрипротоковая карцинома (DCIS), пространственная протеомика, риск рака молочной железы, опухолевая микросреда, иммунные маркеры