Clear Sky Science · pl
Proteomika przestrzenna in situ raka przewodowego piersi ujawnia wyraźne regionalne różnice
Dlaczego wczesne zmiany w piersi mają znaczenie
Rak przewodowy in situ (DCIS) to wczesna postać choroby piersi często wykrywana przy rutynowych mammografiach. Nie wydostał się jeszcze z przewodów mlecznych do otaczających tkanek, ale u niektórych kobiet może ostatecznie przekształcić się w raka inwazyjnego. Obecnie lekarze nie są w stanie wiarygodnie odróżnić zmian DCIS, które są bezpiecznymi „pasażerami”, od tych, które stanowią przyszłe zagrożenie, więc wiele pacjentek otrzymuje zabiegi chirurgiczne i radioterapię, które mogą być niepotrzebne. W tym badaniu zastosowano nowe, wysokorozdzielcze podejście do DCIS, aby sprawdzić, czy rozmieszczenie białek w obrębie i wokół przewodów może pomóc przewidzieć, które przypadki mają większe ryzyko stania się niebezpieczne.
Oglądanie tkanki piersi jak mapy
Zamiast rozdrabniać tkankę do jednego zmiksowanego próbki, badacze użyli technologii zwanej proteomiką przestrzenną, by zmierzyć dziesiątki białek w precyzyjnie wybranych punktach na preparacie — niemal jak umieszczanie pinezek na mapie. Zbadali archiwalne próbki od 103 kobiet leczonych z powodu DCIS: u niektórych nie wystąpiły późniejsze problemy z piersią, u niektórych nawrót DCIS pojawił się w tej samej piersi, a u innych w końcu rozwinął się rak inwazyjny. Patolodzy oznaczyli w każdym przypadku obszary wewnątrz przewodów z DCIS, pobliską tkankę podporową (stroma), przewody wyglądające na normalne oraz miejsca biopsji. Z ponad 1 200 takich maleńkich regionów zespół ilościowo określił 53 białka związane z hormonami, czynnikami wzrostu, strukturą i aktywnością układu odpornościowego, tworząc szczegółowy przestrzenny portret każdej zmiany. 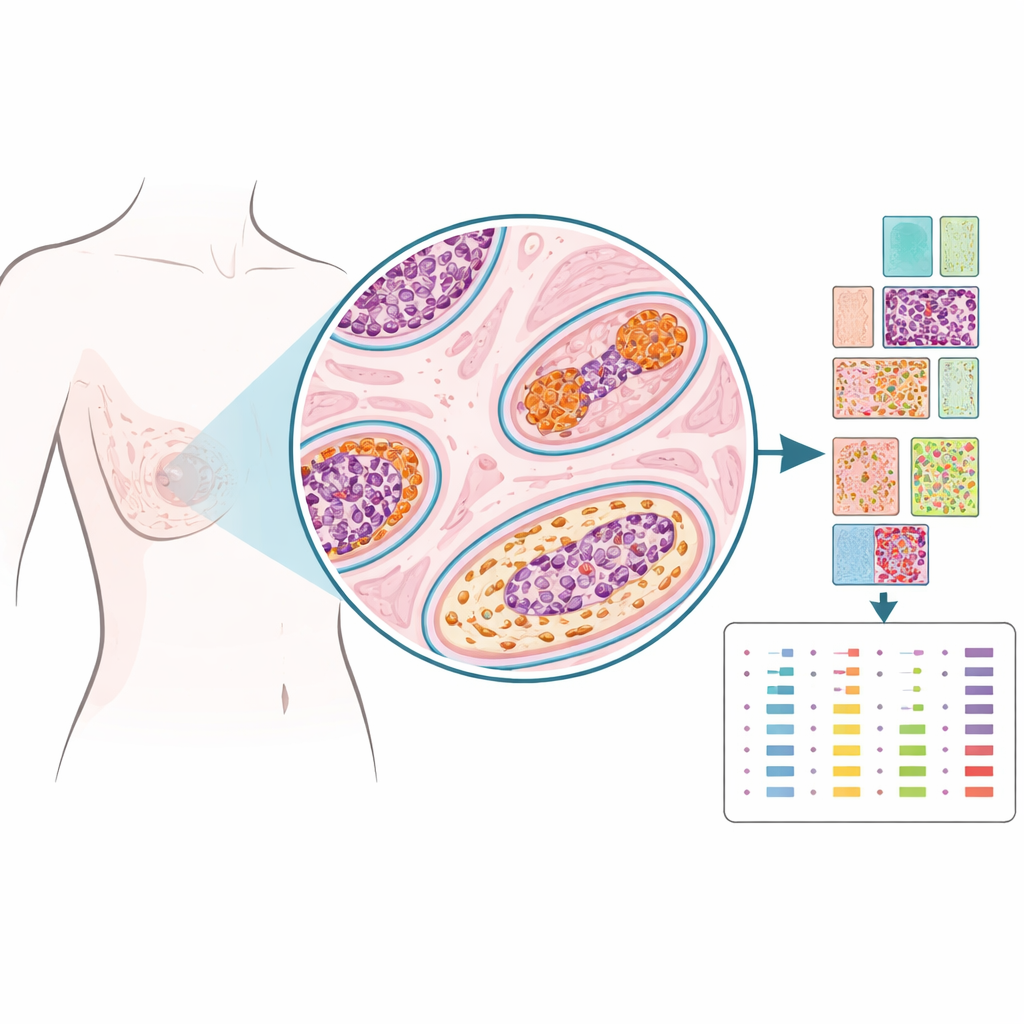
Dwa główne typy wczesnych zmian
Gdy zespół pogrupował dane bez podawania komputerowi informacji klinicznych, wyłonił się uderzający wzorzec. Większość próbek DCIS należała do jednej z dwóch grup: te o wysokim poziomie receptora estrogenowego (ER) i niskim poziomie receptora wzrostu HER2 oraz te o przeciwnym profilu — niskim ER i wysokim HER2. To rozdzielenie przypominało, ale nie było identyczne z, klasyfikacją stosowaną w przypadku raka inwazyjnego. Przewody wyglądające na normalne nie wykazywały tak ostrego grupowania, a tkanka podporowa wokół DCIS miała własne, odrębne wzorce białkowe. W stromie otaczającym obszary przy DCIS ER‑ujemnym występowało zwykle więcej markerów komórek odpornościowych, co sugeruje bardziej aktywne „sąsiedztwo” odpornościowe w porównaniu z regionami wokół DCIS ER‑pozytywnego.
Ukryte różnice w obrębie każdego przewodu
Dzięki możliwości rozdzielenia regionów w obrębie pojedynczego przewodu badacze porównali też poziomy białek na brzegu przewodu z tymi w jego centrum. Białka związane z kurczliwą zewnętrzną warstwą przewodu i z podziałami komórkowymi były bardziej obfite na obwodzie, co sugeruje, że komórki przylegające do ściany przewodu są szczególnie aktywne. Natomiast transporter cukrów związany z dostawą energii był wyższy w centrum przewodu, co wskazuje na odmienny metabolizm w zatłoczonych komórkach wewnętrznych. Co istotne, ogólne poziomy receptorów hormonalnych nie zmieniały się znacząco między centrum a brzegiem, ale drobne różnice w równowadze białek strukturalnych i związanych ze wzrostem ujawniły wewnętrzną organizację, której testy typu „bulk” by nie wykryły.
Wskazówki, które DCIS może postępować
Kluczowe pytanie brzmiało, czy któryś z tych przestrzennych wzorców białkowych przewiduje późniejszy rozwój raka inwazyjnego. Porównując kobiety, u których wystąpiła choroba inwazyjna, z tymi, u których nie wystąpiła, badacze zauważyli sugestywne, lecz statystycznie umiarkowane różnice w białkach związanych ze wzrostem i strukturą przy analizie samego DCIS. Silniejsze sygnały pojawiły się, gdy porównano poziomy białek w DCIS z pobliskimi, wyglądającymi na normalne przewodami tej samej pacjentki. W zmianach, które później stały się inwazyjne, stosunek niektórych białek związanych z odpornością wewnątrz przewodów przesunął się: markery cytotoksycznych limfocytów T i związane z nimi receptory miały tendencję do obniżenia, podczas gdy względnie wyższy był białko mogące tłumić odpowiedzi immunologiczne. To wskazuje na lokalne środowisko odpornościowe wewnątrz przewodów, które może być mniej zdolne do powstrzymywania wyłaniających się komórek nowotworowych. 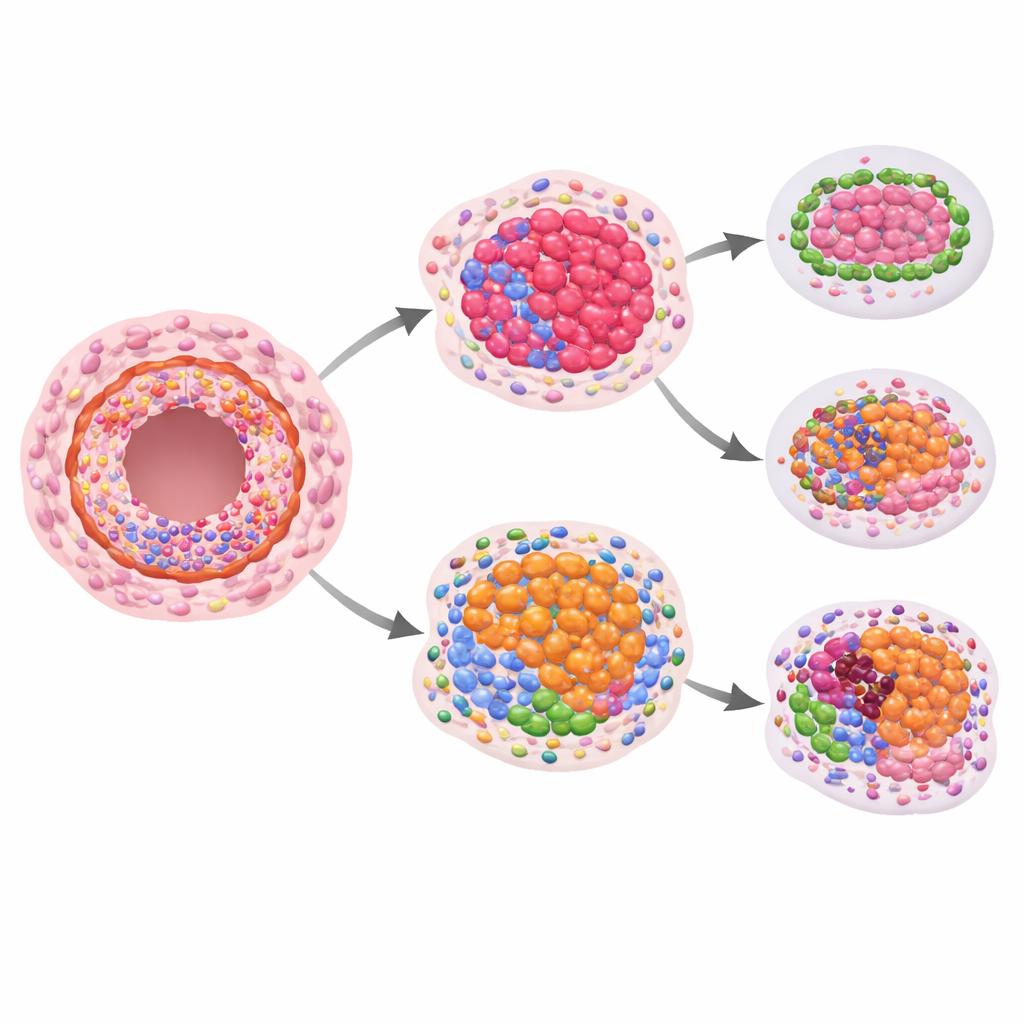
Jak leczenie i czas przekształcają guzy
Dla podgrupy pacjentek badacze przeanalizowali także tkanki z późniejszych zdarzeń w tej samej piersi — albo kolejnej zmiany DCIS, albo guza inwazyjnego — i porównali je z pierwotnym DCIS. W wielu parach wzorce hormonalne i HER2 były podobne, ale niektóre wykazywały istotne zmiany, w tym przypadki, w których DCIS o profilu ER‑wysokie, HER2‑niskie został zastąpiony nawrotem HER2‑wysokim, ER‑niskim, albo gdy DCIS HER2‑wysokie poprzedzał raka inwazyjnego z dużo niższym poziomem HER2. Część tych zmian prawdopodobnie odzwierciedla powstanie całkowicie nowych guzów niezależnych, a nie liniową ewolucję zmiany pierwotnej. Wśród kobiet, które otrzymały terapię hormonalną, późniejsze nowotwory często miały obniżone poziomy białek napędzanych przez estrogen, co sugeruje, że leczenie może przekształcać profil molekularny kolejnych zmian.
Co to oznacza dla pacjentek
Badanie pokazuje, że DCIS nie jest jednorodnym stanem, lecz mozaiką regionów różniących się sygnalizacją hormonalną, obecnością elementów odpornościowych i zachowaniem komórek — różnice te mogą wpływać na przyszłe ryzyko. Choć żadne pojedyncze białko nie okazało się doskonałą „kryształową kulą”, praca wskazuje konkretne markery odpornościowe wewnątrz przewodów oraz kontrast między DCIS a sąsiednią tkanką normalną jako obiecujące składniki przyszłych punktacji ryzyka. Dodając tę przestrzenną warstwę do istniejących danych genetycznych i klinicznych, badacze mają nadzieję zmierzać ku przyszłości, w której kobiety z DCIS będą mogły otrzymać pewniejszą informację, czy bezpiecznie wybrać czujne monitorowanie, czy też potrzebne jest agresywne leczenie.
Cytowanie: Marks, J.R., Dai, Y., King, L.M. et al. Spatial proteomics of breast ductal carcinoma in situ reveal distinct regional differences. Sci Rep 16, 13350 (2026). https://doi.org/10.1038/s41598-026-43486-9
Słowa kluczowe: rak przewodowy in situ, proteomika przestrzenna, ryzyko raka piersi, mikrośrodowisko guza, markery odpornościowe