Clear Sky Science · sv
Spatiell proteomik av ductal bröstcarcinom in situ avslöjar tydliga regionala skillnader
Varför tidiga förändringar i bröstet spelar roll
Ductalt carcinom in situ (DCIS) är en tidig form av bröstsjukdom som ofta upptäcks vid rutinmässiga mammografier. Det har ännu inte brutit igenom mjölkgångarna in i den omgivande vävnaden, men hos vissa kvinnor utvecklas det så småningom till invasiv bröstcancer. I dag kan läkare inte på ett tillförlitligt sätt skilja vilka DCIS‑lesioner som är ofarliga följare och vilka som utgör framtida hot, vilket gör att många patienter får operation och strålbehandling som de kanske inte behöver. Denna studie ger en ny, högupplöst bild av DCIS för att undersöka hur fördelningen av proteiner i och runt gångarna kan hjälpa till att förutsäga vilka fall som har större risk att bli farliga.
Att betrakta bröstvävnad som en karta
I stället för att mala ner vävnaden till ett enda blandprov använde forskarna en teknik kallad spatiell proteomik för att mäta dussintals proteiner i noggrant utvalda punkter på preparatet, nästan som att sätta stift på en karta. De undersökte arkiverad vävnad från 103 kvinnor behandlade för DCIS; vissa fick aldrig ytterligare bröstproblem, några fick senare DCIS igen i samma bröst, och andra utvecklade så småningom invasiv cancer i det bröstet. För varje fall markerade patologer områden inne i DCIS‑gångarna, närliggande stödjande vävnad (stroma), normalt utseende gångar och biopsiställen. Från mer än 1 200 sådana små regioner kvantifierade teamet 53 proteiner kopplade till hormoner, tillväxt, struktur och immunsvar, vilket skapade ett detaljerat spatialt porträtt av varje lesion. 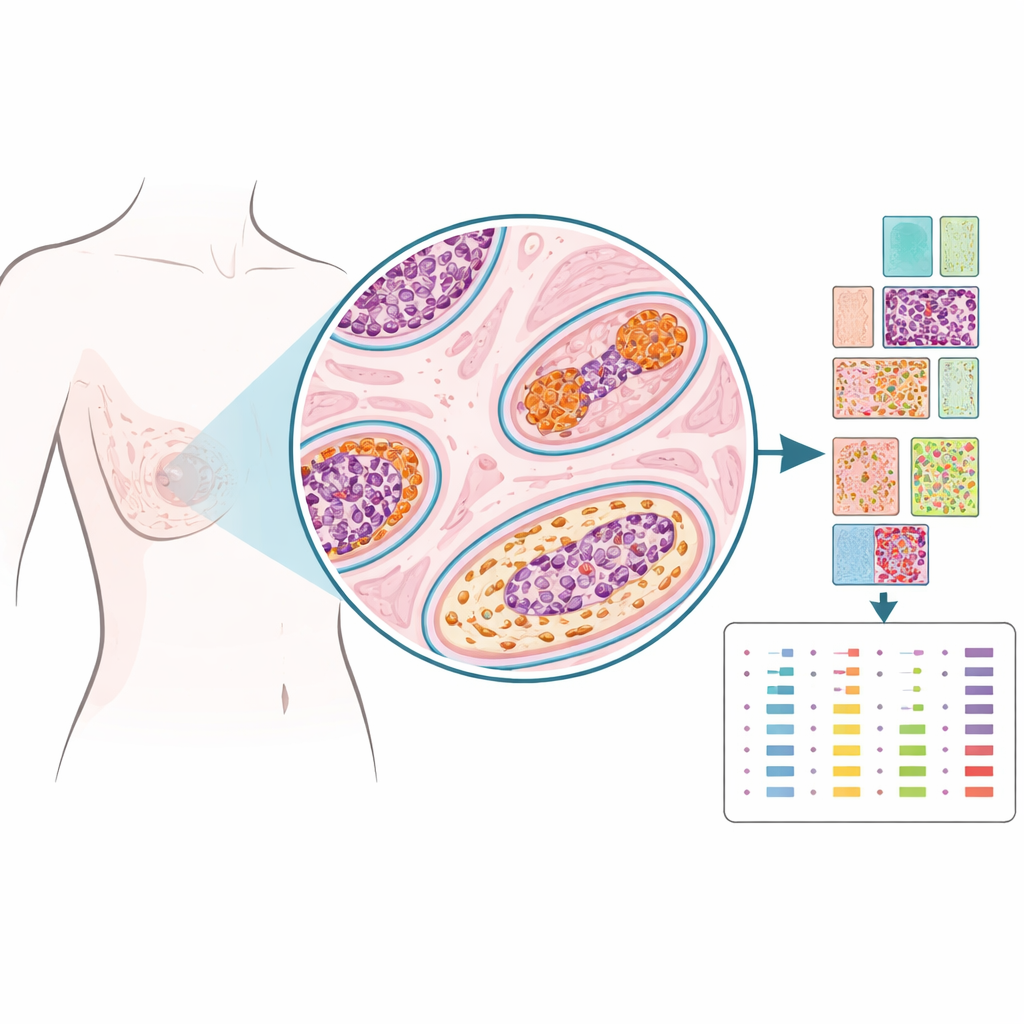
Två huvudsakliga typer av tidiga lesioner
När teamet grupperade data utan att berätta kliniska detaljer för datorn framträdde ett slående mönster. De flesta DCIS‑proverna hamnade i en av två grupper: de med höga nivåer av östrogenreceptor (ER) och låga nivåer av tillväxtfaktorreceptorn HER2, och de med motsatt mönster, låg ER och hög HER2. Denna uppdelning liknade, men var inte identisk med, hur invasiva bröstcancerformer klassificeras. Normalt utseende gångar visade inte samma skarpa klustring, och den stödjande vävnaden runt DCIS hade egna distinkta proteingrupper. I omgivande stroma tenderade områden intill ER‑negativ DCIS att vara rika på immuncellmarkörer, vilket tyder på ett mer aktivt immunmiljö jämfört med regioner runt ER‑positiv DCIS.
Dolda skillnader inom varje gång
Eftersom tekniken kunde separera regioner inom en enda gång jämförde forskarna också proteinnivåer vid gångens kant med de i centrum. Proteiner kopplade till den kontraktila yttre lagret av gången och till celldelning var mer rikligt förekommande i periferin, vilket antyder att celler intill gångväggen är särskilt aktiva. Däremot var en sockertransportör kopplad till energiförsörjning högre i gångens mitt, vilket pekar mot olika metaboliska behov hos trängda inre celler. Föga anmärkningsvärt förändrades inte de övergripande nivåerna av hormonreceptorer mycket mellan centrum och kant, men den finskaliga balansen mellan strukturella och tillväxtrelaterade proteiner gjorde det, och avslöjade en intern organisation som bulktester skulle missa.
Ledtrådar om vilka DCIS som kan progrediera
Den avgörande frågan var om något av dessa spatiala proteininmönster kunde förutsäga framtida invasiv cancer. När kvinnors prover som senare utvecklade invasiv sjukdom jämfördes med de som inte gjorde det sågs antydande men statistiskt blygsamma skillnader i tillväxt‑ och strukturproteiner när man bara tittade på DCIS. Starkare signaler framträdde när man jämförde proteinnivåer i DCIS med närliggande normalt utseende gångar från samma patient. I lesioner som senare blev invasiva skiftade förhållandet för vissa immunrelaterade proteiner inne i gångarna: markörer för hjälpsamma mördande T‑celler och relaterade receptorer tenderade att vara lägre, medan ett protein som kan dämpa immunresponsen var relativt högre. Detta pekar på en lokal immunmiljö inne i gångarna som kan vara mindre förmögen att hålla nya cancerceller i schack. 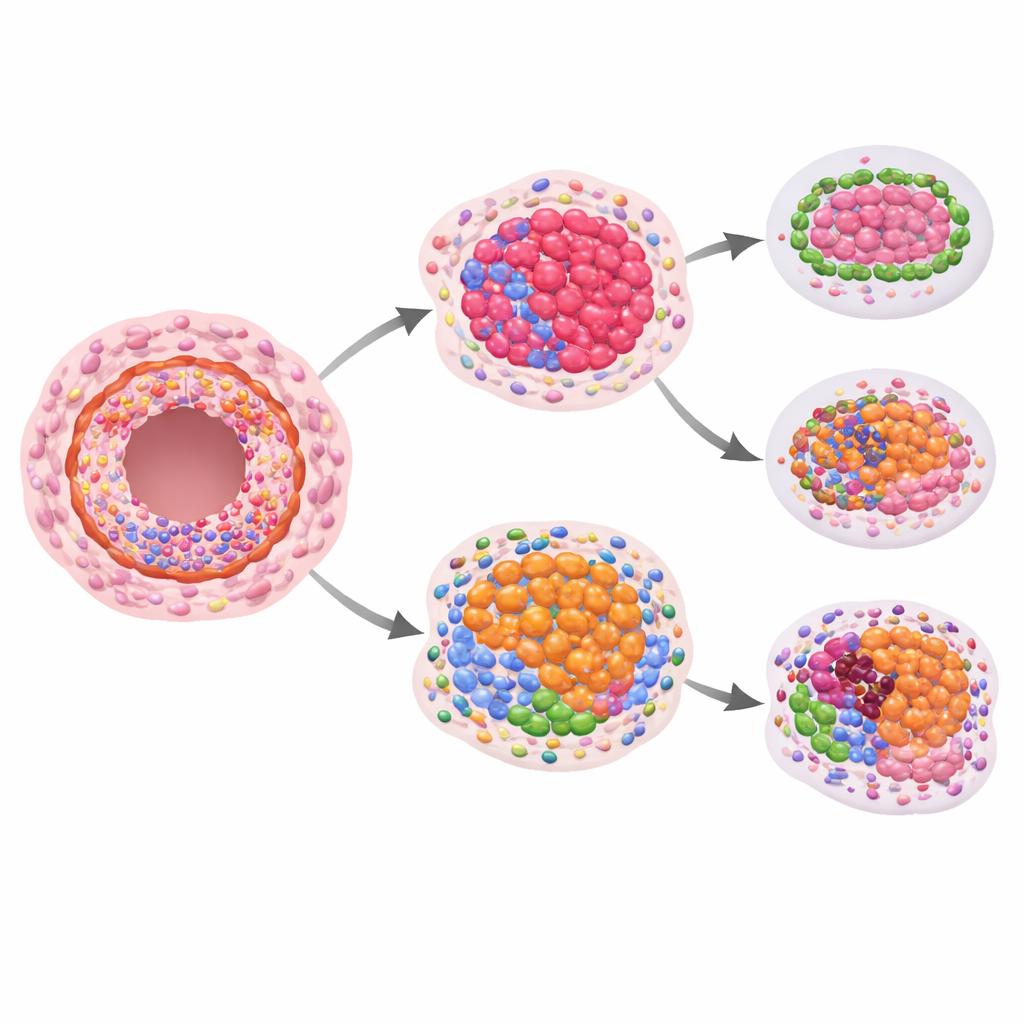
Hur behandling och tid omformar tumörer
För en delmängd av patienterna studerade forskarna också vävnad från senare händelser i samma bröst — antingen en ny DCIS‑lesion eller en invasiv tumör — och jämförde dem med ursprunglig DCIS. I många par var mönstren för hormon‑ och HER2‑uttryck liknande, men vissa visade stora skift, inklusive fall där en ER‑hög, HER2‑låg DCIS följdes av en HER2‑hög, ER‑låg återkomst, eller där HER2‑hög DCIS följdes av en invasiv cancer med mycket mindre HER2. Några av dessa förändringar speglar sannolikt helt nya tumörer som uppstår oberoende snarare än en enkel linjär utveckling från ursprungslesionen. Bland kvinnor som fick hormonbehandling hade senare cancerformer ofta minskade nivåer av proteiner som drivs av östrogen, vilket tyder på att behandling kan omforma den molekylära profilen hos efterföljande sjukdom.
Vad detta betyder för patienter
Studien visar att DCIS inte är en enhetlig åkomma utan ett lapptäcke av regioner som skiljer sig åt i hormonsignalering, immunnärvaro och cellbeteende, och att dessa skillnader kan spela roll för framtida risk. Även om inget enskilt protein framträdde som en perfekt spåkula lyfter arbetet fram specifika immumarkörer inne i gångarna — liksom kontrasten mellan DCIS och intilliggande normal vävnad — som lovande komponenter för framtida riskpoäng. Genom att lägga detta spatiala lager på befintlig genetisk och klinisk information hoppas forskare kunna röra sig mot en framtid där kvinnor med DCIS kan få tydligare besked om de med större säkerhet kan välja noggrann uppföljning eller verkligen behöver aggressiv behandling.
Citering: Marks, J.R., Dai, Y., King, L.M. et al. Spatial proteomics of breast ductal carcinoma in situ reveal distinct regional differences. Sci Rep 16, 13350 (2026). https://doi.org/10.1038/s41598-026-43486-9
Nyckelord: ductalt carcinom in situ, spatiell proteomik, bröstcancerrisk, tumörmikromiljö, immunkorsmarkörer