Clear Sky Science · pt
Proteômica espacial do carcinoma ductal in situ da mama revela diferenças regionais distintas
Por que alterações precoces na mama importam
O carcinoma ductal in situ (CDIS) é uma forma precoce de doença mamária frequentemente detectada em mamografias de rotina. Ainda não rompeu os ductos mamários para o tecido circundante, mas em algumas mulheres pode evoluir para câncer de mama invasivo. Hoje, os médicos não conseguem distinguir com segurança quais lesões de CDIS são inofensivas e quais representam risco futuro, de modo que muitas pacientes recebem cirurgia e radioterapia que talvez não precisem. Este estudo faz uma análise nova e de alta resolução do CDIS para ver como a disposição das proteínas dentro e ao redor desses ductos pode ajudar a prever quais casos têm maior probabilidade de se tornar perigosos.
Olhando o tecido mamário como um mapa
Em vez de triturar o tecido até obter uma amostra homogênea, os pesquisadores usaram uma tecnologia chamada proteômica espacial para medir dezenas de proteínas em pontos escolhidos com precisão no corte histológico, quase como colocar alfinetes num mapa. Eles examinaram material arquivado de 103 mulheres tratadas por CDIS — algumas que nunca tiveram problemas mamários subsequentes, outras que tiveram recidiva de CDIS na mesma mama, e outras que acabaram desenvolvendo câncer invasivo nessa mama. Para cada caso, patologistas marcaram regiões dentro dos ductos com CDIS, o tecido de sustentação próximo (estroma), ductos com aparência normal e locais de biópsia. A partir de mais de 1.200 dessas pequenas regiões, a equipe quantificou 53 proteínas ligadas a hormônios, crescimento, estrutura e atividade imune, criando um retrato espacial detalhado de cada lesão. 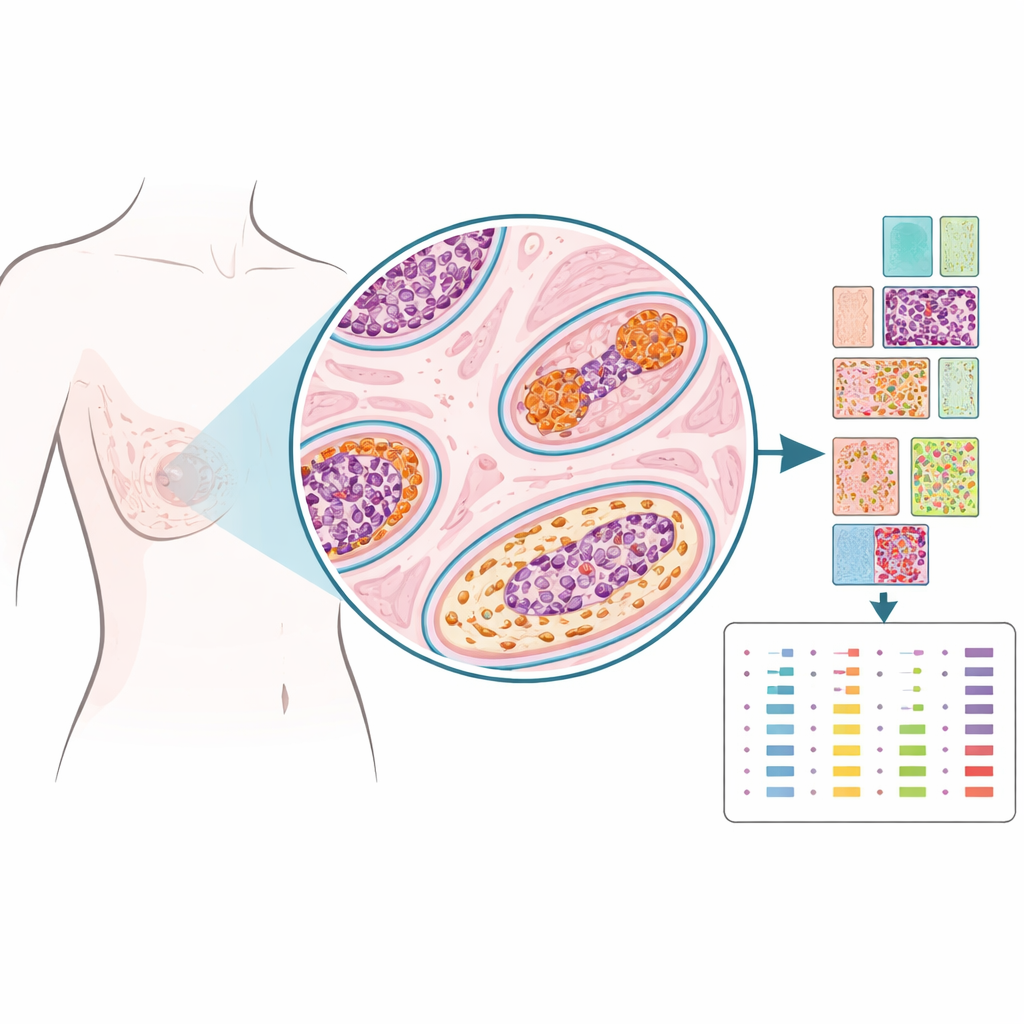
Dois tipos principais de lesões precoces
Quando a equipe agrupou os dados sem informar ao computador detalhes clínicos, um padrão marcante surgiu. A maioria das amostras de CDIS caiu em um de dois grupos: aquelas com altos níveis do receptor de estrogênio (ER) e baixos níveis do receptor do fator de crescimento HER2, e aquelas com o padrão oposto, baixo ER e alto HER2. Essa divisão se assemelha, mas não é idêntica, à categorização dos cânceres de mama invasivos. Ductos com aparência normal não exibiram o mesmo agrupamento nítido, e o tecido de suporte ao redor do CDIS apresentou padrões protéicos distintos. No estroma adjacente, áreas próximas a CDIS ER-negativo tendiam a ser ricas em marcadores de células imunes, sugerindo um ambiente imune mais ativo em comparação com regiões ao redor de CDIS ER-positivo.
Diferenças ocultas dentro de cada ducto
Como a técnica permitia separar regiões dentro de um único ducto, os pesquisadores também compararam os níveis de proteínas na borda do ducto com os do centro. Proteínas associadas à camada contrátil externa do ducto e à divisão celular foram mais abundantes na periferia, indicando que as células junto à parede ductal estão especialmente ativas. Em contraste, um transportador de açúcar ligado ao fornecimento de energia era mais alto no centro do ducto, sugerindo demandas metabólicas diferentes nas células internas mais agrupadas. Notavelmente, os níveis gerais dos receptores hormonais não mudaram muito entre centro e borda, mas o equilíbrio em pequena escala de proteínas estruturais e relacionadas ao crescimento variou, revelando uma organização interna que testes de amostra única não detectariam.
Pistas sobre quais CDIS podem progredir
A questão-chave era se algum desses padrões espaciais de proteínas antevia câncer invasivo futuro. Comparando mulheres que evoluíram para doença invasiva com as que não evoluíram, os pesquisadores observaram diferenças sugestivas, embora estatisticamente moderadas, em proteínas de crescimento e estruturais ao analisar apenas o CDIS. Sinais mais fortes surgiram quando compararam os níveis de proteínas no CDIS com ductos de aparência normal próximos da mesma paciente. Nas lesões que depois se tornaram invasivas, a razão de certas proteínas relacionadas ao sistema imune dentro dos ductos mudou: marcadores de células T citotóxicas e receptores associados tenderam a ser mais baixos, enquanto uma proteína que pode atenuar respostas imunes estava relativamente mais alta. Isso aponta para um ambiente imune local dentro dos ductos que pode estar menos apto a conter células cancerígenas em surgimento. 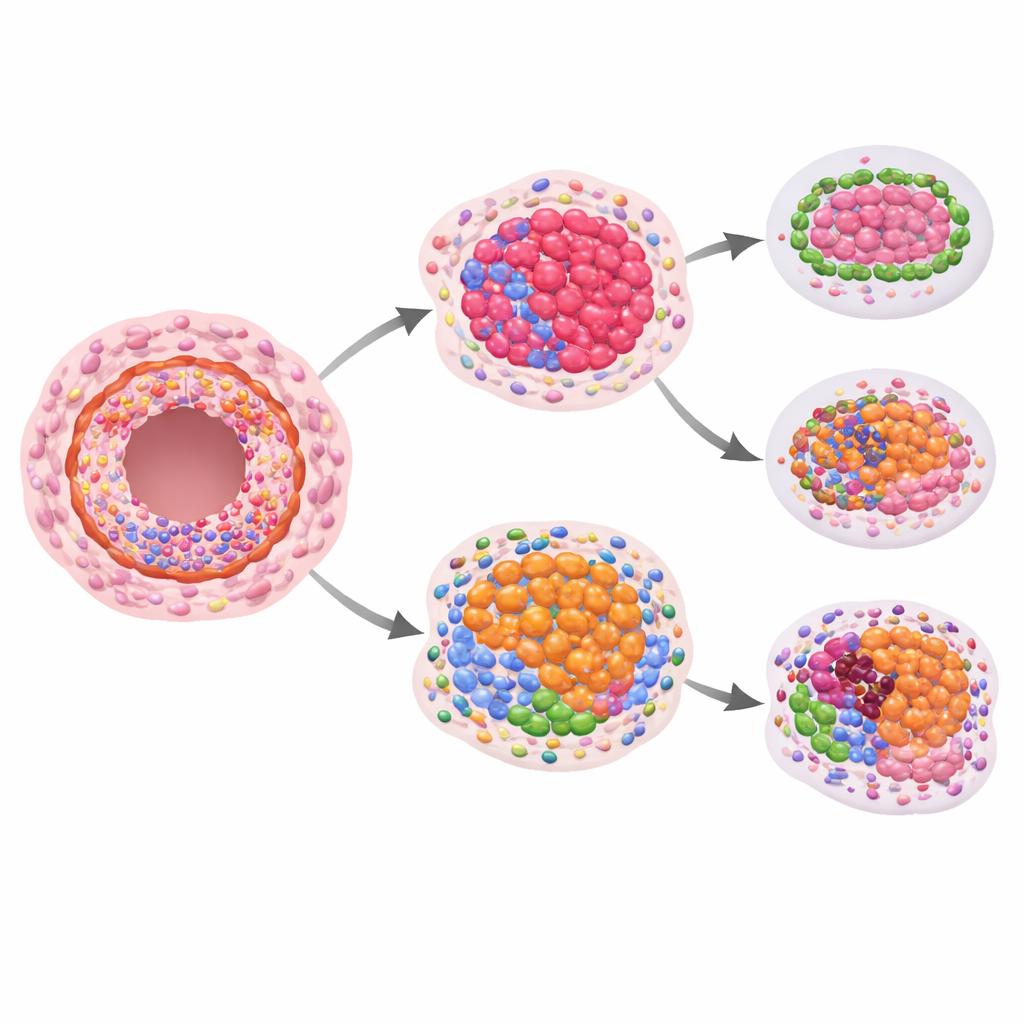
Como tratamento e tempo remodelam os tumores
Para um subconjunto de pacientes, os investigadores também estudaram tecido de eventos posteriores na mesma mama — seja outra lesão de CDIS ou um tumor invasivo — e os compararam com o CDIS original. Em muitos pares, os padrões de hormônio e HER2 eram semelhantes, mas alguns mostraram mudanças importantes, incluindo casos em que um CDIS com ER alto e HER2 baixo foi seguido por uma recorrência HER2 alta e ER baixo, ou onde um CDIS HER2 alto foi seguido por um câncer invasivo com muito menos HER2. Algumas dessas mudanças provavelmente refletem tumores inteiramente novos surgindo de forma independente, em vez de uma evolução linear da lesão original. Entre mulheres que receberam terapia hormonal, os cânceres posteriores frequentemente apresentaram níveis reduzidos de proteínas induzidas por estrogênio, sugerindo que o tratamento pode remodelar o perfil molecular da doença subsequente.
O que isso significa para as pacientes
O estudo mostra que o CDIS não é uma condição uniforme, mas um mosaico de regiões que diferem em sinalização hormonal, presença imune e comportamento celular, e que essas diferenças podem importar para o risco futuro. Embora nenhuma proteína isolada tenha surgido como uma bola de cristal perfeita, o trabalho destaca marcadores imunes específicos dentro dos ductos — assim como o contraste entre CDIS e tecido normal vizinho — como ingredientes promissores para pontuações de risco futuras. Ao adicionar essa camada espacial às informações genéticas e clínicas já existentes, os pesquisadores esperam avançar para um futuro em que mulheres com CDIS possam ser informadas, com maior confiança, se podem optar por acompanhamento cuidadoso ou se realmente precisam de tratamento agressivo.
Citação: Marks, J.R., Dai, Y., King, L.M. et al. Spatial proteomics of breast ductal carcinoma in situ reveal distinct regional differences. Sci Rep 16, 13350 (2026). https://doi.org/10.1038/s41598-026-43486-9
Palavras-chave: carcinoma ductal in situ, proteômica espacial, risco de câncer de mama, microambiente tumoral, marcadores imunes