Clear Sky Science · es
Proteómica espacial del carcinoma ductal in situ de mama revela diferencias regionales claras
Por qué importan los cambios tempranos en la mama
El carcinoma ductal in situ (CDIS) es una forma temprana de enfermedad mamaria que a menudo se detecta en mamografías de rutina. Aún no ha invadido fuera de los conductos mamarios hacia el tejido circundante, pero en algunas mujeres puede evolucionar hasta convertirse en cáncer de mama invasivo. Hoy por hoy, los médicos no pueden predecir con fiabilidad qué lesiones de CDIS son inofensivas y cuáles acabarán siendo peligrosas, por lo que muchas pacientes reciben cirugía y radioterapia que quizá no necesiten. Este estudio aplica una mirada nueva y de alta resolución al CDIS para ver cómo la disposición de las proteínas dentro y alrededor de estos conductos podría ayudar a predecir qué casos tienen mayor probabilidad de volverse peligrosos.
Mirar el tejido mamario como un mapa
En lugar de triturar el tejido hasta obtener una muestra homogénea, los investigadores utilizaron una tecnología llamada proteómica espacial para medir docenas de proteínas en puntos escogidos con precisión sobre la lámina, casi como si colocaran chinchetas en un mapa. Examinaron tejido archivado de 103 mujeres tratadas por CDIS, algunas de las cuales no tuvieron problemas posteriores en la mama, otras que más tarde desarrollaron CDIS de nuevo en la misma mama y otras que finalmente presentaron cáncer invasivo en esa mama. Para cada caso, los patólogos marcaron regiones dentro de los conductos con CDIS, el tejido de sostén cercano (estroma), conductos de aspecto normal y los sitios de biopsia. A partir de más de 1.200 de esas diminutas regiones, el equipo cuantificó 53 proteínas relacionadas con hormonas, crecimiento, estructura y actividad inmunitaria, creando un retrato espacial detallado de cada lesión. 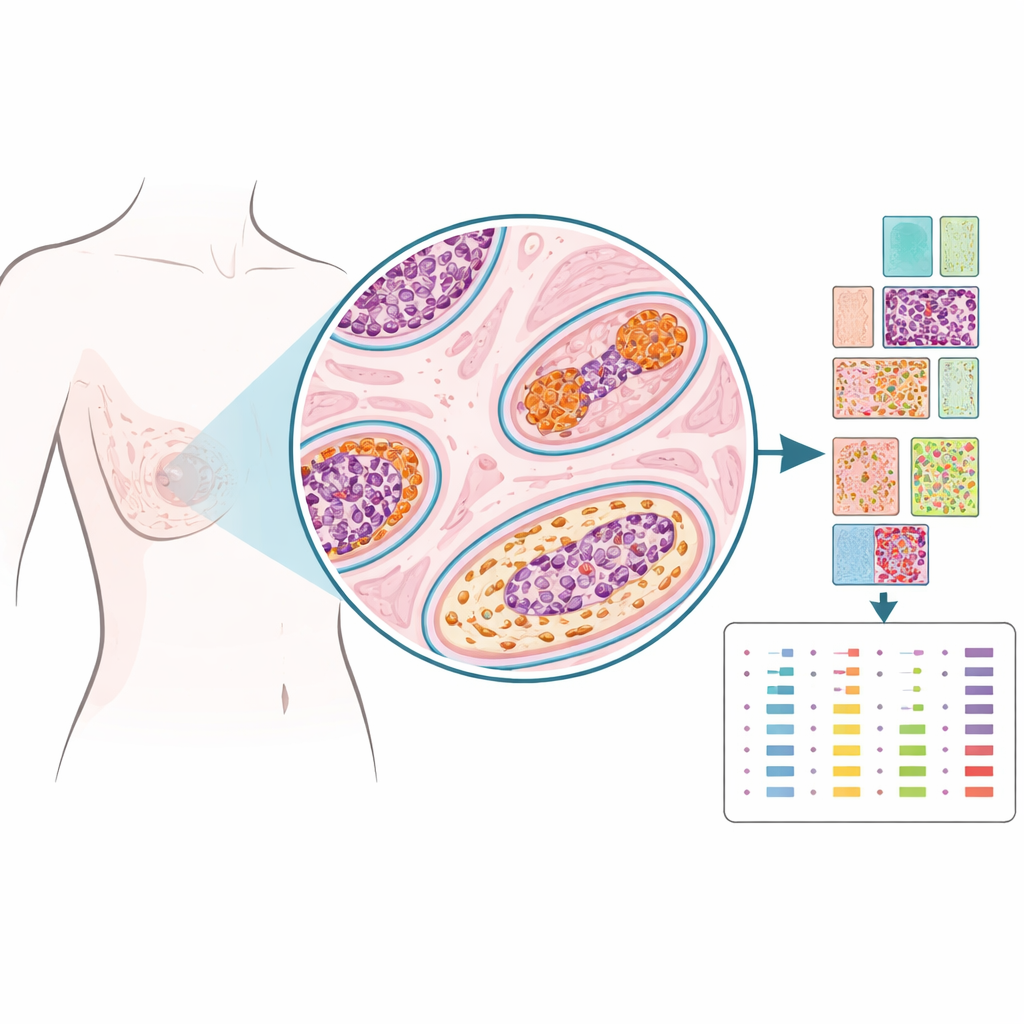
Dos tipos principales de lesiones tempranas
Cuando el equipo agrupó los datos sin aportar al algoritmo detalles clínicos, surgió un patrón llamativo. La mayoría de las muestras de CDIS se dividieron en dos grupos: aquellas con niveles altos de receptor de estrógeno (ER) y bajos de receptor del factor de crecimiento HER2, y aquellas con el patrón opuesto, ER bajo y HER2 alto. Esta separación se parecía, aunque no era idéntica, a la forma en que se categorizan los cánceres de mama invasivos. Los conductos de aspecto normal no mostraron el mismo agrupamiento nítido, y el tejido de sostén alrededor del CDIS mostró sus propios patrones proteicos distintivos. En el estroma circundante, las áreas junto a CDIS ER-negativo tendieron a ser ricas en marcadores de células inmunitarias, lo que sugiere un vecindario inmunitario más activo en comparación con las regiones alrededor de CDIS ER-positivo.
Diferencias ocultas dentro de cada conducto
Como la técnica podía separar regiones dentro de un mismo conducto, los investigadores también compararon los niveles de proteínas en el borde del conducto con los del centro. Las proteínas asociadas con la capa contráctil externa del conducto y con la división celular eran más abundantes en la periferia, lo que implica que las células junto a la pared ductal están especialmente activas. En contraste, un transportador de azúcares vinculado al suministro de energía era más alto en el centro del conducto, lo que sugiere demandas metabólicas distintas en las células internas más apretadas. De forma notable, los niveles globales de receptores hormonales no variaron mucho entre centro y borde, pero el equilibrio a pequeña escala de proteínas estructurales y relacionadas con el crecimiento sí cambió, revelando una organización interna que las pruebas globales pasarían por alto.
Pistas sobre qué CDIS puede progresar
La pregunta clave era si alguno de estos patrones proteicos espaciales podía predecir el desarrollo futuro de cáncer invasivo. Al comparar a las mujeres que progresaron a enfermedad invasiva con las que no lo hicieron, los investigadores observaron diferencias sugestivas pero estadísticamente modestas en proteínas de crecimiento y estructurales al analizar solo el CDIS. Señales más fuertes aparecieron cuando compararon cómo los niveles proteicos en el CDIS se relacionaban con los conductos de aspecto normal cercanos del mismo paciente. En lesiones que más tarde se volvieron invasivas, la proporción de ciertas proteínas relacionadas con la inmunidad dentro de los conductos cambió: los marcadores de células T citotóxicas útiles y receptores relacionados tendieron a ser más bajos, mientras que una proteína que puede atenuar las respuestas inmunitarias fue relativamente más alta. Esto apunta a un microambiente inmunitario local dentro de los conductos que puede ser menos capaz de mantener a raya a las células cancerosas emergentes. 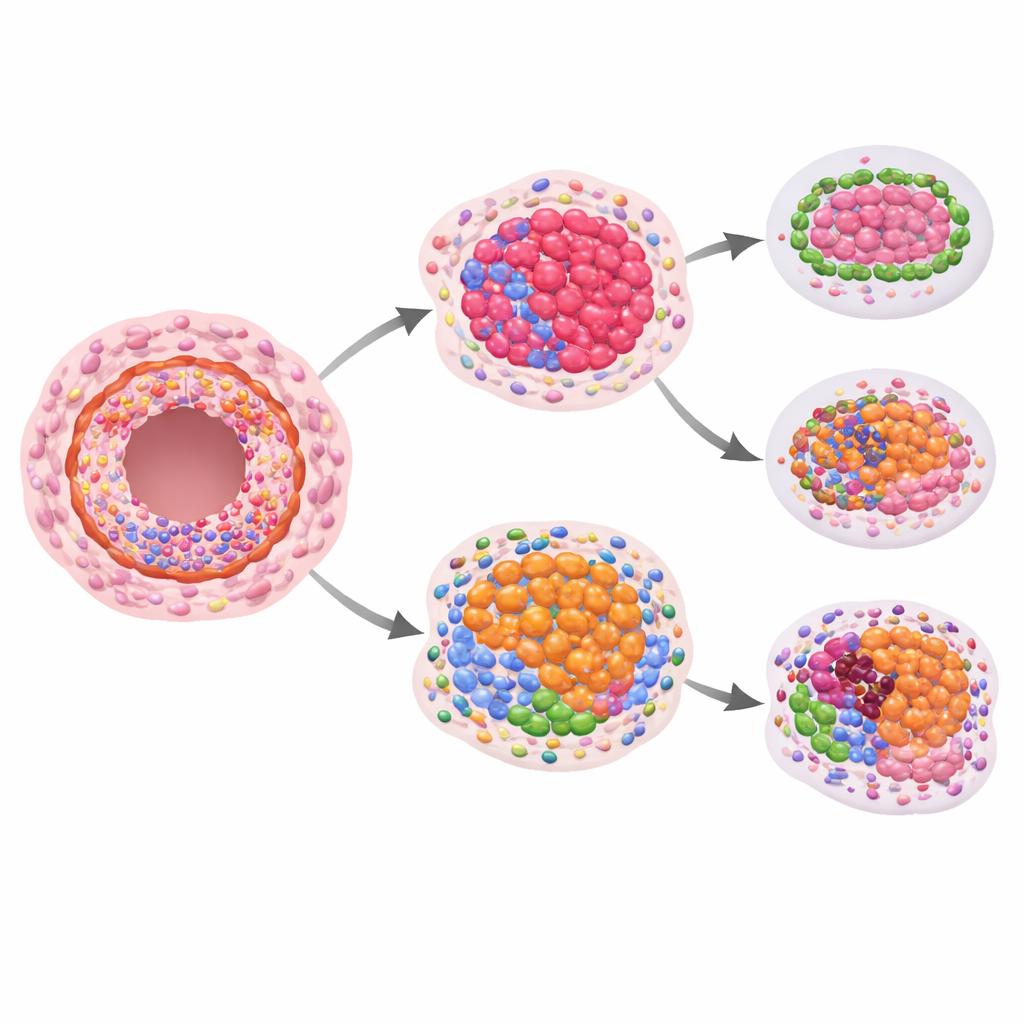
Cómo el tratamiento y el tiempo remodelan los tumores
Para un subconjunto de pacientes, los investigadores también estudiaron tejido de eventos posteriores en la misma mama—ya fuera otra lesión de CDIS o un tumor invasivo—y los compararon con el CDIS original. En muchas parejas, los patrones de hormonas y HER2 fueron similares, pero algunos mostraron cambios importantes, incluidos casos en los que un CDIS con ER alto y HER2 bajo fue seguido por una recurrencia HER2 alta y ER baja, o en los que un CDIS HER2 alto fue sucedido por un cáncer invasivo con mucho menos HER2. Algunos de estos cambios probablemente reflejan tumores completamente nuevos que surgen de forma independiente más que una evolución lineal de la lesión original. Entre las mujeres que recibieron terapia hormonal, los cánceres posteriores a menudo presentaron niveles reducidos de proteínas impulsadas por el estrógeno, lo que sugiere que el tratamiento puede remodelar el perfil molecular de la enfermedad subsiguiente.
Qué significa esto para las pacientes
El estudio muestra que el CDIS no es una condición uniforme, sino un mosaico de regiones que difieren en señalización hormonal, presencia inmunitaria y comportamiento celular, y que estas diferencias pueden influir en el riesgo futuro. Aunque ninguna proteína individual surgió como una bola de cristal perfecta, el trabajo destaca marcadores inmunitarios específicos dentro de los conductos—así como el contraste entre el CDIS y el tejido normal vecino—como ingredientes prometedores para futuras puntuaciones de riesgo. Al añadir esta capa espacial a la información genética y clínica existente, los investigadores esperan avanzar hacia un futuro en el que a las mujeres con CDIS se les pueda decir con mayor confianza si pueden optar por una vigilancia cuidadosa o si realmente necesitan un tratamiento agresivo.
Cita: Marks, J.R., Dai, Y., King, L.M. et al. Spatial proteomics of breast ductal carcinoma in situ reveal distinct regional differences. Sci Rep 16, 13350 (2026). https://doi.org/10.1038/s41598-026-43486-9
Palabras clave: carcinoma ductal in situ, proteómica espacial, riesgo de cáncer de mama, microambiente tumoral, marcadores inmunitarios