Clear Sky Science · nl
Ruimtelijke proteomica van ductaal carcinoom in situ van de borst onthult duidelijke regionale verschillen
Waarom vroegtijdige veranderingen in de borst ertoe doen
Ductaal carcinoom in situ (DCIS) is een vroege vorm van borstaandoening die vaak bij routinematige mammografie wordt gevonden. Het is nog niet uit de melkgangen naar het omliggende weefsel doorgebroken, maar bij sommige vrouwen leidt het uiteindelijk tot invasieve borstkanker. Op dit moment kunnen artsen niet betrouwbaar aangeven welke DCIS-laesies onschadelijke metgezellen zijn en welke toekomstige bedreigingen vormen, waardoor veel patiënten chirurgie en bestraling krijgen die mogelijk niet noodzakelijk zijn. Deze studie bekijkt DCIS op een nieuwe, hoogopgeloste manier om te zien hoe de rangschikking van eiwitten in en rond deze gangen kan helpen voorspellen welke gevallen waarschijnlijk gevaarlijker worden.
Het borstweefsel als een kaart bekijken
In plaats van weefsel te verpulveren tot één samenhangend monster, gebruikten de onderzoekers een technologie genaamd ruimtelijke proteomica om tientallen eiwitten te meten op precies gekozen plekken op het preparaat, bijna alsof ze spelden in een kaart zetten. Ze onderzochten gearchiveerd weefsel van 103 vrouwen die voor DCIS waren behandeld; sommigen van hen kregen daarna geen verdere borstaandoeningen, sommigen ontwikkelden later opnieuw DCIS in dezelfde borst, en sommigen kregen uiteindelijk invasieve kanker in die borst. Voor elk geval markeerden pathologen regio's binnen de DCIS-gangen, het nabijgelegen steunweefsel (stroma), normaal uitziende gangen en biopsieplaatsen. Uit meer dan 1.200 van zulke kleine regio's kwantificeerde het team 53 eiwitten die gelinkt zijn aan hormonen, groei, structuur en immuunactiviteit, en creëerden zo een gedetailleerd ruimtelijk portret van elke laesie. 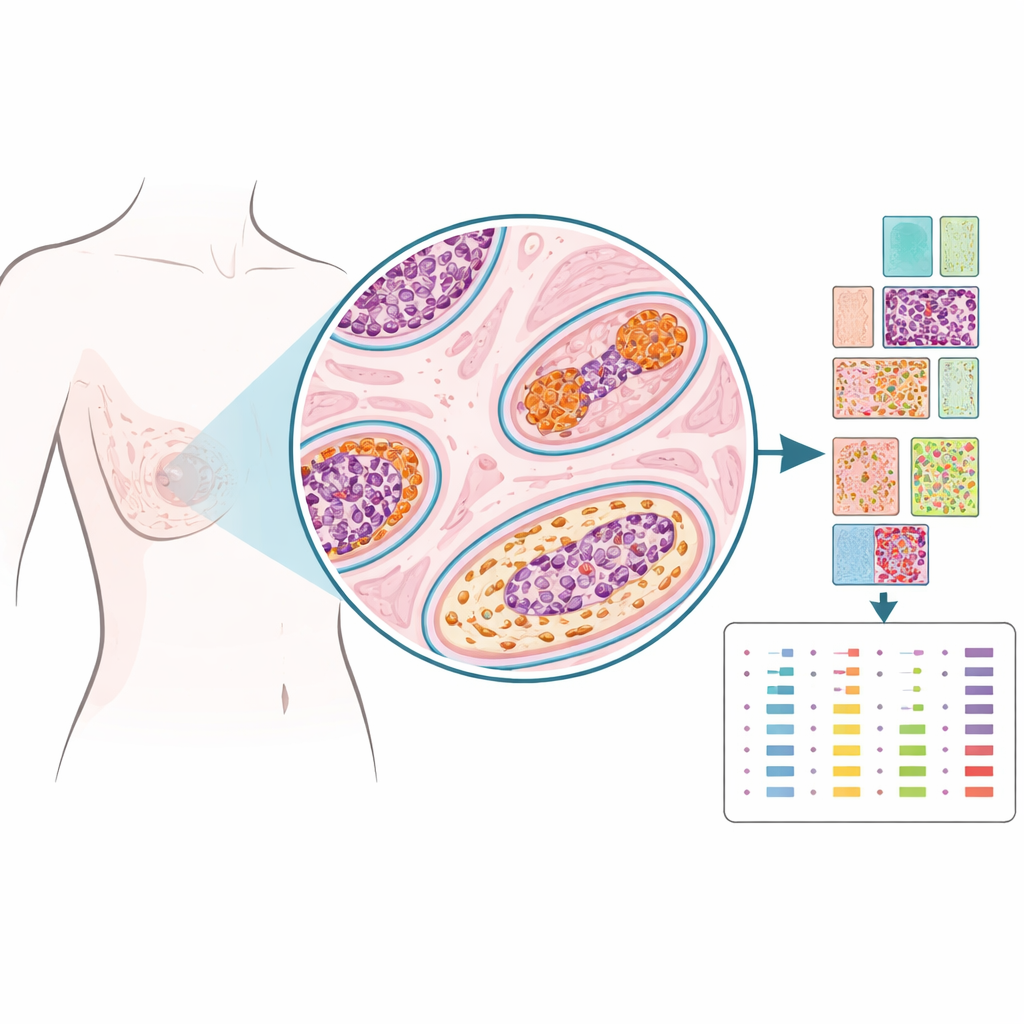
Twee hoofdtypen van vroege laesies
Toen het team de data groepsgewijs analyseerde zonder de computer klinische details te geven, kwam een opvallend patroon naar voren. De meeste DCIS-monsters vielen in een van twee kampen: die met hoge niveaus van oestrogeenreceptor (ER) en lage niveaus van de groeifactorreceptor HER2, en die met het omgekeerde patroon, lage ER en hoge HER2. Deze scheiding leek op, maar was niet identiek aan, de indeling die bij invasieve borstkankers wordt gebruikt. Normaal uitziende gangen toonden niet dezelfde scherpe clustering, en het steunweefsel rond DCIS vertoonde weer eigen, onderscheidende eiwitpatronen. In het omringende stroma waren gebieden naast ER-negatieve DCIS vaak rijk aan immuuncelmke markers, wat wijst op een actievere immuunomgeving vergeleken met regio's rond ER-positieve DCIS.
Verborgen verschillen binnen elke gang
Aangezien de techniek regio's binnen een enkele gang kon onderscheiden, vergeleken de onderzoekers ook eiwitniveaus aan de rand van de gang met die in het midden. Eiwitten die geassocieerd zijn met de contractiele buitenlaag van de gang en celdeling waren meer aanwezig aan de periferie, wat impliceert dat cellen langs de gangwand bijzonder actief zijn. Daarentegen was een suikervervoerder die gekoppeld is aan energietoevoer hoger in het gangcentrum, wat wijst op verschillende metabolische behoeften bij de dicht opeengepakte binnenste cellen. Opmerkelijk was dat de totale hormoonreceptorniveaus niet veel veranderden tussen centrum en rand, maar het fijnmazige evenwicht van structurele en groeigerelateerde eiwitten wel, waardoor een interne organisatie zichtbaar wordt die bulktests zouden missen.
Wegluidingen naar welke DCIS kan doorgroeien
De cruciale vraag was of een van deze ruimtelijke eiwitpatronen toekomstige invasieve kanker kon voorspellen. Bij vergelijking van vrouwen die later invasieve ziekte kregen met degenen die dat niet deden, zagen de onderzoekers veelbelovende maar statistisch bescheiden verschillen in groeieiwitten en structurele eiwitten wanneer alleen naar DCIS werd gekeken. Sterkere signalen verschenen toen ze onderzochten hoe eiwitniveaus in DCIS zich verhouden tot nabijgelegen normaal ogende gangen van dezelfde patiënt. In laesies die later invasief werden, verschoof de verhouding van bepaalde immuun-gerelateerde eiwitten binnen de gangen: markers van behulpzame killer T-cellen en gerelateerde receptoren waren vaak lager, terwijl een eiwit dat immuunreacties kan dempen relatief hoger was. Dit wijst op een lokale immuunomgeving binnen de gangen die mogelijk minder in staat is opkomende kankercellen onder controle te houden. 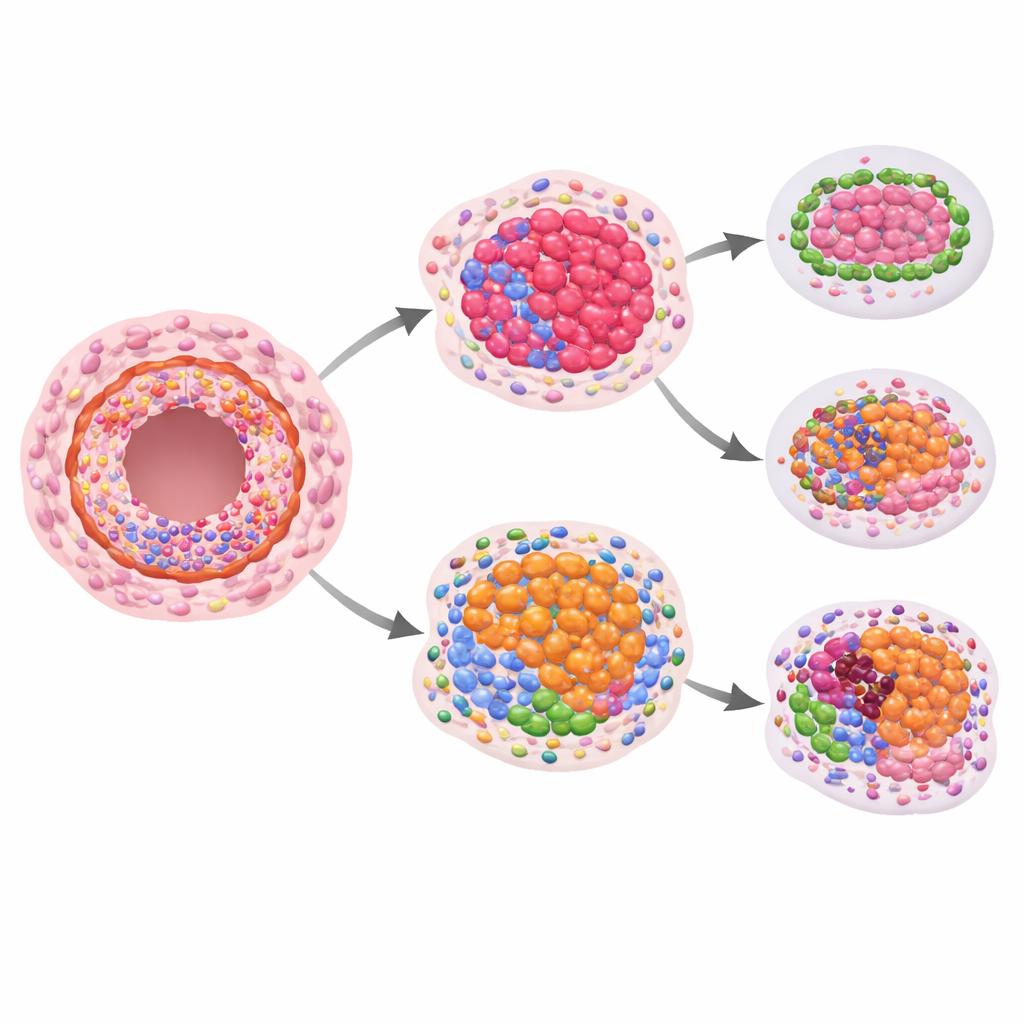
Hoe behandeling en tijd tumoren hervormen
Voor een deel van de patiënten bestudeerden de onderzoekers ook weefsel van latere gebeurtenissen in dezelfde borst—ofwel een andere DCIS-laesie of een invasieve tumor—en vergeleken die met de oorspronkelijke DCIS. In veel paren waren hormoon- en HER2-patronen vergelijkbaar, maar sommige toonden grote verschuivingen, waaronder gevallen waarin een ER-hoog, HER2-laag DCIS gevolgd werd door een HER2-hoog, ER-laag recidief, of waarin HER2-hoog DCIS gevolgd werd door een invasieve kanker met veel minder HER2. Sommige van deze veranderingen weerspiegelen waarschijnlijk geheel nieuwe tumoren die onafhankelijk zijn ontstaan in plaats van een rechtlijnige evolutie van de oorspronkelijke laesie. Bij vrouwen die hormoontherapie kregen, hadden latere kankers vaak verminderde niveaus van door oestrogeen aangedreven eiwitten, wat suggereert dat behandeling het moleculaire profiel van daaropvolgende ziekte kan hervormen.
Wat dit betekent voor patiënten
De studie laat zien dat DCIS geen uniforme aandoening is, maar een lappendeken van regio's die verschillen in hormoonsignaalgeving, immuunaanwezigheid en celgedrag, en dat deze verschillen van belang kunnen zijn voor toekomstig risico. Hoewel geen enkel eiwit als perfecte waarzegger naar voren kwam, belicht het werk specifieke immuunmarkers binnen de gangen—en het contrast tussen DCIS en aangrenzend normaal weefsel—als veelbelovende ingrediënten voor toekomstige risicoscores. Door deze ruimtelijke laag toe te voegen aan bestaande genetische en klinische informatie, hopen onderzoekers op een toekomst waarin vrouwen met DCIS met grotere zekerheid kunnen horen of ze veilig voor zorgvuldig volgen kunnen kiezen of echt een agressievere behandeling nodig hebben.
Bronvermelding: Marks, J.R., Dai, Y., King, L.M. et al. Spatial proteomics of breast ductal carcinoma in situ reveal distinct regional differences. Sci Rep 16, 13350 (2026). https://doi.org/10.1038/s41598-026-43486-9
Trefwoorden: ductaal carcinoom in situ, ruimtelijke proteomica, borstkankerrisico, tumormicroomgeving, immuunmarkers