Clear Sky Science · it
La proteomica spaziale del carcinoma duttale in situ del seno rivela chiare differenze regionali
Perché contano i cambiamenti precoci al seno
Il carcinoma duttale in situ (DCIS) è una forma precoce di malattia mammaria spesso rilevata durante mammografie di routine. Non ha ancora oltrepassato i dotti lattiferi nel tessuto circostante, ma in alcune donne può evolvere in un tumore mammario invasivo. Al momento i medici non sono in grado di distinguere con sicurezza quali lesioni DCIS sono innocue e quali rappresentano una minaccia futura, perciò molte pazienti ricevono interventi chirurgici e radioterapia che potrebbero non essere necessari. Questo studio adotta un approccio nuovo e ad alta risoluzione per esaminare il DCIS e capire se l’organizzazione delle proteine dentro e attorno ai dotti possa aiutare a prevedere quali casi sono più propensi a diventare pericolosi.
Esaminare il tessuto mammario come una mappa
Invece di macinare il tessuto in un campione unico e omogeneo, i ricercatori hanno utilizzato una tecnologia chiamata proteomica spaziale per misurare decine di proteine in punti scelti con precisione sul vetrino, quasi come piantare dei pin su una mappa. Hanno analizzato tessuti d’archivio di 103 donne trattate per DCIS: alcune non hanno avuto ulteriori problemi al seno, altre hanno sviluppato di nuovo DCIS nello stesso seno, e altre ancora hanno poi sviluppato un tumore invasivo nello stesso seno. Per ogni caso i patologi hanno marcato regioni all’interno dei dotti DCIS, il tessuto di supporto vicino (stroma), dotti dall’aspetto normale e siti di biopsia. Da oltre 1.200 di queste piccole regioni il team ha quantificato 53 proteine legate a ormoni, fattori di crescita, struttura e attività immunitaria, creando un ritratto spaziale dettagliato di ciascuna lesione. 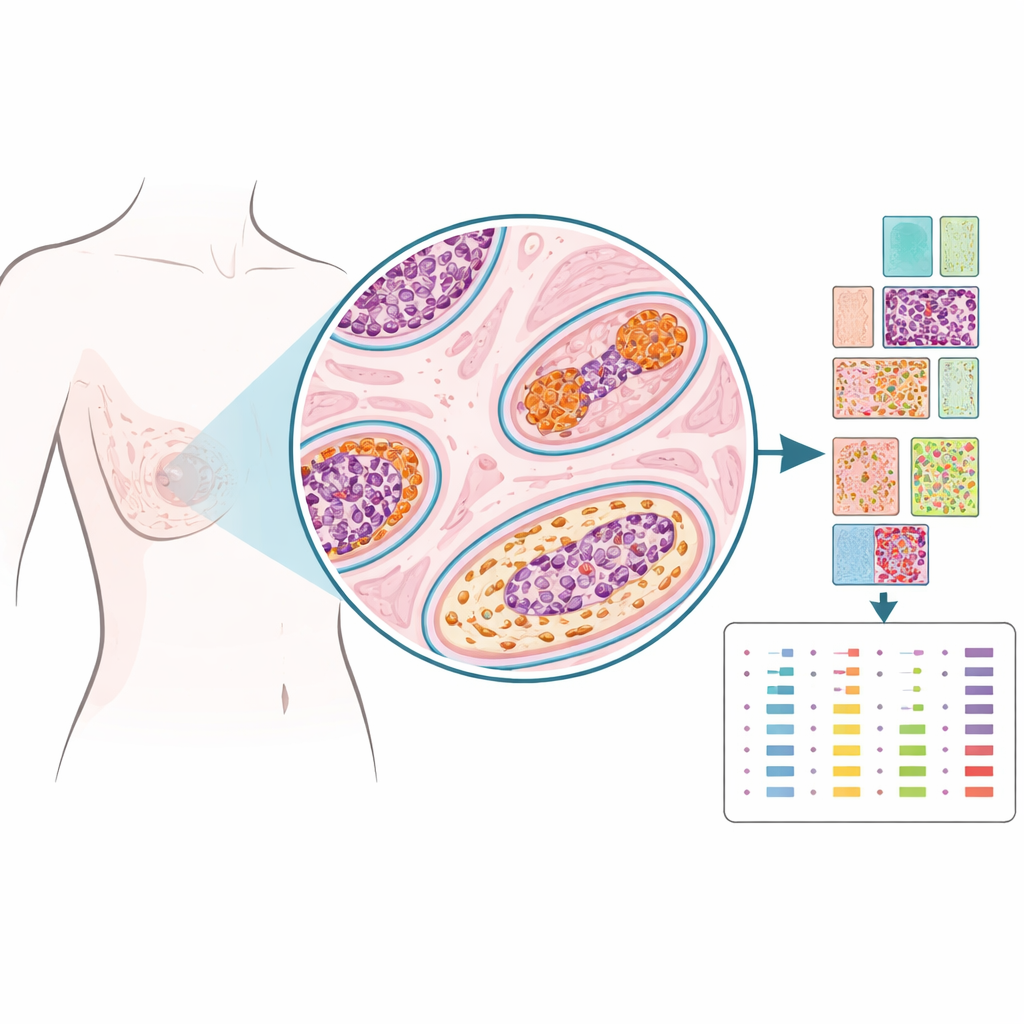
Due tipi principali di lesioni precoci
Quando il gruppo ha raggruppato i dati senza fornire al computer informazioni cliniche, è emerso un pattern netto. La maggior parte dei campioni DCIS si è distribuita in due categorie: quelli con alti livelli del recettore degli estrogeni (ER) e bassi livelli del recettore del fattore di crescita HER2, e quelli con lo schema opposto, bassi ER e alto HER2. Questa divisione somigliava, ma non era identica, alla classificazione dei tumori mammari invasivi. I dotti dall’aspetto normale non mostravano lo stesso raggruppamento netto, e il tessuto di supporto attorno al DCIS presentava pattern proteici distinti. Nello stroma circostante, le aree adiacenti a DCIS ER‑negativo tendevano a essere ricche di marcatori di cellule immunitarie, suggerendo un quartiere immunitario più attivo rispetto alle regioni intorno a DCIS ER‑positivo.
Differenze nascoste all’interno di ogni dotto
Poiché la tecnica poteva separare regioni all’interno di un singolo dotto, i ricercatori hanno anche confrontato i livelli proteici al bordo del dotto con quelli al centro. Le proteine associate allo strato esterno contrattilе del dotto e alla divisione cellulare erano più abbondanti in periferia, implicando che le cellule attaccate alla parete duttale siano particolarmente attive. Al contrario, un trasportatore di zuccheri collegato alla fornitura energetica risultava più elevato nel centro del dotto, suggerendo differenti esigenze metaboliche nelle cellule interne più affollate. È importante notare che i livelli complessivi dei recettori ormonali non cambiavano molto tra centro e bordo, ma l’equilibrio su scala fine di proteine strutturali e legate alla crescita sì, rivelando un’organizzazione interna che i test su campioni omogenei non potrebbero cogliere.
Indizi su quali DCIS potrebbero progredire
La domanda cruciale era se alcuni di questi pattern proteici spaziali potessero predire un futuro tumore invasivo. Confrontando le donne che hanno poi sviluppato malattia invasiva con quelle che non l’hanno fatto, i ricercatori hanno osservato differenze suggestive ma statisticamente modeste nelle proteine legate alla crescita e alla struttura quando si guardava solo al DCIS. Segnali più forti sono emersi confrontando i livelli proteici nel DCIS con quelli dei dotti dall’aspetto normale adiacenti nello stesso paziente. Nelle lesioni che successivamente sono diventate invasive, il rapporto di certe proteine correlate all’immunità all’interno dei dotti cambiava: i marcatori delle cellule T citotossiche utili e dei recettori correlati tendevano ad essere più bassi, mentre una proteina che può attenuare le risposte immunitarie risultava relativamente più alta. Ciò indica un ambiente immunitario locale all’interno dei dotti che potrebbe essere meno in grado di tenere sotto controllo le cellule tumorali emergenti. 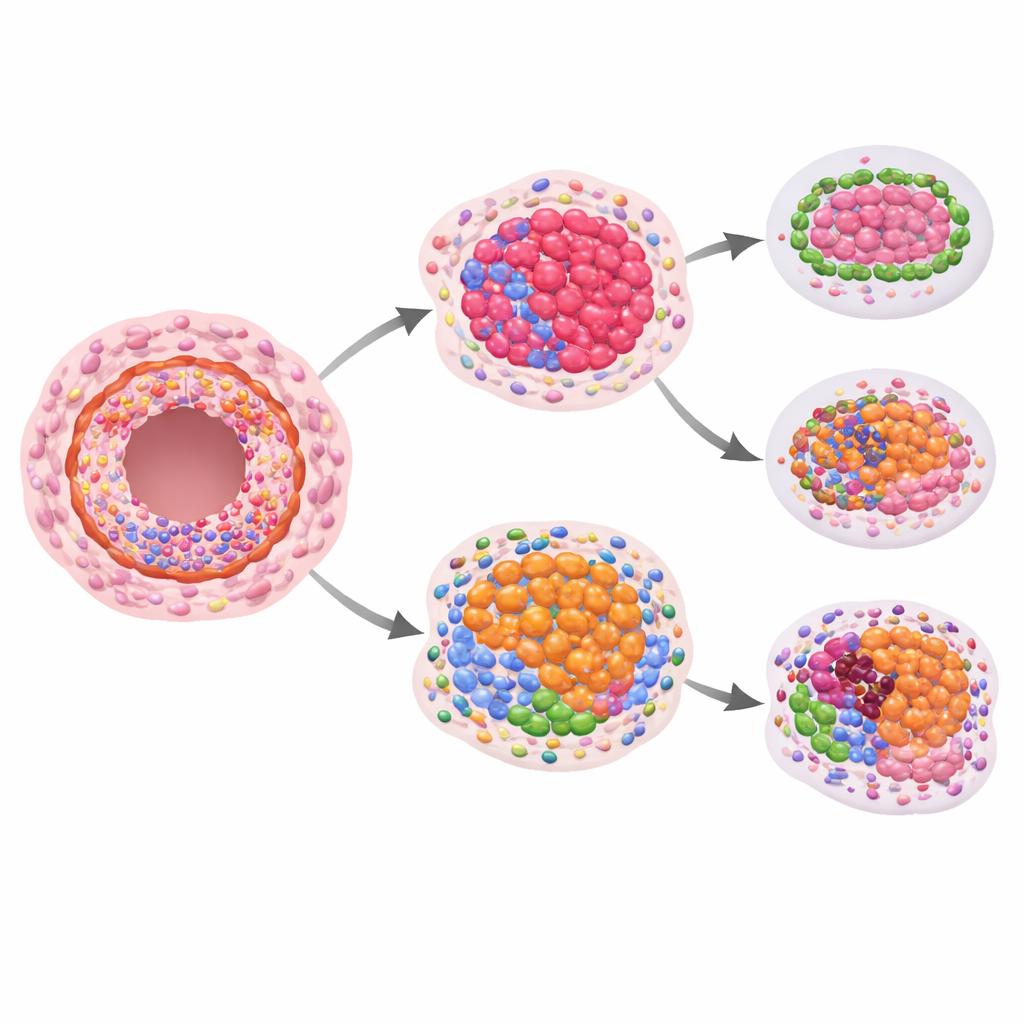
Come il trattamento e il tempo rimodellano i tumori
Per un sottoinsieme di pazienti, gli investigatori hanno anche studiato tessuto di eventi successivi nello stesso seno — sia un’altra lesione DCIS sia un tumore invasivo — confrontandoli con il DCIS originale. In molte coppie, gli schemi ormonali e di HER2 risultavano simili, ma alcune mostravano cambiamenti marcati, inclusi casi in cui un DCIS ER‑alto, HER2‑basso era seguito da una recidiva HER2‑alta, ER‑bassa, o dove un DCIS HER2‑alto era seguito da un tumore invasivo con molto meno HER2. Alcuni di questi cambiamenti probabilmente riflettono tumori completamente nuovi che nascono in modo indipendente piuttosto che un’evoluzione lineare della lesione originale. Tra le donne che hanno ricevuto terapia ormonale, i tumori successivi spesso presentavano livelli ridotti di proteine guidate dagli estrogeni, suggerendo che il trattamento possa rimodellare il profilo molecolare della malattia successiva.
Cosa significa per le pazienti
Lo studio mostra che il DCIS non è una condizione uniforme, ma un mosaico di regioni che differiscono per segnalazione ormonale, presenza immunitaria e comportamento cellulare, e che queste differenze possono influire sul rischio futuro. Pur non essendo emersa una singola proteina in grado di predire il destino con certezza, il lavoro mette in luce specifici marcatori immunitari all’interno dei dotti — così come il confronto tra DCIS e tessuto normale vicino — come ingredienti promettenti per futuri punteggi di rischio. Aggiungendo questo livello spaziale alle informazioni genetiche e cliniche esistenti, i ricercatori sperano di arrivare a un futuro in cui alle donne con DCIS si possa dire, con maggiore fiducia, se possono scegliere un monitoraggio attento o se necessitano davvero di un trattamento aggressivo.
Citazione: Marks, J.R., Dai, Y., King, L.M. et al. Spatial proteomics of breast ductal carcinoma in situ reveal distinct regional differences. Sci Rep 16, 13350 (2026). https://doi.org/10.1038/s41598-026-43486-9
Parole chiave: carcinoma duttale in situ, proteomica spaziale, rischio di tumore al seno, microambiente tumorale, marcatori immunitari