Clear Sky Science · zh
通过 cGAS‑STING–干扰素‑β 轴,γ‑氨基丁酸转氨酶在肾细胞癌中介导肿瘤抑制
将一种神经递质变为癌症弱点
肾癌,尤其是其最常见的类型——透明细胞肾细胞癌,一旦转移后治疗非常困难,常常对化疗和放疗都具有耐受性。本研究揭示了一种在脑化学中更为人所知但长期被忽视的酶——γ‑氨基丁酸转氨酶(ABAT),可以成为对抗肾脏肿瘤的隐秘盟友。通过在癌细胞内增强该酶的活性,研究人员能够唤醒一种强大的内源性免疫报警系统,从而减缓肿瘤生长并重塑肿瘤的免疫环境。
肾肿瘤中缺失的守护者
研究团队首先分析了大型患者数据库和肿瘤样本,观察 ABAT 在肾癌中的表现。在健康组织中,ABAT 有助于分解镇静性神经递质 GABA,维持其水平平衡。然而在肿瘤样本中,ABAT 水平持续显著低于邻近的正常肾组织,且 ABAT 含量最低的患者预后往往更差。这一模式提示肿瘤可能通过沉默 ABAT 来获得生长优势。
唤醒细胞的入侵者报警系统
为了解析一种代谢酶如何产生如此强烈的抗肿瘤效应,研究人员比较了有无额外 ABAT 的癌细胞的基因表达。他们发现一组通常由抗病毒防御信号激活的基因显著上调,尤其是由一种名为干扰素‑β 的分子调控的基因,这指向了先天免疫中的“入侵者报警”被激活——该报警通常用于感知病毒或 DNA 损伤。通过使用选择性药物阻断不同的感知通路,他们将该效应追踪到 cGAS‑STING 通路——一个在细胞内不应出现 DNA 时响应的系统。当化学方式关闭这一通路时,ABAT 就无法再驱动高水平的干扰素‑β 或有效抑制肿瘤,表明其抗癌能力依赖于这一内部报警系统。
细胞能量工厂内部的应激
ABAT 通常位于线粒体内,线粒体是细胞的能量工厂。作者发现,提高 ABAT 水平会破坏线粒体健康:驱动其功能的膜电位下降,电子显微镜下形态异常,并且线粒体 DNA 的片段泄漏到细胞内的周围液体中。这些逸出的 DNA 片段正是能触发 cGAS‑STING 的信号类型。研究团队还发现 ABAT 与另一种酶 PRMT5 发生结合,PRMT5 与癌症生长以及抑制免疫报警有关。当 PRMT5 水平降低时,STING 和干扰素‑β 活性上升,暗示 ABAT 可能既损害线粒体又抑制 PRMT5,从而解除对报警通路的抑制,尽管具体细节尚需进一步研究。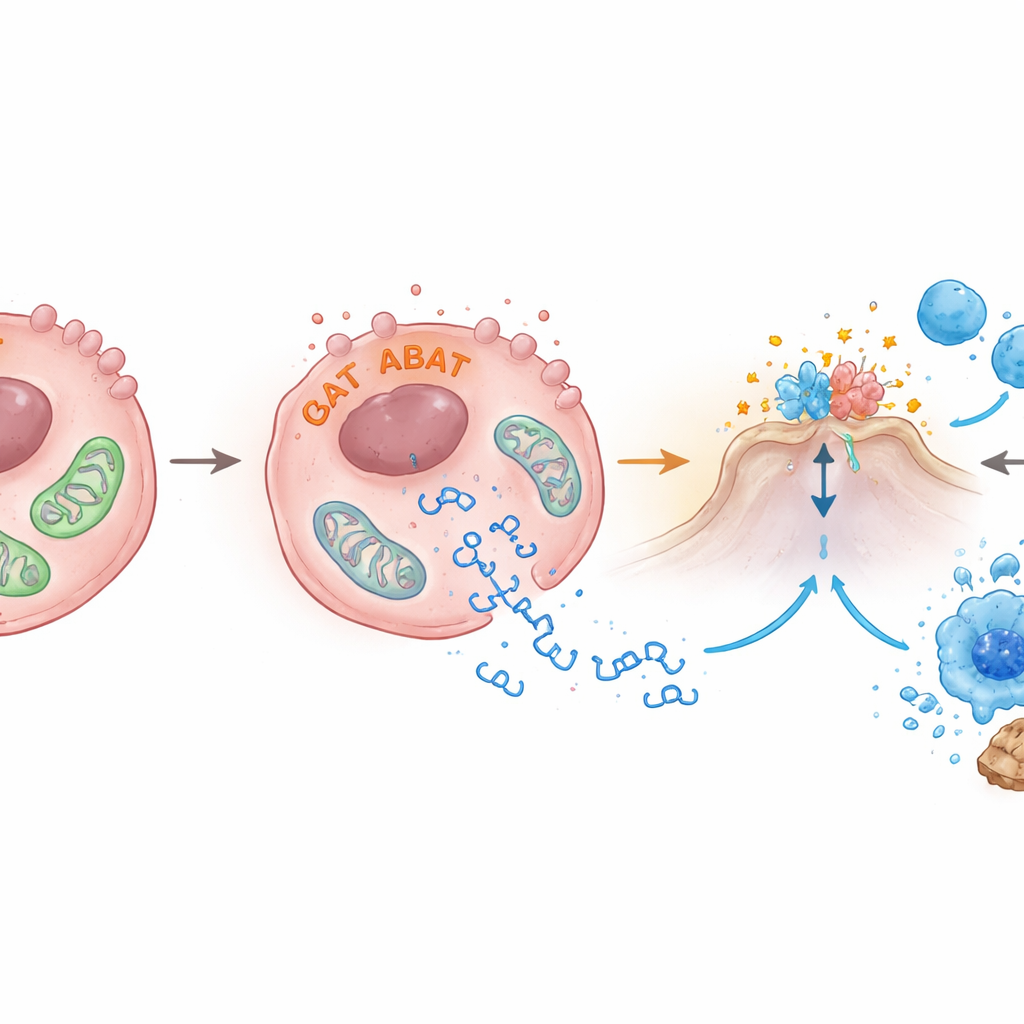
改变肿瘤周围的免疫平衡
癌症并非孤立生长;它存在于一个由免疫细胞组成的复杂邻里中,这些细胞既可以攻击也可以保护肿瘤。在免疫健全的小鼠模型中,由高 ABAT 含量的肾癌细胞形成的肿瘤不仅生长更慢,而且显示出不同的免疫构成。调节性 T 细胞的比例——这类细胞通常抑制免疫反应并常被肿瘤利用来自我保护——明显降低,而细胞毒性 T 细胞的比例则相对增加。这表明 ABAT 通过触发干扰素和损伤信号,能将局部免疫环境从免疫抑制转向抗肿瘤活动,可能使像检查点抑制剂这样的其他治疗更有效。
对未来治疗的潜在意义
总体而言,该研究将 ABAT 描绘为不仅仅是代谢清道夫:在肾癌中它表现得像一种内源性肿瘤抑制因子,恢复其功能会给癌细胞的能量工厂施加应激,释放危险信号,并启动内部报警召唤免疫系统介入。由于患者肿瘤中常见 ABAT 水平下降,提升其活性或模拟其引发的线粒体与免疫激活效应的策略,可能为晚期肾癌开辟新的治疗途径,尤其是与现有的靶向疗法和免疫疗法联合使用时。
引用: Feng, Y., Cao, S., Cai, T. et al. Gamma-aminobutyric acid transaminase mediates tumor suppression in renal cell carcinoma through the cGAS-STING–interferon-β axis. Sci Rep 16, 13082 (2026). https://doi.org/10.1038/s41598-026-42861-w
关键词: 肾癌, 先天免疫, 肿瘤微环境, 线粒体, 干扰素信号