Clear Sky Science · ru
Трансаминаза гамма-аминомасляной кислоты опосредует подавление опухоли при почечно-клеточном раке через ось cGAS-STING–интерферон-β
Преобразование нейромедиатора в слабое место рака
Рак почки, особенно его наиболее распространённая форма — прозрачноклеточный почечно-клеточный рак, крайне трудно поддаётся лечению после метастазирования и часто устойчив к химио- и радиотерапии. В этом исследовании показано, что мало замеченный фермент, более известный по нейрохимии — трансаминаза гамма-аминомасляной кислоты, или ABAT — может выступать скрытым союзником против опухолей почки. Повышая уровень этого фермента внутри раковых клеток, исследователи смогли пробудить мощную встроенную иммунную «сигнализацию тревоги», которая замедляет рост опухоли и перестраивает иммунное микроокружение опухоли.
Отсутствующий защитник в опухолях почки
Команда начала с анализа больших баз данных пациентов и образцов опухолей, чтобы изучить поведение ABAT при раке почки. В здоровой ткани ABAT участвует в расщеплении успокаивающего нейромедиатора ГАМК, поддерживая его уровень в равновесии. В образцах опухолей, напротив, уровень ABAT был последовательно заметно ниже, чем в прилежащей нормальной почечной ткани, и у пациентов с наименьшим содержанием ABAT прогноз был хуже. Такая картина намекала, что опухоли могут подавлять ABAT, чтобы получить преимущество. 
Пробуждение внутриклеточной сигнализации о проникновении
Чтобы понять, как метаболический фермент может оказывать столь сильный антитуморный эффект, исследователи сравнили активность генов в раковых клетках с повышенным уровнем ABAT и без него. Они обнаружили резкое повышение экспрессии генов, обычно включаемых антивирусными защитными сигналами, особенно тех, которые контролируются молекулой интерферон-β. Это указывало на активацию врождённой иммунной «сигнализации о вторжении», используемой для распознавания вирусов или повреждений ДНК. С помощью селективных препаратов, блокирующих разные пути распознавания, они проследили эффект до пути cGAS‑STING — клеточной системы, реагирующей на появление ДНК в неправильном месте внутри клетки. Когда этот путь был химически подавлен, ABAT больше не мог вызывать высокий уровень интерферона-β и столь эффективно подавлять опухоли, что показывает: противоопухолевая сила ABAT зависит от этой внутренней системы тревоги.
Стресс внутри энергетических станций клетки
ABAT обычно локализуется в митохондриях — энергостанциях клетки. Авторы обнаружили, что повышение уровня ABAT нарушает здоровье митохондрий: упала мембранная потенциальная разность, питающая их, их форма стала аномальной при электронно-микроскопическом исследовании, и фрагменты митохондриальной ДНК утекали в окружение внутри клетки. Эти ушедшие кусочки ДНК как раз представляют собой сигнал, включающий cGAS‑STING. Команда также обнаружила, что ABAT связывается с другим ферментом, PRMT5, который связывают с ростом опухолей и подавлением иммунных сигналов. При снижении PRMT5 активность STING и интерферона‑β возрастала, что даёт понять, что ABAT может одновременно повреждать митохондрии и противодействовать PRMT5, снимая тормоза с пути сигнализации, хотя точные механизмы ещё предстоит уточнить. 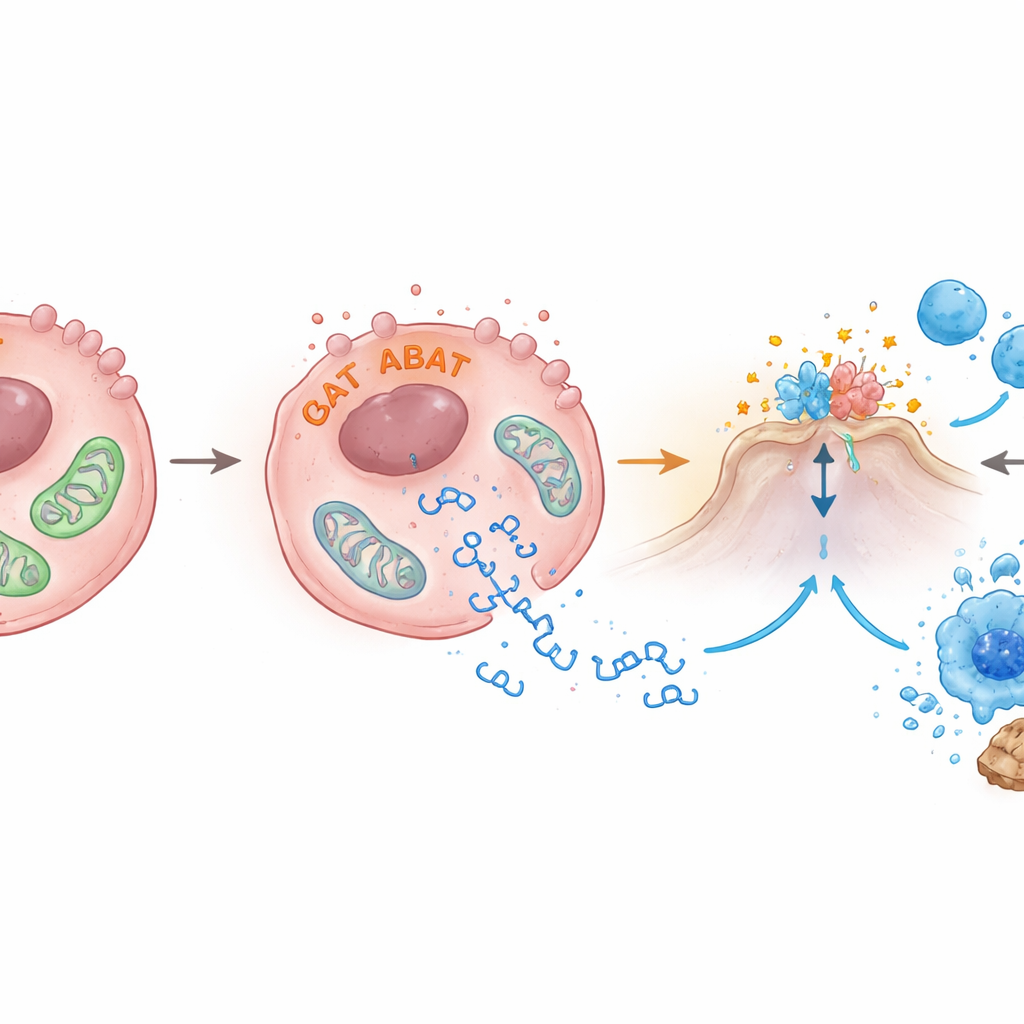
Сдвиг иммунного баланса вокруг опухоли
Опухоль не растёт в изоляции; она существет в сложном окружении иммунных клеток, которые могут либо атаковать её, либо защищать. У иммунокомпетентных мышей опухоли, образованные клетками рака почки с высоким содержанием ABAT, не только росли медленнее, но и имели иной иммунный состав. Доля регуляторных T-клеток — иммунных клеток, которые обычно успокаивают ответы и часто используются опухолями для защиты — заметно снизилась, тогда как баланс сместился в пользу киллерных (цитотоксических) T-клеток. Это указывает на то, что ABAT, активируя интерферон и сигналы повреждения, может сдвинуть локальное иммунное микроокружение от состояния подавления к противоопухолевой активности, что потенциально делает другие методы лечения, такие как ингибиторы контрольных точек, более эффективными.
Что это может значить для будущих терапий
В совокупности исследование представляет ABAT как нечто большее, чем фермент метаболического обслуживания: при раке почки он ведёт себя как встроенный супрессор опухоли, который при восстановлении вызывает стресс в энергетических центрах раковой клетки, высвобождает сигналы опасности и включает внутреннюю «тревогу», привлекающую иммунную систему. Поскольку ABAT часто снижен в опухолях пациентов, стратегии, повышающие его активность — или имитирующие митохондриальные и имуноактивирующие эффекты, которые он вызывает — могут открыть новые терапевтические возможности для продвинутого рака почки, особенно в комбинации с существующими таргетными и иммунотерапиями.
Цитирование: Feng, Y., Cao, S., Cai, T. et al. Gamma-aminobutyric acid transaminase mediates tumor suppression in renal cell carcinoma through the cGAS-STING–interferon-β axis. Sci Rep 16, 13082 (2026). https://doi.org/10.1038/s41598-026-42861-w
Ключевые слова: рак почки, врождённый иммунитет, микроокружение опухоли, митохондрии, сигнализация интерферонов