Clear Sky Science · tr
Gamma-aminobütirik asit transaminazı, cGAS-STING–interferon-β ekseni aracılığıyla böbrek hücreli karsinomada tümör baskılayıcılığı sağlar
Bir Sinir Kimyasalını Kanser Zayıflığına Çevirmek
Böbrek kanseri, özellikle en yaygın türü olan clear cell renal cell carcinoma yayıldığında tedavisi zor bir hastalıktır; genellikle hem kemoterapiye hem de radyoterapiye direnç gösterir. Bu çalışma, beyin kimyasından tanınan ama dikkatten kaçmış bir enzim olan gamma-aminobütirik asit transaminaz (ABAT)’ın böbrek tümörlerine karşı gizli bir müttefik olabileceğini ortaya koyuyor. Araştırmacılar kanser hücreleri içinde bu enzimi artırarak, tümör büyümesini yavaşlatan ve tümörün bağışıklık ortamını yeniden şekillendiren güçlü yerleşik bir bağışıklık alarm sistemini uyandırabildiler.
Böbrek Tümörlerinde Eksik Bir Savunmacı
Ekip, ABAT’ın böbrek kanserinde nasıl davrandığını görmek için büyük hasta veri tabanları ve tümör örneklerini inceleyerek başladı. Sağlıklı dokuda ABAT, sakinleştirici beyin habercisi GABA’yı parçalayarak düzeylerini dengelemeye yardımcı olur. Ancak tümör örneklerinde ABAT düzeyleri çevreleyen normal böbrek dokusuna kıyasla tutarlı şekilde çok daha düşüktü ve en düşük ABAT miktarına sahip hastaların prognozu genellikle daha kötüydu. Bu desen, tümörlerin avantaj sağlamak için ABAT’ı susturuyor olabileceğini düşündürdü. 
Hücresel İzinsiz Giriş Alarmını Uyandırmak
Bir metabolik enzim nasıl bu kadar güçlü bir anti-tümör etki gösterebilir diye anlamak için araştırmacılar ekstra ABAT bulunan ve bulunmayan kanser hücrelerindeki gen aktivitesini karşılaştırdılar. Antiviral savunma sinyalleriyle genellikle açılan genlerde çarpıcı bir artış buldular; özellikle interferon-β tarafından kontrol edilenlerin yükseldiği görüldü. Bu, normalde viral varlığı veya DNA hasarını algılamak için kullanılan doğuştan gelen bir “izinsiz giriş alarmı”nın etkinleştiğine işaret ediyordu. Farklı algılama yollarını engelleyen seçici ilaçlar kullanarak etkiyi cGAS‑STING yoluna bağladılar—hücre içinde DNA yanlış yerde belirdiğinde yanıt veren bir sistem. Bu yol kimyasal olarak kapatıldığında, ABAT artık yüksek interferon-β düzeyleri üretemedi ve tümörleri etkili şekilde baskılayamadı; bu da ABAT’ın kanserle savaşma gücünün bu iç alarm sistemine bağlı olduğunu gösterdi.
Hücresel Enerji Santrallerindeki Stres
ABAT genellikle hücrenin enerji fabrikaları olan mitokondriler içinde yer alır. Yazarlar, ABAT düzeylerini yükseltmenin mitokondri sağlığını bozduğunu keşfettiler: bunların membran potansiyeli düştü, elektron mikroskobunda şekilleri anormal hale geldi ve mitokondriyal DNA parçaları hücre içindeki sıvıya sızdı. Bu kaçan DNA parçaları tam olarak cGAS‑STING’i tetikleyen sinyallerdir. Ekip ayrıca ABAT’ın kanser büyümesi ve bağışıklık alarmlarını baskılama ile ilişkilendirilmiş başka bir enzim olan PRMT5 ile bağlandığını buldu. PRMT5 azaltıldığında STING ve interferon-β aktivitesi arttı; bu da ABAT’ın hem mitokondrileri zarar vererek hem de PRMT5’i karşılayarak alarm yolunun frenlerini kaldırabileceğini düşündürüyor, ancak ayrıntıların tam olarak nasıl işlediği hâlâ çözülecek.
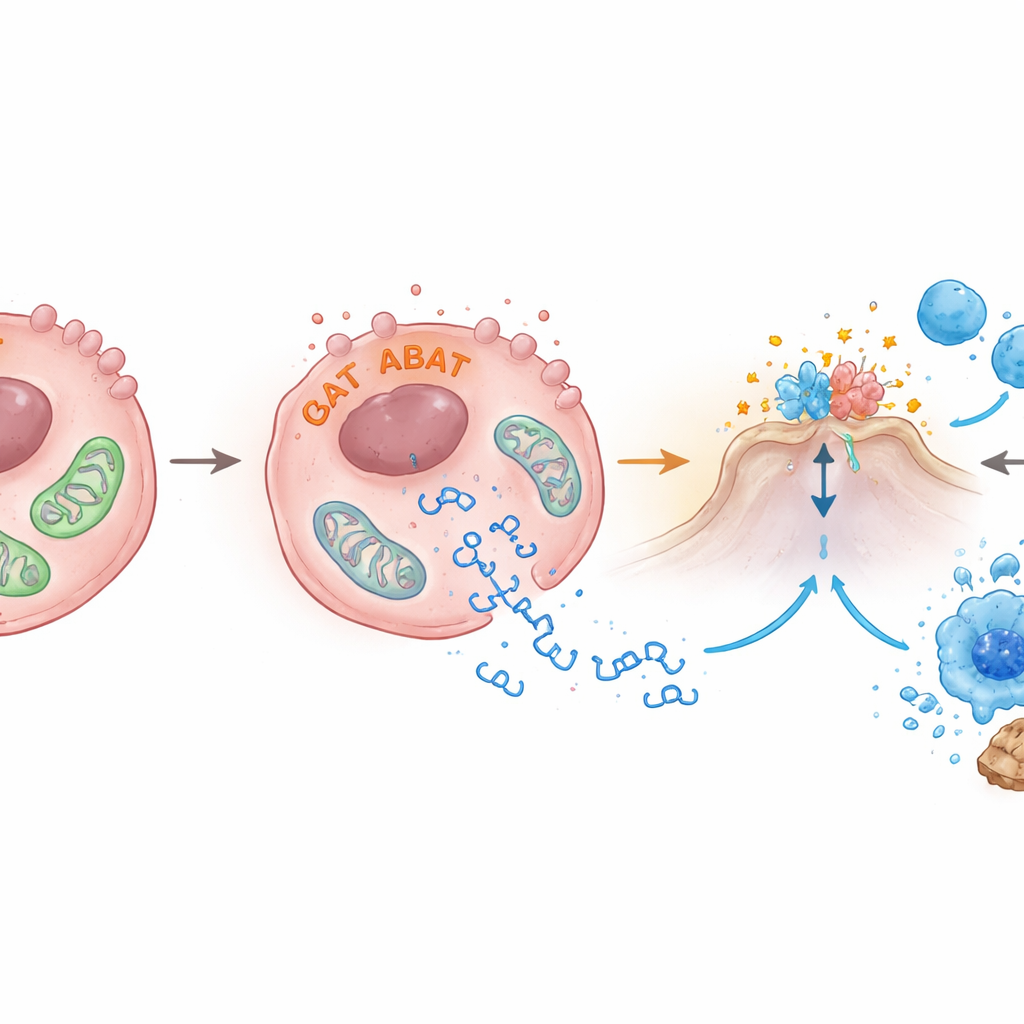
Tümör Çevresindeki Bağışıklık Dengesini Değiştirmek
Kanser izole büyümez; saldırabilecek veya koruyabilecek karmaşık bir bağışıklık hücreleri mahallesinin içinde var olur. Bağışıklık açısından yetkin farelerde, ABAT açısından zengin böbrek kanseri hücrelerinden oluşan tümörler yalnızca daha yavaş büyümekle kalmadı, aynı zamanda farklı bir bağışıklık bileşimine sahipti. Normalde yanıtları yatıştıran ve sıklıkla tümörlerin korunması için sömürdüğü düzenleyici T hücrelerinin oranı belirgin şekilde daha düşüktü; denge, öldürücü T hücreleri lehine kaymıştı. Bu, ABAT’ın interferon ve hasar sinyallerini tetikleyerek yerel bağışıklık ortamını baskıdan uzaklaştırıp anti-tümör etkinliğe yönlendirebileceğini ve muhtemelen kontrol noktası inhibitörleri gibi diğer tedavileri daha etkili hale getirebileceğini düşündürüyor.
Gelecekteki Tedaviler İçin Ne Anlama Gelebilir
Toplamda çalışma, ABAT’ı yalnızca bir metabolik temizlik enzimi olarak değil: böbrek kanserinde restorasyonu yapıldığında tümör baskılayıcı gibi davranan, kanser hücresi enerji santrallerine stres uygulayan, tehlike sinyalleri salan ve bağışıklık sistemini harekete geçiren bir unsur olarak gösteriyor. ABAT hastaların tümörlerinde sıklıkla azaldığı için, onun aktivitesini artıran veya yol açtığı mitokondriyal ve bağışıklık-aktive edici etkileri taklit eden stratejiler, özellikle mevcut hedefe yönelik ve immünoterapilerle kombinasyon halinde, ileri evre böbrek kanseri için yeni tedavi yolları açabilir.
Atıf: Feng, Y., Cao, S., Cai, T. et al. Gamma-aminobutyric acid transaminase mediates tumor suppression in renal cell carcinoma through the cGAS-STING–interferon-β axis. Sci Rep 16, 13082 (2026). https://doi.org/10.1038/s41598-026-42861-w
Anahtar kelimeler: böbrek kanseri, doğal bağışıklık, tümör mikroçevresi, mitokondri, interferon sinyalleşmesi