Clear Sky Science · de
Gamma-Aminobuttersäure-Transaminase vermittelt Tumorunterdrückung beim Nierenzellkarzinom über die cGAS-STING–Interferon-β-Achse
Aus einer Nervenchemikalie eine Krebs-Schwachstelle machen
Nierenkrebs, insbesondere seine häufigste Form, das klarzellige Nierenzellkarzinom, ist nach Metastasierung schwer zu behandeln und spricht oft weder auf Chemotherapie noch auf Strahlung an. Diese Studie zeigt, dass ein in der Gehirnchemie bekanntes, aber bislang wenig beachtetes Enzym – die Gamma-Aminobuttersäure-Transaminase, kurz ABAT – als verbündeter Gegner von Nierentumoren wirken kann. Durch Erhöhen dieses Enzyms in Krebszellen gelang es den Forschern, ein starkes, eingebautes Immunwarnsystem zu aktivieren, das das Tumorwachstum verlangsamt und die Immunlandschaft des Tumors umgestaltet.
Ein fehlender Verteidiger in Nierentumoren
Das Team begann mit der Analyse großer Patientendatenbanken und Tumorproben, um das Verhalten von ABAT beim Nierenkrebs zu untersuchen. Im gesunden Gewebe hilft ABAT beim Abbau des beruhigenden Botenstoffs GABA und hält dessen Spiegel im Gleichgewicht. In Tumorproben jedoch waren die ABAT-Werte durchweg deutlich niedriger als im angrenzenden normalen Nierengewebe, und Patientinnen und Patienten mit den geringsten ABAT-Mengen hatten tendenziell schlechtere Verläufe. Dieses Muster deutete darauf hin, dass Tumoren ABAT möglicherweise stummschalten, um sich einen Vorteil zu verschaffen. 
Die intrazelluläre Alarmanlage wecken
Um zu verstehen, wie ein Stoffwechselenzym eine so starke Anti-Tumor-Wirkung entfalten kann, verglichen die Forscher die Genaktivität in Krebszellen mit und ohne zusätzliches ABAT. Sie fanden einen auffälligen Anstieg jener Gene, die normalerweise durch antivirale Abwehrsignale aktiviert werden, insbesondere solche, die durch das Molekül Interferon-β gesteuert werden. Das deutete auf die Aktivierung einer angeborenen Immun-„Alarmanlage“ hin, die normalerweise auf Viren oder DNA-Schäden reagiert. Mithilfe selektiver Wirkstoffe, die verschiedene Erkennungswege blockieren, führten sie den Effekt auf den cGAS‑STING-Weg zurück – ein zelluläres System, das anspringt, wenn DNA am falschen Ort innerhalb der Zelle auftaucht. Wurde dieser Weg chemisch abgeschaltet, konnte ABAT nicht mehr hohe Interferon‑β-Spiegel treiben oder Tumoren so effektiv unterdrücken, was zeigt, dass seine krebsbekämpfende Wirkung von diesem internen Alarmsystem abhängt.
Stress in den Kraftwerken der Zelle
ABAT sitzt normalerweise in den Mitochondrien, den Energieproduktionsstätten der Zelle. Die Autoren fanden heraus, dass erhöhte ABAT-Spiegel die mitochondriale Gesundheit stören: das Membranpotenzial, das sie antreibt, fiel, ihre Strukturen erschienen unter dem Elektronenmikroskop abnormal, und Fragmente mitochondrialer DNA entkamen in die umgebende intrazelluläre Flüssigkeit. Diese entwichenen DNA-Teile sind genau die Signale, die cGAS‑STING aktivieren. Das Team fand außerdem, dass ABAT an ein anderes Enzym, PRMT5, bindet, das mit Krebswachstum und der Dämpfung von Immunalarmen in Verbindung gebracht wird. Bei verminderter PRMT5-Aktivität stiegen STING- und Interferon‑β-Aktivität an, was darauf hindeutet, dass ABAT sowohl Mitochondrien schädigen als auch PRMT5 entgegenwirken könnte, um die Bremsen des Alarmwegs zu lösen – die genauen Details müssen jedoch noch aufgeklärt werden. 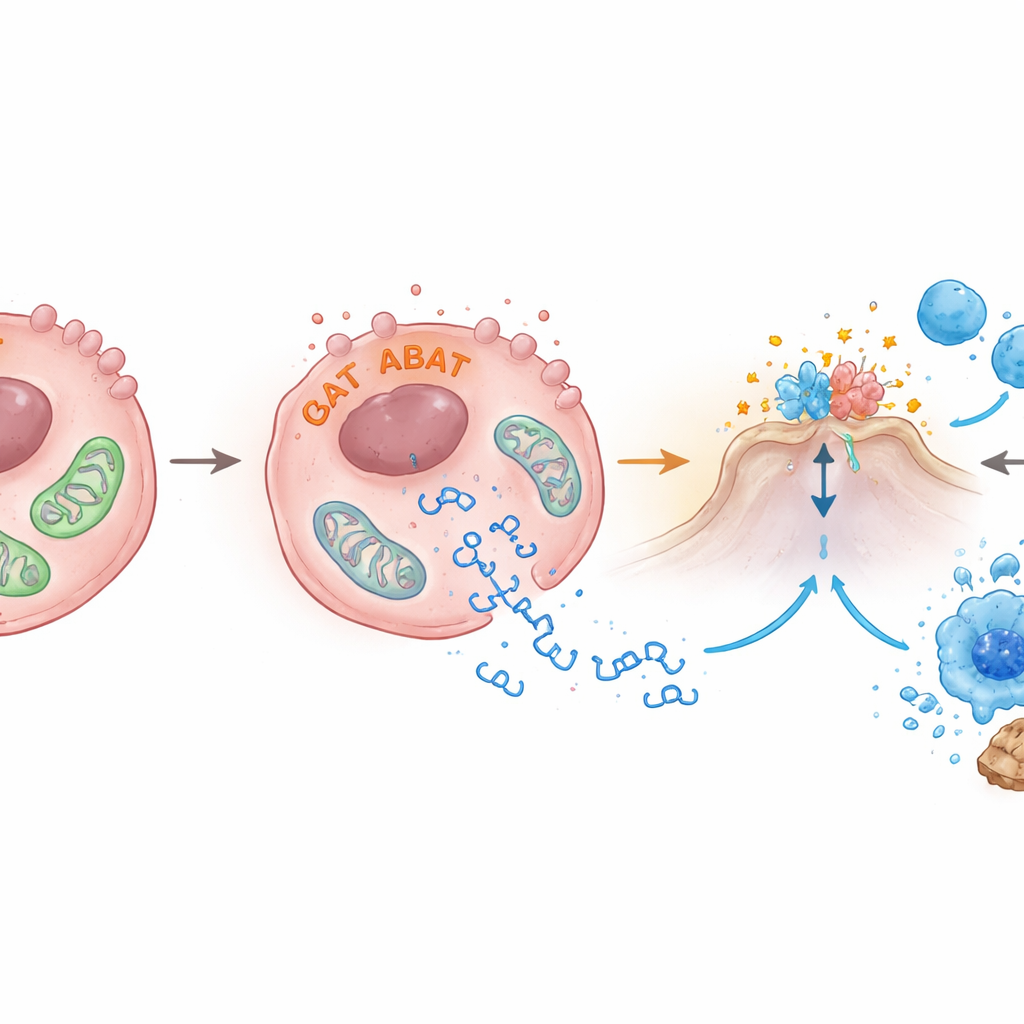
Verschiebung des Immungleichgewichts rund um den Tumor
Krebs wächst nicht isoliert; er existiert in einer komplexen Nachbarschaft von Immunzellen, die ihn angreifen oder schützen können. In immunkompetenten Mäusen wuchsen Tumoren aus ABAT-reichen Nierenkrebszellen nicht nur langsamer, sie zeigten auch eine veränderte Immunzusammensetzung. Der Anteil regulatorischer T-Zellen – jener Immunzellen, die normalerweise Reaktionen dämpfen und von Tumoren oft zur Abschirmung missbraucht werden – war deutlich geringer, während das Gleichgewicht zugunsten zytotoxischer T-Zellen verschoben war. Das legt nahe, dass ABAT durch Auslösen von Interferon- und Schadenssignalen die lokale Immunumgebung von Unterdrückung hin zu antitumoraler Aktivität kippen kann und so möglicherweise andere Behandlungen wie Checkpoint-Inhibitoren wirksamer macht.
Was das für künftige Therapien bedeuten könnte
Insgesamt zeichnet die Studie ABAT nicht nur als normales Stoffwechselhausmeister-Enzym, sondern als eingebautes Tumorsuppressor-Element: Wird es wiederhergestellt, setzt es Mitochondrien unter Stress, setzt Gefahrensignale frei und schaltet eine interne Alarmierung ein, die das Immunsystem mobilisiert. Da ABAT in Patientenproben häufig reduziert ist, könnten Strategien, die seine Aktivität steigern oder die mitochondrialen und immunaktivierenden Effekte nachahmen, neue therapeutische Wege für fortgeschrittenen Nierenkrebs eröffnen – besonders in Kombination mit bestehenden zielgerichteten und immuntherapeutischen Ansätzen.
Zitation: Feng, Y., Cao, S., Cai, T. et al. Gamma-aminobutyric acid transaminase mediates tumor suppression in renal cell carcinoma through the cGAS-STING–interferon-β axis. Sci Rep 16, 13082 (2026). https://doi.org/10.1038/s41598-026-42861-w
Schlüsselwörter: Nierenkrebs, angeborene Immunität, Tumormikroumgebung, Mitochondrien, Interferon-Signalgebung