Clear Sky Science · pt
A transaminase do ácido gama-aminobutírico media supressão tumoral no carcinoma renal de células claras através do eixo cGAS-STING–interferon-β
Transformando um químico nervoso em uma fraqueza do câncer
O câncer renal, especialmente sua forma mais comum chamada carcinoma renal de células claras, é notoriamente difícil de tratar quando se dissemina, frequentemente resistente tanto à quimioterapia quanto à radiação. Este estudo revela que uma enzima pouco considerada, mais conhecida pela atuação na química do cérebro — a transaminase do ácido gama-aminobutírico, ou ABAT — pode funcionar como uma aliada oculta contra tumores renais. Ao aumentar essa enzima dentro das células cancerígenas, os pesquisadores conseguiram despertar um poderoso sistema de alarme imune embutido que retarda o crescimento tumoral e remodela o ambiente imune do tumor.
Um defensor ausente nos tumores renais
A equipe começou examinando grandes bancos de dados de pacientes e amostras tumorais para observar como o ABAT se comporta no câncer renal. Em tecido saudável, o ABAT ajuda a degradar o mensageiro calmante do cérebro, o GABA, mantendo seus níveis em equilíbrio. Nas amostras tumorais, entretanto, os níveis de ABAT foram consistentemente muito mais baixos do que no tecido renal normal adjacente, e pacientes com as menores quantidades de ABAT tenderam a ter pior prognóstico. Esse padrão sugeriu que os tumores podem silenciar o ABAT para ganhar vantagem. 
Despertando o alarme de intruso da célula
Para entender como uma enzima metabólica poderia ter um efeito antitumoral tão forte, os pesquisadores compararam a atividade gênica em células cancerígenas com e sem ABAT extra. Eles encontraram um aumento notável em genes normalmente ativados por sinais de defesa antiviral, especialmente aqueles controlados por uma molécula chamada interferon-β. Isso indicou a ativação de um “alarme de intruso” da imunidade inata normalmente usado para detectar vírus ou danos no DNA. Ao usar fármacos seletivos que bloqueiam diferentes vias de detecção, eles rastrearam o efeito até a via cGAS-STING — um sistema celular que responde quando DNA aparece no lugar errado dentro da célula. Quando essa via foi quimicamente desligada, o ABAT deixou de induzir altos níveis de interferon-β ou de suprimir tumores tão efetivamente, mostrando que seu poder antitumoral depende desse sistema de alarme interno.
Estresse nas usinas de energia da célula
O ABAT normalmente reside nas mitocôndrias, as fábricas de energia da célula. Os autores descobriram que aumentar os níveis de ABAT perturba a saúde mitocondrial: o potencial de membrana que as alimenta caiu, suas formas ficaram anormais em microscopia eletrônica, e fragmentos de DNA mitocondrial vazaram para o fluido ao redor dentro da célula. Esses pedaços de DNA escapados são exatamente o tipo de sinal que ativa cGAS-STING. A equipe também encontrou que o ABAT se liga a outra enzima, PRMT5, que tem sido associada ao crescimento tumoral e à supressão de alarmes imunes. Quando o PRMT5 foi reduzido, a atividade de STING e do interferon-β aumentou, sugerindo que o ABAT pode tanto danificar mitocôndrias quanto contrabalançar o PRMT5 para liberar os freios da via de alarme, embora os detalhes finos ainda precisem ser esclarecidos. 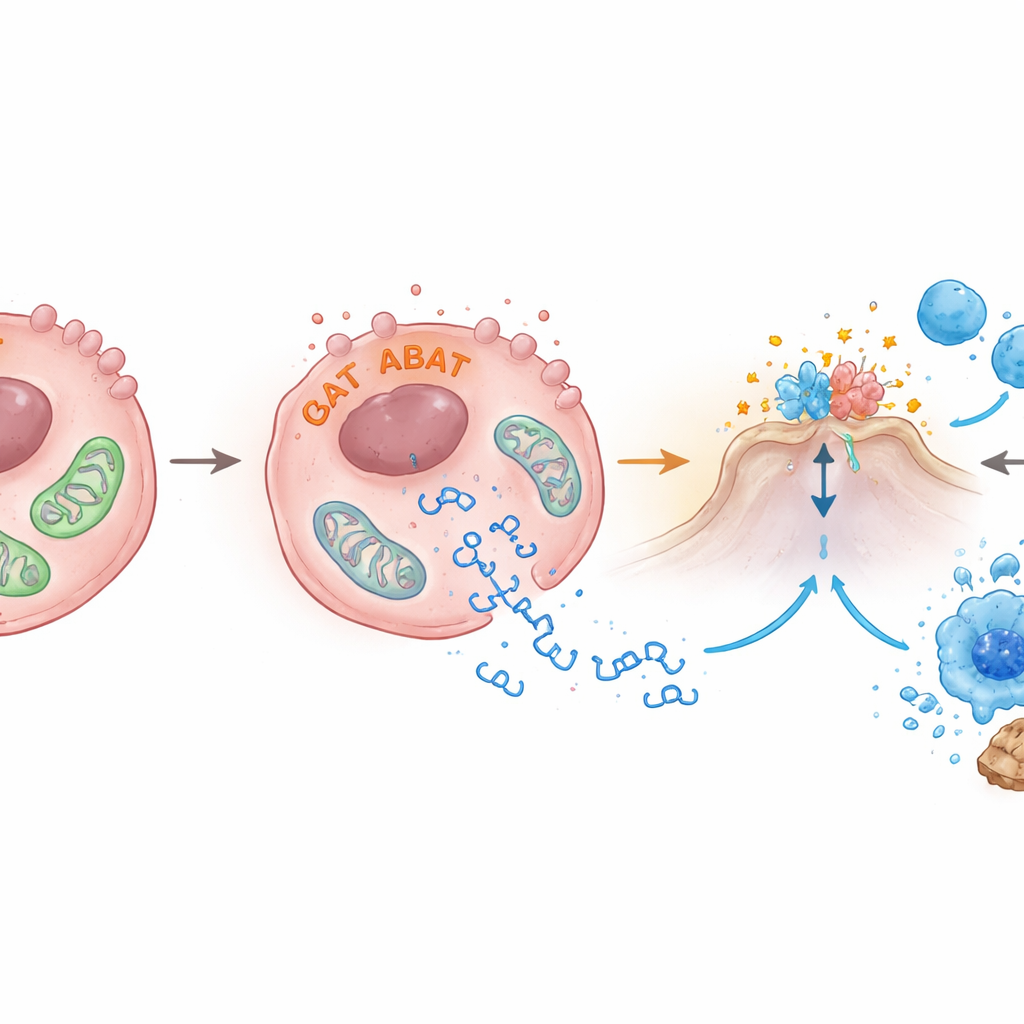
Reequilibrando a resposta imune ao redor do tumor
O câncer não cresce isoladamente; ele vive dentro de um bairro complicado de células imunes que podem tanto atacá-lo quanto protegê-lo. Em camundongos com sistema imune competente, tumores formados por células de câncer renal ricas em ABAT não apenas cresceram mais lentamente, mas também mostraram uma composição imune diferente. A proporção de células T reguladoras — células imunes que normalmente acalmam respostas e são frequentemente cooptadas pelos tumores para se protegerem — foi visivelmente menor, enquanto o equilíbrio mudou a favor de células T citotóxicas. Isso sugere que o ABAT, ao desencadear sinais de interferon e de dano, pode inclinar o ambiente imune local para longe da supressão e em direção à atividade antitumoral, potencialmente tornando outros tratamentos, como inibidores de checkpoint, mais eficazes.
O que isso pode significar para tratamentos futuros
No conjunto, o estudo retrata o ABAT como mais do que uma enzima de manutenção metabólica: no câncer renal ele se comporta como um supressor tumoral embutido que, quando restaurado, causa estresse nas usinas de energia das células cancerígenas, libera sinais de perigo e liga um alarme interno que convoca o sistema imune para agir. Como o ABAT é frequentemente reduzido em tumores de pacientes, estratégias que aumentem sua atividade — ou que imitem os efeitos mitocondriais e ativadores do sistema imune que ele provoca — podem abrir novas vias terapêuticas para câncer renal avançado, especialmente em combinação com terapias alvo e imunoterapias já existentes.
Citação: Feng, Y., Cao, S., Cai, T. et al. Gamma-aminobutyric acid transaminase mediates tumor suppression in renal cell carcinoma through the cGAS-STING–interferon-β axis. Sci Rep 16, 13082 (2026). https://doi.org/10.1038/s41598-026-42861-w
Palavras-chave: câncer de rim, imunidade inata, microambiente tumoral, mitocôndrias, sinalização de interferon