Clear Sky Science · nl
Gamma-aminoboterzuur-transaminase bemiddelt tumorremming bij niercelcarcinoom via de cGAS-STING–interferon-β-as
Een zenuwchemische stof als zwakke plek van kanker
Nierkanker, vooral de meest voorkomende vorm bekend als clear cell niercelcarcinoom, is berucht moeilijk te behandelen zodra het zich verspreidt en weigert vaak zowel chemotherapie als bestraling. Deze studie onthult dat een weinig geziene enzym, vooral bekend uit de hersenchemie—gamma-aminoboterzuur-transaminase, of ABAT—als een verborgen bondgenoot tegen niertumoren kan optreden. Door dit enzym in kankercellen te verhogen, wisten de onderzoekers een krachtig ingebouwd immuunalarm te activeren dat tumorgroei vertraagt en de immuunomgeving van de tumor herstructureert.
Een ontbrekende verdediger in niertumoren
Het team begon met het onderzoeken van grote patiëntendatabases en tumormonsters om te zien hoe ABAT zich gedraagt bij nierkanker. In gezond weefsel helpt ABAT bij de afbraak van de rustgevende boodschapper GABA, waardoor de niveaus in balans blijven. In tumormonsters waren de ABAT-niveaus echter consequent veel lager dan in nabijgelegen normaal nierweefsel, en patiënten met de laagste hoeveelheden ABAT hadden doorgaans een slechtere prognose. Dit patroon suggereert dat tumoren ABAT kunnen stilleggen om een voordeel te behalen. 
Het immuunalarm van de cel wakker maken
Om te begrijpen hoe een metabool enzym zo’n sterke antitumorale werking kan hebben, vergeleken de onderzoekers genactiviteit in kankercellen met en zonder extra ABAT. Ze vonden een opvallende toename van genen die gewoonlijk worden aangeschakeld door antivirale verdedigingssignalen, vooral die onder controle van een molecuul genaamd interferon-β. Dit wees op activatie van een aangeboren immuun “inbreukalarm” dat normaal wordt gebruikt om virussen of DNA-schade te detecteren. Met selectieve geneesmiddelen die verschillende detectieroutes blokkeren, terugvoerden ze het effect naar de cGAS-STING-route—een cellulair systeem dat reageert wanneer DNA op de verkeerde plaats in de cel verschijnt. Wanneer deze route chemisch werd uitgeschakeld, kon ABAT niet langer hoge interferon-β-niveaus opwekken of tumoren even effectief onderdrukken, waarmee werd aangetoond dat zijn kankerbestrijdende kracht afhankelijk is van dit interne alarmsysteem.
Stress in de energiecentrales van de cel
ABAT bevindt zich normaal in de mitochondriën, de energiecentrales van de cel. De auteurs ontdekten dat het verhogen van ABAT-niveaus de mitochondriale gezondheid verstoort: het membraanpotentiaal dat ze aandrijft daalde, hun vormen werden onder elektronenmicroscopie abnormaal en fragmenten van mitochondriaal DNA lekten uit in de omringende vloeistof binnen de cel. Deze ontsnapte DNA-stukjes zijn precies het soort signaal dat cGAS-STING activeert. Het team vond ook dat ABAT bindt aan een ander enzym, PRMT5, dat is gelinkt aan kankergroei en aan het dempen van immuunalarmsignalen. Toen PRMT5 werd verminderd, namen STING- en interferon-β-activiteit toe, wat suggereert dat ABAT zowel mitochondriën kan beschadigen als PRMT5 kan tegenwerken om de rem op de alarmsignaalweg op te heffen, hoewel de precieze details nog verder uitgewerkt moeten worden. 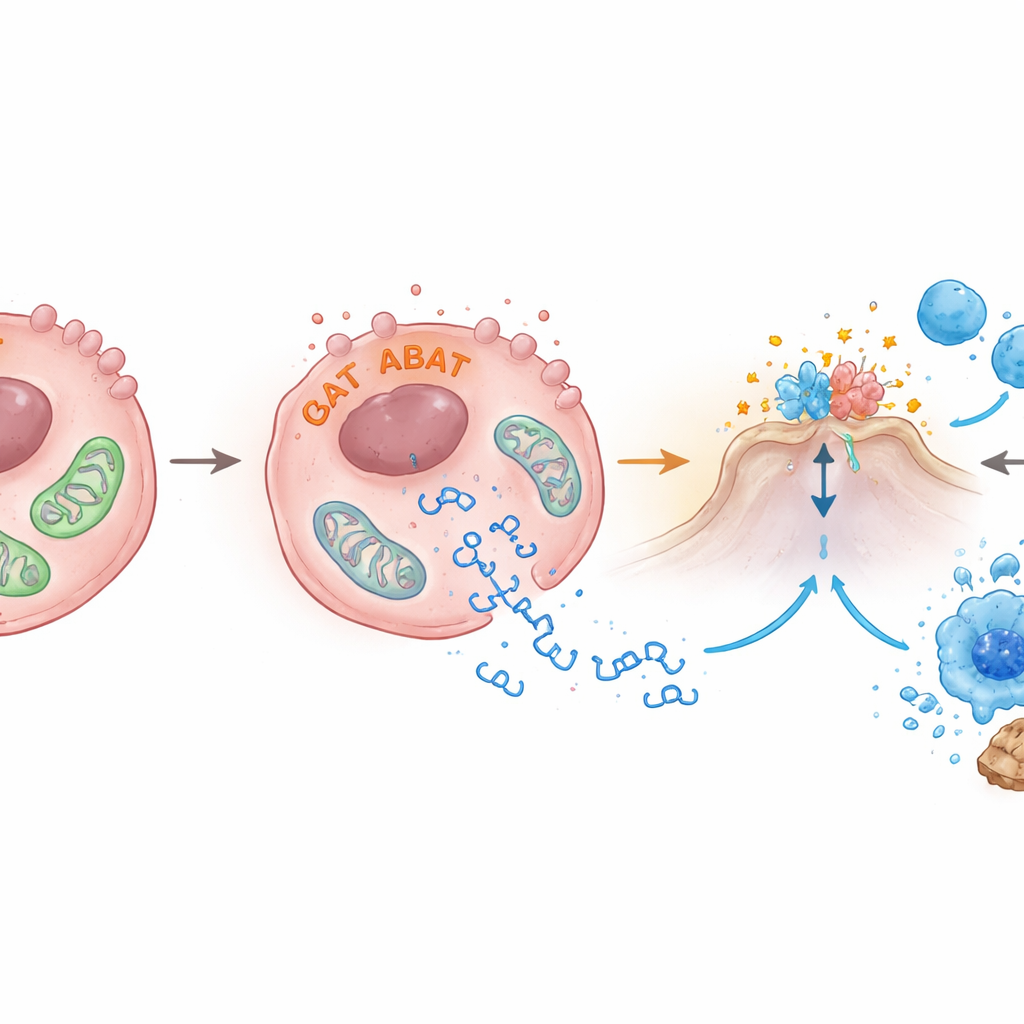
De immuunbalans rond de tumor verschuiven
Kanker groeit niet geïsoleerd; het leeft binnen een gecompliceerde buurt van immuuncellen die haar of aanvallen of beschermen. In immuuncompetente muizen groeiden tumoren die bestonden uit ABAT-rijke nierkankercellen niet alleen langzamer maar vertoonden ze ook een andere immuunsamenstelling. Het aandeel regulerende T-cellen—immuuncellen die normaal reacties kalmeren en vaak door tumoren worden misbruikt om zichzelf te beschermen—was merkbaar lager, terwijl de balans verschoof ten gunste van cytotoxische T-cellen. Dit suggereert dat ABAT, door interferon- en schade-signalen te activeren, de lokale immuunomgeving kan kantelen van onderdrukking naar antitumorale activiteit, wat andere behandelingen zoals checkpointremmers mogelijk effectiever maakt.
Wat dit kan betekenen voor toekomstige behandelingen
Alles bij elkaar portretteert de studie ABAT als meer dan een metabolisch huishoudelijk enzym: bij nierkanker gedraagt het zich als een ingebouwde tumorsuppressor die, wanneer hersteld, stress veroorzaakt in de energiecentrales van kankercellen, gevaarsignalen vrijgeeft en een intern alarm activeert dat het immuunsysteem oproept. Omdat ABAT vaak verlaagd is in patiëntertumoren, kunnen strategieën die de activiteit ervan verhogen—or de mitochondriale en immuunactiverende effecten nabootsen—nieuwe therapeutische wegen openen voor gevorderde nierkanker, vooral in combinatie met bestaande gerichte en immuuntherapieën.
Bronvermelding: Feng, Y., Cao, S., Cai, T. et al. Gamma-aminobutyric acid transaminase mediates tumor suppression in renal cell carcinoma through the cGAS-STING–interferon-β axis. Sci Rep 16, 13082 (2026). https://doi.org/10.1038/s41598-026-42861-w
Trefwoorden: nierkanker, aangeboren immuniteit, tumormicro-omgeving, mitochondriën, interferon-signaleringsweg