Clear Sky Science · it
La transaminasi dell’acido γ‑aminobutirrico media la soppressione tumorale nel carcinoma renale attraverso l’asse cGAS‑STING–interferone‑β
Trasformare un neurotrasmettitore in una vulnerabilità del cancro
Il cancro del rene, in particolare la sua forma più comune chiamata carcinoma renale a cellule chiare, è notoriamente difficile da trattare una volta che si è diffuso, spesso resistente sia alla chemioterapia sia alla radioterapia. Questo studio rivela che un enzima trascurato, noto soprattutto per il suo ruolo nella chimica cerebrale—la transaminasi dell’acido γ‑aminobutirrico, o ABAT—può agire come un alleato nascosto contro i tumori renali. Potenziando questo enzima all’interno delle cellule tumorali, i ricercatori sono riusciti a risvegliare un potente sistema di allarme immunitario intrinseco che rallenta la crescita del tumore e rimodella l’ambiente immunitario del tumore.
Un difensore mancante nei tumori renali
Il gruppo ha iniziato esaminando grandi banche dati di pazienti e campioni tumorali per comprendere il comportamento di ABAT nel cancro del rene. Nei tessuti sani, ABAT aiuta a degradare il messaggero cerebrale calmante GABA, mantenendone l’equilibrio. Nei campioni tumorali, tuttavia, i livelli di ABAT risultavano costantemente molto più bassi rispetto al tessuto renale normale circostante, e i pazienti con le quantità minori di ABAT tendevano ad avere una prognosi peggiore. Questo schema suggeriva che i tumori potessero silenziare ABAT per ottenere un vantaggio. 
Risvegliare l’allarme intruso della cellula
Per capire come un enzima metabolico potesse avere un effetto antitumorale così marcato, i ricercatori hanno confrontato l’attività genica nelle cellule tumorali con e senza ABAT in eccesso. Hanno osservato un incremento netto nei geni generalmente attivati da segnali di difesa antivirale, in particolare quelli controllati da una molecola chiamata interferone‑β. Questo puntava all’attivazione di un “allarme intruso” dell’immunità innata normalmente impiegato per rilevare virus o danni al DNA. Usando farmaci selettivi che bloccano differenti vie di rilevamento, hanno ricondotto l’effetto alla via cGAS‑STING—un sistema cellulare che risponde quando il DNA si trova nel posto sbagliato all’interno della cellula. Quando questa via è stata chimicamente spenta, ABAT non è più riuscita a indurre alti livelli di interferone‑β né a sopprimere efficacemente i tumori, dimostrando che il suo potere antitumorale dipende da questo sistema di allarme interno.
Stress all’interno delle centrali energetiche della cellula
ABAT si localizza normalmente nei mitocondri, le centrali energetiche della cellula. Gli autori hanno scoperto che aumentare i livelli di ABAT altera la funzionalità mitocondriale: il potenziale di membrana che le alimenta si riduce, le loro forme appaiono anomale all’esame con microscopia elettronica e frammenti di DNA mitocondriale fuoriescono nel fluido circostante dentro la cellula. Questi frammenti di DNA sfuggiti sono esattamente il tipo di segnale che attiva cGAS‑STING. Il gruppo ha anche riscontrato che ABAT si lega a un altro enzima, PRMT5, che è stato collegato alla crescita tumorale e alla soppressione degli allarmi immunitari. Quando PRMT5 è stato ridotto, l’attività di STING e dell’interferone‑β è aumentata, suggerendo che ABAT potrebbe sia danneggiare i mitocondri sia contrastare PRMT5 per rimuovere i freni sulla via di allarme, sebbene i dettagli fini debbano ancora essere chiariti. 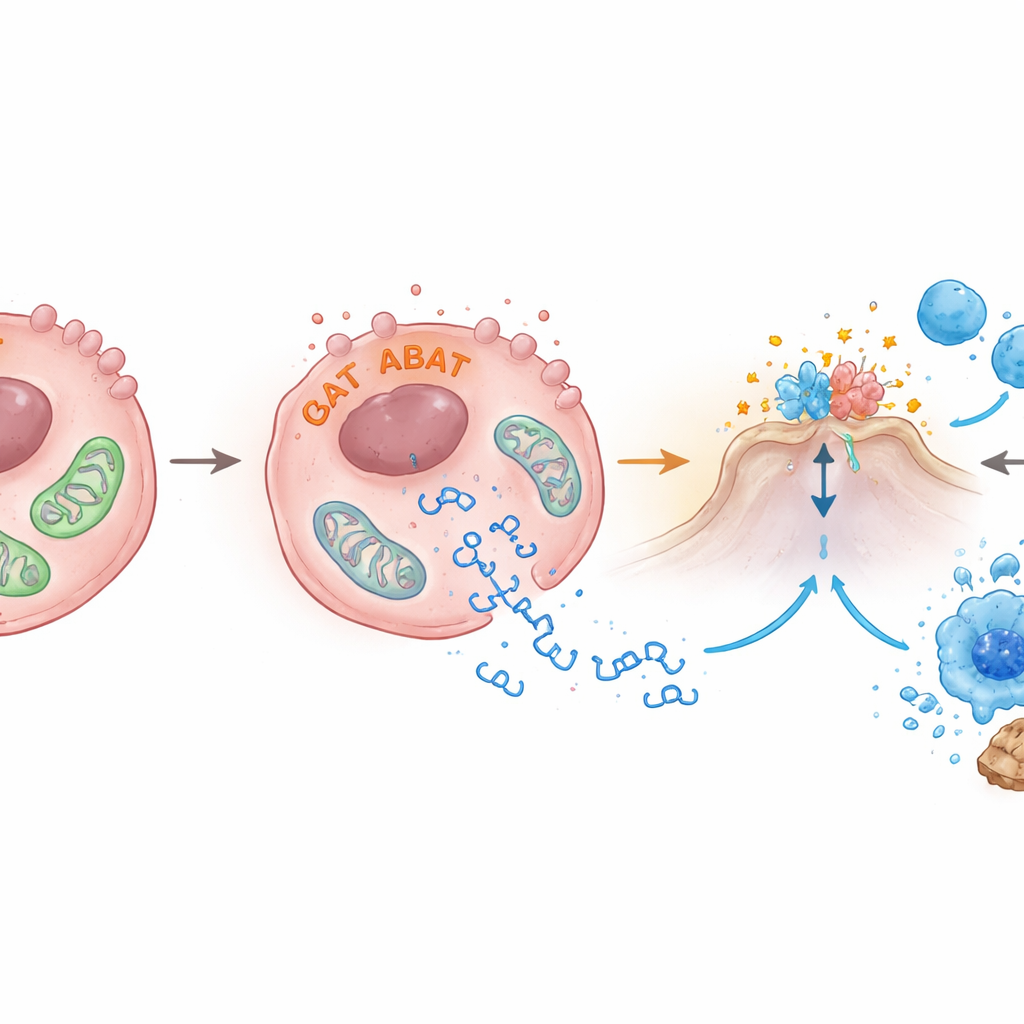
Modificare l’equilibrio immunitario intorno al tumore
Il cancro non cresce isolato; vive in un quartiere complesso di cellule immunitarie che possono attaccarlo o proteggerlo. In topi immunocompetenti, i tumori derivati da cellule di carcinoma renale ricche di ABAT non solo crescevano più lentamente ma mostravano anche una composizione immunitaria diversa. La proporzione di cellule T regolatorie—cellule immunitarie che normalmente attenuano le risposte e sono spesso cooptate dai tumori per proteggersi—era notevolmente più bassa, mentre l’equilibrio si spostava a favore delle cellule T citotossiche. Questo suggerisce che ABAT, attivando segnali di interferone e di danno, può inclinare l’ambiente immunitario locale da uno stato di soppressione verso un’attività antitumorale, potenzialmente rendendo altri trattamenti come gli inibitori dei checkpoint più efficaci.
Cosa potrebbe significare per i trattamenti futuri
Nel complesso, lo studio ritrae ABAT come più di un semplice enzima di manutenzione metabolica: nel cancro del rene si comporta come un soppressore tumorale intrinseco che, una volta ripristinato, infligge stress alle centrali energetiche delle cellule tumorali, rilascia segnali di pericolo e attiva un allarme interno che richiama in azione il sistema immunitario. Poiché ABAT è frequentemente ridotto nei tumori dei pazienti, strategie che ne aumentino l’attività—o che imitino gli effetti mitocondriali e immuno‑attivanti che provoca—potrebbero aprire nuove strade terapeutiche per il carcinoma renale avanzato, specialmente in combinazione con terapie mirate e immunoterapie già esistenti.
Citazione: Feng, Y., Cao, S., Cai, T. et al. Gamma-aminobutyric acid transaminase mediates tumor suppression in renal cell carcinoma through the cGAS-STING–interferon-β axis. Sci Rep 16, 13082 (2026). https://doi.org/10.1038/s41598-026-42861-w
Parole chiave: cancro del rene, immunità innata, microambiente tumorale, mitocondri, segnalazione degli interferoni