Clear Sky Science · sv
Gamma-aminosmörsyra‑transaminas medierar tumörundertryck i njurcellscancer via cGAS‑STING–interferon‑β‑axeln
Att förvandla en nervkemikalie till en cancersvaghet
Njurcancer, särskilt den vanligaste formen klarcellig njurcellscancer, är ökänd för att vara svårbehandlad när den sprider sig och motståndskraftig mot både cytostatika och strålning. Denna studie visar att ett försummat enzym, känt från hjärnans kemi—gamma‑aminosmörsyra‑transaminas, eller ABAT—kan fungera som en dold allierad mot njurtumörer. Genom att öka detta enzym i cancerceller lyckades forskarna väcka ett kraftfullt inbyggt immunlarm som bromsar tumörtillväxt och omformar tumörens immungsmiljö.
En saknad försvarare i njurtumörer
Forskarna började med att granska stora patientdatabaser och tumörprover för att se hur ABAT beter sig i njurcancer. I frisk vävnad hjälper ABAT till att bryta ner den dämpande hjärnkemikalien GABA och håller dess nivåer i balans. I tumörprover var ABAT‑nivåerna dock konsekvent mycket lägre än i intilliggande normal njurvävnad, och patienter med de lägsta mängderna ABAT hade ofta sämre prognos. Detta mönster antydde att tumörer kan tysta ABAT för att vinna fördelar. 
Att väcka cellens inkräktarlarm
För att förstå hur ett metabolt enzym kan ge ett så starkt antitumöreffekt jämförde forskarna genaktivitet i cancerceller med och utan extra ABAT. De fann en påtaglig uppreglering av gener som normalt aktiveras av antivirala försvarssignaler, särskilt sådana som styrs av molekylen interferon‑β. Detta pekade på aktivering av ett medfött immunologiskt ”inkräktarlarm” som normalt används för att upptäcka virus eller DNA‑skador. Genom att använda selektiva läkemedel som blockerar olika sensorvägar spårade de effekten till cGAS‑STING‑vägen—ett cellsystem som reagerar när DNA dyker upp på fel plats inne i cellen. När denna väg kemiskt stängdes av kunde ABAT inte längre driva upp interferon‑β‑nivåerna eller undertrycka tumörer lika effektivt, vilket visar att dess cancerbekämpande kraft är beroende av detta interna larmsystem.
Stress inne i cellens kraftverk
ABAT finns vanligtvis i mitokondrierna, cellens energifabriker. Författarna upptäckte att ökade ABAT‑nivåer stör mitokondriernas hälsa: membranpotentialen som driver dem sjönk, deras form blev onormal vid elektronmikroskopi och fragment av mitokondriellt DNA läckte ut i cellens inre vätska. Dessa undflyende DNA‑delar är precis den typ av signal som aktiverar cGAS‑STING. Teamet fann också att ABAT binder till ett annat enzym, PRMT5, som kopplats till tumörtillväxt och till dämpning av immunsignaler. När PRMT5 minskades ökade STING‑ och interferon‑β‑aktiviteten, vilket antyder att ABAT både kan skada mitokondrier och motverka PRMT5 för att lyfta bromsarna på larmsystemet, även om de exakta detaljerna återstår att klarlägga. 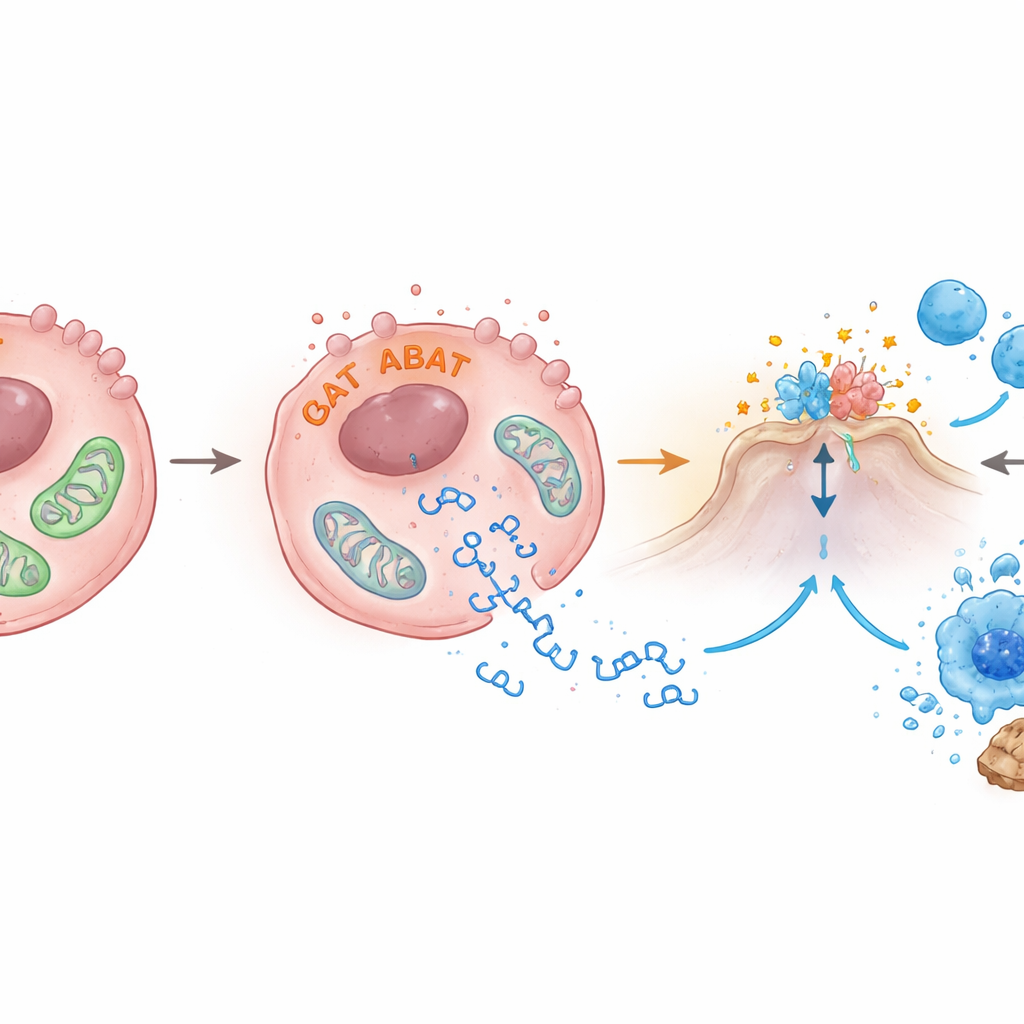
Att förändra immunsaldot runt tumören
Cancer växer inte isolerat; den lever i ett komplicerat grannskap av immunceller som antingen kan attackera eller skydda den. I immunintakta möss växte tumörer som härstammade från ABAT‑rika njurcancerceller inte bara långsammare utan visade också en annorlunda immunprofil. Andelen regulatoriska T‑celler—immunceller som normalt dämpar svar och ofta utnyttjas av tumörer för att skydda sig—var märkbart lägre, medan balansen skiftade till förmån för cytotoxiska T‑celler. Detta tyder på att ABAT, genom att utlösa interferon och skadesignaler, kan tippa den lokala immungsmiljön bort från undertryck och mot antitumöreffekt, vilket potentiellt kan göra andra behandlingar som checkpoint‑hämmare mer effektiva.
Vad detta kan innebära för framtida behandlingar
Sammantaget framställer studien ABAT som mer än ett metabolt hushållsenzym: i njurcancer beter det sig som en inbyggd tumörsuppressor som, när det återställs, åstadkommer stress i cancercellernas kraftverk, släpper ut farosignaler och slår på ett internt larm som kallar in immunsystemet. Eftersom ABAT ofta är nedsatt i patienttumörer kan strategier som ökar dess aktivitet—eller efterliknar de mitokondriella och immunaktiverande effekter det orsakar—öppna nya terapeutiska vägar för avancerad njurcancer, särskilt i kombination med befintliga riktade och immunterapier.
Citering: Feng, Y., Cao, S., Cai, T. et al. Gamma-aminobutyric acid transaminase mediates tumor suppression in renal cell carcinoma through the cGAS-STING–interferon-β axis. Sci Rep 16, 13082 (2026). https://doi.org/10.1038/s41598-026-42861-w
Nyckelord: njurcancer, medfödd immunitet, tumörmikromiljö, mitokondrier, interferonsignalering