Clear Sky Science · pl
Transaminaza kwasu gamma-aminomasłowego pośredniczy w hamowaniu nowotworu w raku nerkowokomórkowym poprzez oś cGAS‑STING–interferon‑β
Przekształcenie neuroprzekaźnika w słabość nowotworu
Rak nerki, a szczególnie jego najczęstsza postać — jasnokomórkowy rak nerkowokomórkowy — jest wyjątkowo trudny do leczenia po rozsiewie, często oporny zarówno na chemioterapię, jak i radioterapię. Badanie to ujawnia, że pomijany enzym znany z chemii mózgu — transaminaza kwasu gamma-aminomasłowego, czyli ABAT — może działać jako ukryty sprzymierzeniec przeciw guzom nerek. Zwiększając poziom tego enzymu w komórkach nowotworowych, naukowcy byli w stanie uruchomić potężny wewnętrzny alarm immunologiczny, który spowalnia wzrost guza i przekształca jego środowisko immunologiczne.
Brakujący obrońca w guzach nerek
Zespół rozpoczął od analizy dużych baz danych pacjentów i próbek guza, aby sprawdzić, jak zachowuje się ABAT w raku nerkowym. W tkance zdrowej ABAT pomaga rozkładać uspokajający przekaźnik mózgowy GABA, utrzymując jego poziomy w równowadze. W próbkach guzów jednak poziomy ABAT były konsekwentnie znacznie niższe niż w pobliskiej zdrowej tkance nerki, a pacjenci z najniższymi ilościami ABAT mieli zwykle gorsze rokowania. Ten wzorzec sugerował, że guzy mogą wyciszać ABAT, by zyskać przewagę. 
Obudzenie komórkowego alarmu przed intruzami
Aby zrozumieć, jak enzym metaboliczny może wywoływać tak silny efekt przeciwnowotworowy, badacze porównali aktywność genów w komórkach nowotworowych z dodatkowymi poziomami ABAT i bez nich. Stwierdzili wyraźny wzrost ekspresji genów zazwyczaj włączanych przez sygnały obrony przeciwwirusowej, zwłaszcza tych kontrolowanych przez cząsteczkę zwaną interferonem‑β. Wskazywało to na aktywację wrodzonego „alarmu” immunologicznego używanego do wykrywania wirusów lub uszkodzeń DNA. Korzystając z selektywnych leków blokujących różne drogi detekcji, zlokalizowali efekt do szlaku cGAS‑STING — systemu komórkowego reagującego, gdy DNA pojawia się w niewłaściwym miejscu wewnątrz komórki. Gdy tę ścieżkę chemicznie wyłączono, ABAT nie był już w stanie indukować wysokich poziomów interferonu‑β ani skutecznie hamować guzów, co pokazuje, że jego przeciwnowotworowa siła zależy od tego wewnętrznego systemu alarmowego.
Stres w elektrowniach komórkowych
ABAT zwykle występuje w mitochondriach, fabrykach energii komórki. Autorzy odkryli, że podwyższenie poziomów ABAT zaburza zdrowie mitochondriów: spadł potencjał błonowy, ich kształty stały się nieprawidłowe w mikroskopii elektronowej, a fragmenty mitochondrialnego DNA przeciekły do płynu wewnątrzkomórkowego. Uciekające kawałki DNA są właśnie tym sygnałem, który uruchamia cGAS‑STING. Zespół odkrył również, że ABAT wiąże się z innym enzymem, PRMT5, który wiązano z wzrostem nowotworu i tłumieniem alarmów immunologicznych. Gdy PRMT5 został zmniejszony, aktywność STING i interferonu‑β wzrosła, co sugeruje, że ABAT może jednocześnie uszkadzać mitochondria i przeciwstawiać się PRMT5, by zdjąć hamulec z drogi alarmowej, choć szczegóły tego mechanizmu wymagają dalszych badań. 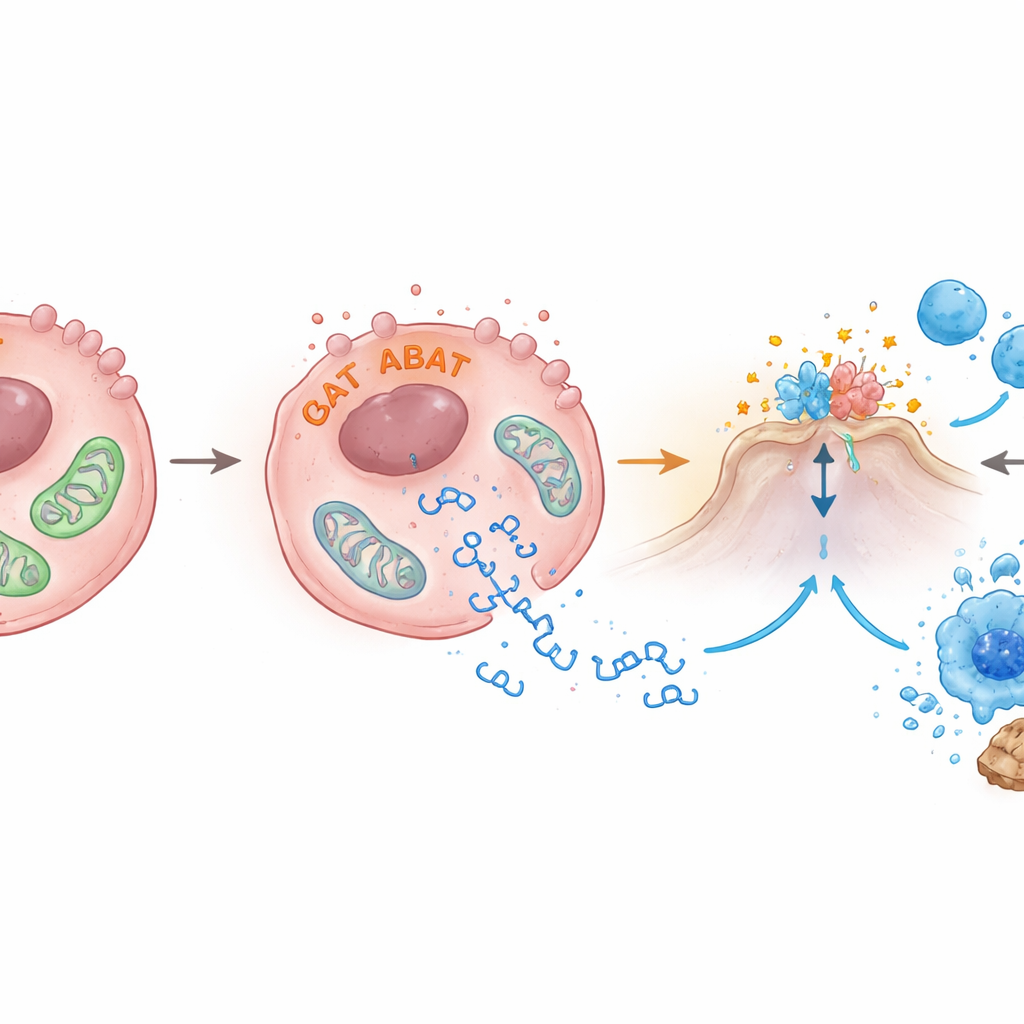
Zmiana równowagi immunologicznej wokół guza
Nowotwór nie rozwija się w izolacji; istnieje w złożonym otoczeniu komórek odpornościowych, które mogą go albo atakować, albo chronić. U myszy z nienaruszonym układem odpornościowym guzy powstałe z komórek raka nerkowego bogatych w ABAT nie tylko rosły wolniej, ale też miały odmienny skład immunologiczny. Udział komórek T regulatorowych — komórek, które normalnie tłumią odpowiedzi i które często są wykorzystywane przez guzy do ochrony — był zauważalnie niższy, podczas gdy równowaga przesunęła się na korzyść cytotoksycznych komórek T. Sugeruje to, że ABAT, poprzez wywołanie sygnałów interferonowych i uszkodzeniowych, może przesunąć lokalne środowisko immunologiczne od stanu supresji w kierunku aktywności przeciwnowotworowej, co potencjalnie zwiększa skuteczność innych terapii, takich jak inhibitory punktów kontrolnych.
Co to może oznaczać dla przyszłych terapii
Podsumowując, badanie ukazuje ABAT jako coś więcej niż enzymu metabolicznego: w raku nerkowym zachowuje się jak wbudowany supresor guza, który po przywróceniu wywołuje stres w elektrowniach komórek, uwalnia sygnały niebezpieczeństwa i włącza wewnętrzny alarm, przywołując układ odpornościowy do działania. Ponieważ ABAT jest często zredukowany w guzach pacjentów, strategie zwiększające jego aktywność — lub naśladujące efekty aktywujące mitochondria i układ odpornościowy, które on powoduje — mogą otworzyć nowe drogi terapeutyczne w zaawansowanym raku nerkowym, zwłaszcza w połączeniu z istniejącymi terapiami ukierunkowanymi i immunoterapiami.
Cytowanie: Feng, Y., Cao, S., Cai, T. et al. Gamma-aminobutyric acid transaminase mediates tumor suppression in renal cell carcinoma through the cGAS-STING–interferon-β axis. Sci Rep 16, 13082 (2026). https://doi.org/10.1038/s41598-026-42861-w
Słowa kluczowe: rak nerki, odporność wrodzona, mikrośrodowisko guza, mitochondria, sygnalizacja interferonowa