Clear Sky Science · ar
توسط ناقلة أمينة غاما، تثبط الورم في سرطان الكلية عبر محور cGAS‑STING–الإنترفيرون‑β
تحويل مادة عصبية إلى نقطة ضعف سرطانية
سرطان الكلية، وخاصة شكله الأكثر شيوعًا المعروف بسرطان الخلايا الكلوية الصفائحية، يصعب علاجه بشدة بعد انتشاره، وغالبًا ما يقاوم كلًا من العلاج الكيميائي والإشعاعي. تكشف هذه الدراسة أن إنزيمًا مهملًا إلى حد ما ومعروفًا أساسًا في كيمياء الدماغ — ناقلة أمين غاما أو ABAT — يمكن أن يعمل كحليف خفي ضد أورام الكلية. بزيادة هذا الإنزيم داخل الخلايا السرطانية، تمكن الباحثون من إيقاظ نظام إنذار مناعي داخلي قوي يبطئ نمو الورم ويُعيد تشكيل البيئة المناعية المحيطة به.
مدافع مفقود في أورام الكلية
بدأ الفريق بفحص قواعد بيانات كبيرة وعينات من الأورام ليروا كيف يتصرف ABAT في سرطان الكلية. في الأنسجة السليمة، يساعد ABAT على تحلل الناقل العصبي المهدئ GABA، محافظًا على توازنه. أما في عينات الأورام، فكانت مستويات ABAT أقل بكثير باستمرار مقارنةً بالأنسجة الكلوية الطبيعية المجاورة، وكان المرضى ذوو المستويات الأدنى من ABAT يميلون إلى نتيجة أسوأ. أقرت هذه الظاهرة أن الأورام قد تكبت ABAT للحصول على ميزة. 
إيقاظ إنذار الدخلاء الخلوي
لفهم كيف يمكن لإنزيم أيضي أن يمتلك تأثيرًا مضادًا للورم بهذه القوة، قارن الباحثون نشاط الجينات في الخلايا السرطانية مع وبدون زيادة ABAT. وجدوا ارتفاعًا لافتًا في الجينات التي عادة ما تُفعل بإشارات الدفاع المضاد للفيروسات، وخاصة تلك التي يتحكم بها جزيء يُدعى الإنترفيرون‑β. أشارت هذه النتائج إلى تنشيط "إنذار الدخلاء" المناعي الفطري الذي يُستخدم عادة لاستشعار الفيروسات أو تلف الحمض النووي. باستخدام أدوية انتقائية تحجب مسارات استشعار مختلفة، تتبعوا التأثير إلى مسار cGAS‑STING — وهو نظام خلوي يستجيب عند ظهور الحمض النووي في مكان خاطئ داخل الخلية. عندما أُغلق هذا المسار كيميائيًا، لم يعد ABAT قادرًا على دفع مستويات مرتفعة من الإنترفيرون‑β أو كبح الأورام بفعالية، مما يُظهر أن قوته المضادة للسرطان تعتمد على هذا النظام الإنذاري الداخلي.
ضغط داخل مصانع طاقة الخلية
يعيش ABAT عادة داخل الميتوكوندريا، مصانع طاقة الخلية. اكتشف المؤلفون أن رفع مستويات ABAT يزعج صحة الميتوكوندريا: انخفض الجهد الغشائي الذي يمدها بالطاقة، وأصبحت أشكالها غير طبيعية تحت المجهر الإلكتروني، وتسربت شظايا من الحمض النووي الميتوكوندري إلى السائل المحيط داخل الخلية. هذه القطع المُسربة من الحمض النووي هي بالضبط الإشارة التي تُفعّل cGAS‑STING. وجد الفريق أيضًا أن ABAT يرتبط بإنزيم آخر، PRMT5، المرتبط بنمو السرطان وكبح الإنذارات المناعية. عندما نُقص PRMT5، ازداد نشاط STING والإنترفيرون‑β، مما يوحي بأن ABAT قد يسبب تلفًا في الميتوكوندريا ويعاكس عمل PRMT5 لرفع كبح مسار الإنذار، رغم أن التفاصيل الدقيقة لا تزال بحاجة إلى توضيح. 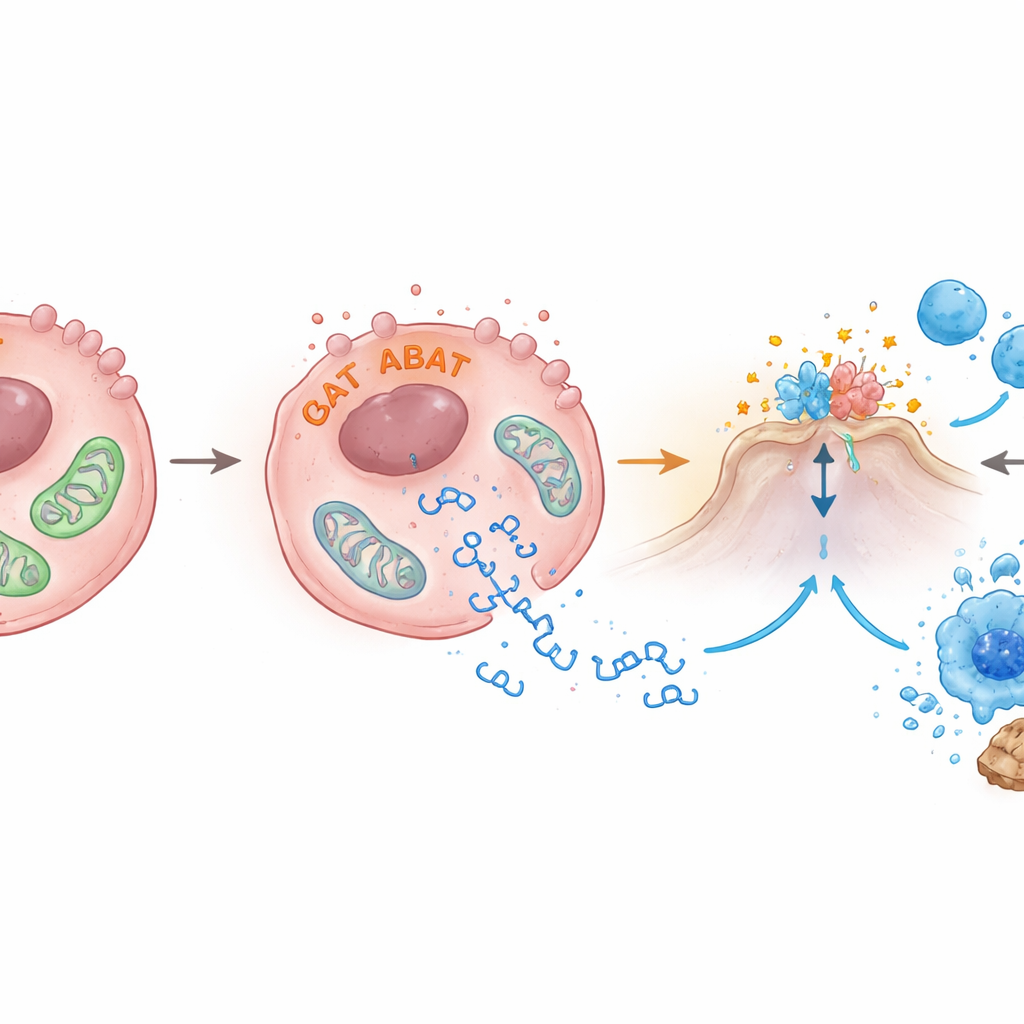
تحويل التوازن المناعي حول الورم
لا ينمو السرطان بمعزل؛ بل يعيش داخل حي معقد من الخلايا المناعية التي يمكن أن تهاجمه أو تحميه. في الفئران ذات المناعة السليمة، لم تكن الأورام المصنوعة من خلايا سرطان الكلية الغنية بـABAT أسرع نموًا فحسب، بل أظهرت أيضًا تركيبًا مناعيًا مختلفًا. كانت نسبة الخلايا التائية المنظمة — الخلايا المناعية التي تُهدئ الاستجابات وغالبًا ما تستغلها الأورام لتحمي نفسها — أقل بشكل ملحوظ، بينما انحرف التوازن لصالح الخلايا التائية القاتلة. يشير هذا إلى أن ABAT، عبر تحفيز إشارات الإنترفيرون والخطر، يمكن أن يقلب البيئة المناعية المحلية بعيدًا عن القمع ونحو النشاط المضاد للورم، مما قد يجعل علاجات أخرى مثل مثبطات نقاط التفتيش أكثر فعالية.
ما الذي قد يعنيه هذا للعلاجات المستقبلية
بشكل إجمالي، تصور الدراسة ABAT كأكثر من إنزيم صيانَة أيضي: ففي سرطان الكلية يتصرف ككابح ورمي مدمج، فعند استعادته يسبب إجهادًا في مصانع طاقة الخلايا السرطانية، ويطلق إشارات الخطر، ويشغّل إنذارًا داخليًا يستدعي الجهاز المناعي إلى العمل. وبما أن ABAT يقل كثيرًا في أورام المرضى، قد تفتح الاستراتيجيات التي تزيد نشاطه — أو تحاكي التأثيرات الميتوكوندرية والمنشطة للمناعة التي يسببها — طرقًا علاجية جديدة لسرطان الكلية المتقدم، خاصةً بالتكامل مع العلاجات المستهدفة والمناعية الحالية.
الاستشهاد: Feng, Y., Cao, S., Cai, T. et al. Gamma-aminobutyric acid transaminase mediates tumor suppression in renal cell carcinoma through the cGAS-STING–interferon-β axis. Sci Rep 16, 13082 (2026). https://doi.org/10.1038/s41598-026-42861-w
الكلمات المفتاحية: سرطان الكلية, المناعة الفطرية, بيئة الورم الدقيقة, الميتوكوندريا, إشارة الإنترفيرون